2026年3月19日,由中山大学孙逸仙纪念医院宋尔卫院士团队领衔的全球多中心I期临床试验HORIZON-X最终分析结果在Signal Transduction and Targeted Therapy上发表,题为“SHR-A1811, a novel HER2-targeting antibody-drug conjugate, in advanced solid tumors (HORIZON-X): a global phase 1 trial”。
该研究旨在评估新型HER2靶向抗体药物偶联物SHR-A1811在经治HER2表达或突变晚期实体瘤患者中的安全性与疗效。结果显示,SHR-A1811在HER2阳性乳腺癌中的中位无进展生存期为25.0个月,HER2低表达乳腺癌11.0个月,非乳腺肿瘤3.5-17.2个月,安全性可控。该研究进一步确认了SHR-A1811作为HER2靶向治疗新选择的重要价值。

研究背景
抗体药物偶联物(ADC)被誉为“生物导弹”,通过将高毒性载荷精准递送至肿瘤细胞,实现了高效低毒的治疗目标。以德曲妥珠单抗(T-DXd) 为代表的HER2靶向ADC已在乳腺癌、胃癌、肺癌等多个瘤种中取得成功。然而,药物间质性肺病(ILD)的发生以及耐药性的出现仍是临床面临的挑战。 SHR-A1811(trastuzumab rezetecan)是一种新型HER2靶向ADC,由抗HER2抗体曲妥珠单抗通过可裂解连接子与拓扑异构酶I抑制剂载荷SHR169265偶联而成。其药物抗体比(DAR)为6,具有优异的膜通透性和旁观者效应,且在血浆中稳定性良好(载荷释放率<1%),这些特性赋予了其潜在的更好安全性和更强效的肿瘤杀伤能力。 HORIZON-X(NCT04446260)是一项全球、多中心、首次人体、I期临床试验。其主要分析已于2024年发表,本文为该研究的长期随访最终分析,重点关注了无进展生存期和缓解持续时间等关键次要终点。 研究设计
HORIZON-X研究在38家研究中心开展,研究分为剂量递增、药代动力学扩展和适应症扩展三个部分。 入组标准:年龄≥18岁,不可切除、晚期或转移性HER2表达(IHC 1+、2+、3+)或突变的实体瘤患者,经标准治疗后进展或不耐受;东部肿瘤协作组体能状态评分(ECOG PS)0~1分,至少有1个根据实体瘤疗效评价标准(RECIST v1.1)可测量的病灶;排除活动性中枢神经系统转移、有临床意义的肺部疾病(如间质性肺炎、肺纤维化)的患者。 给药方案:SHR-A1811通过静脉输注给药,剂量范围为1.0至8.0 mg/kg,每三周(Q3W)一次。 研究终点:主要终点包括剂量限制性毒性(DLT)、安全性和推荐II期剂量(RP2D)。次要终点包括客观缓解率(ORR)、缓解持续时间(DOR)、无进展生存期(PFS)、疾病控制率(DCR)、药代动力学和免疫原性。 研究方案 患者入组流程 研究结果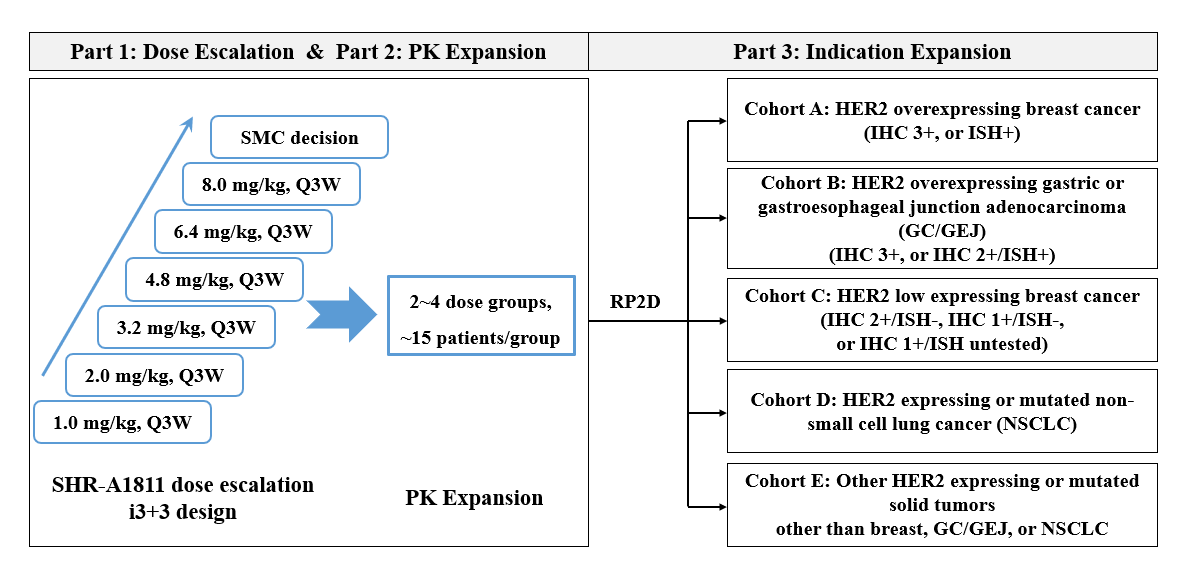
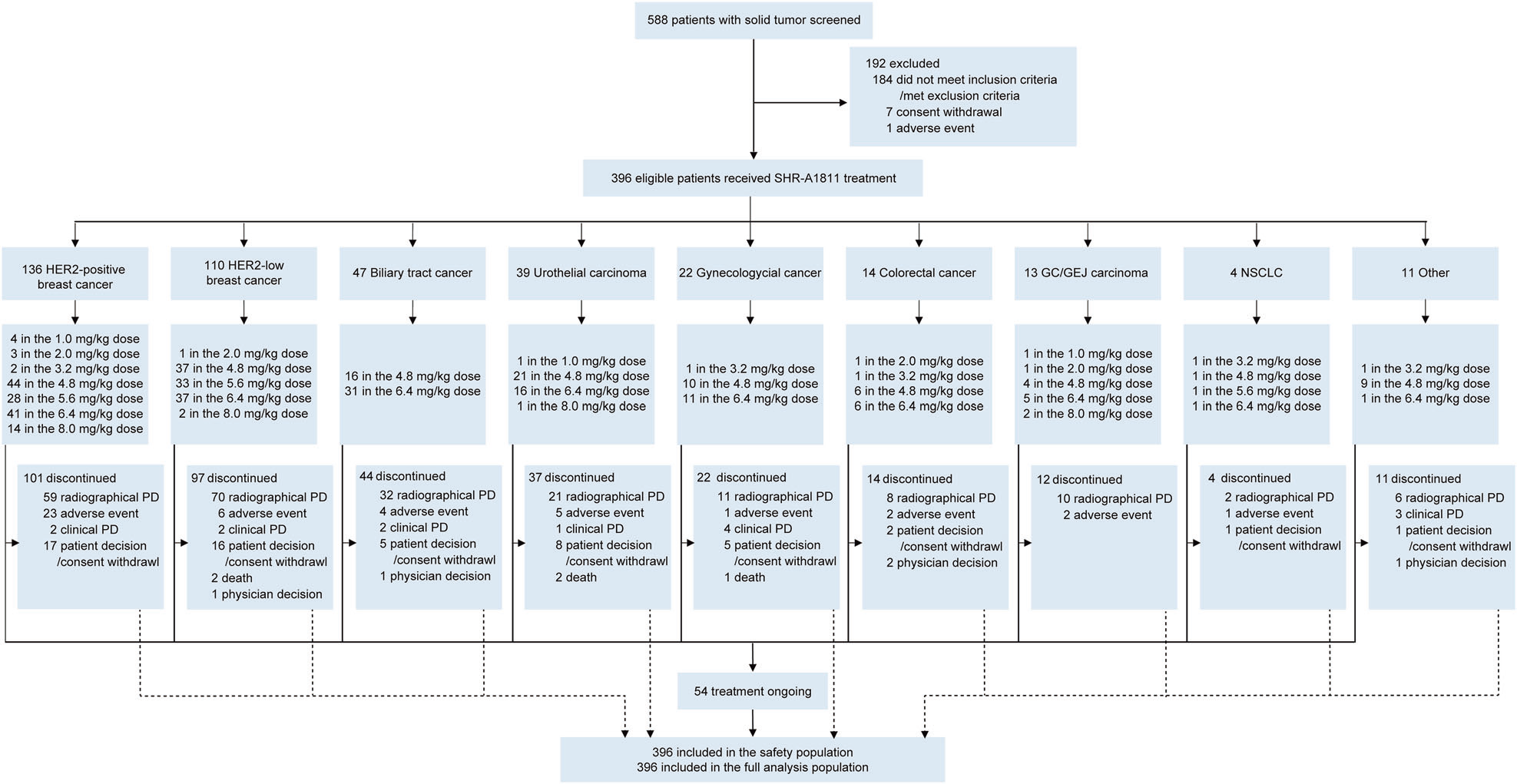
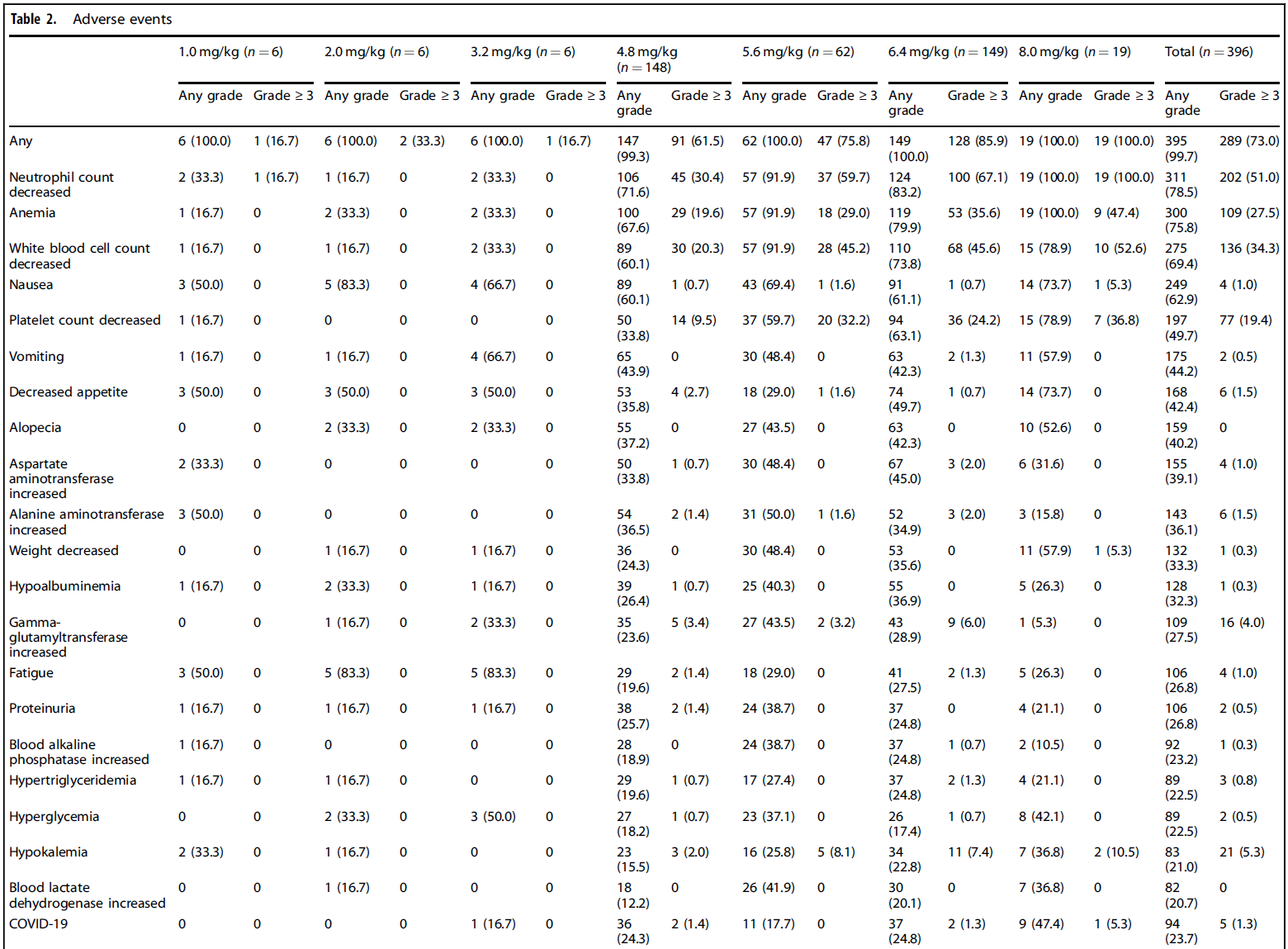
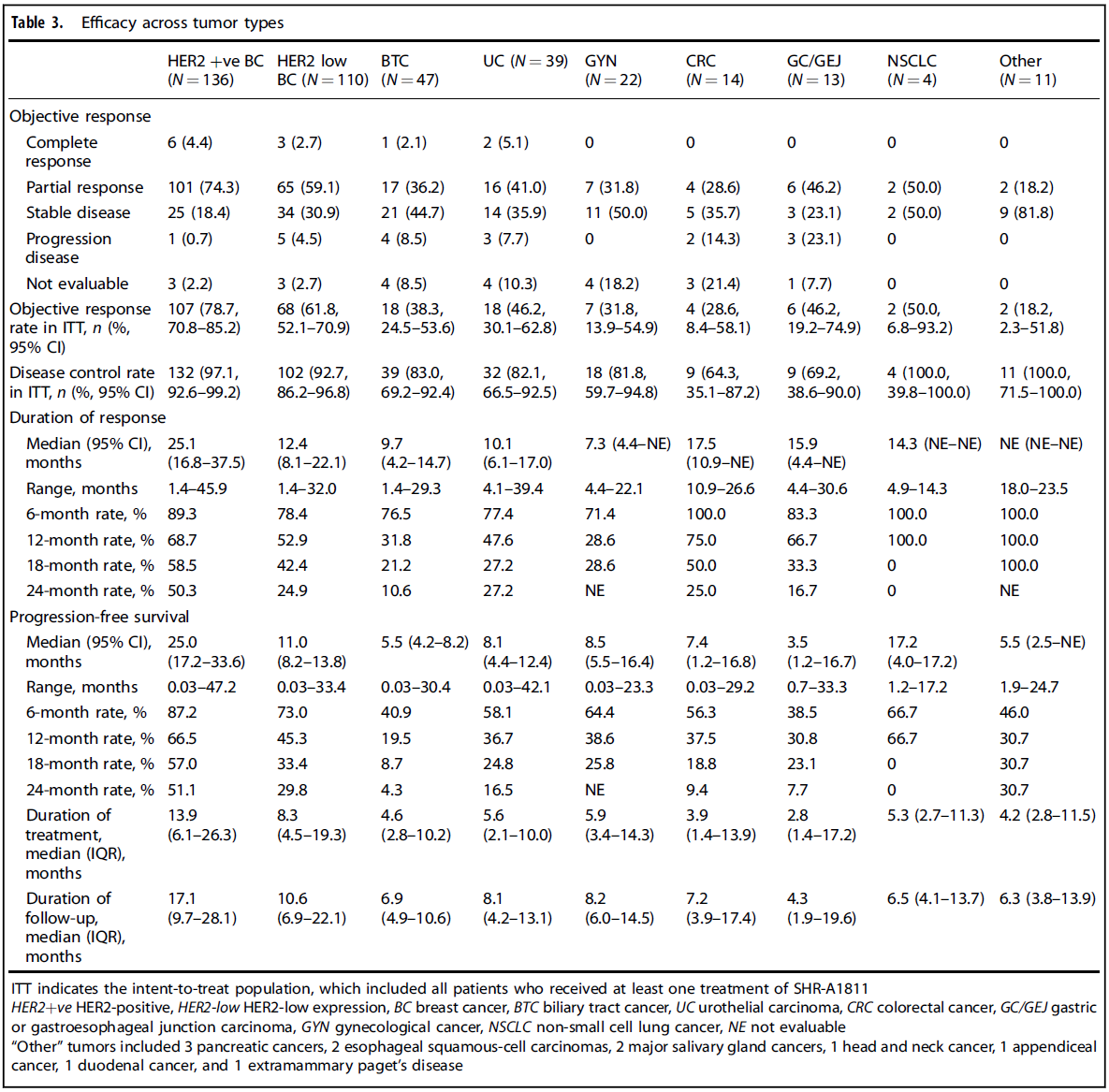
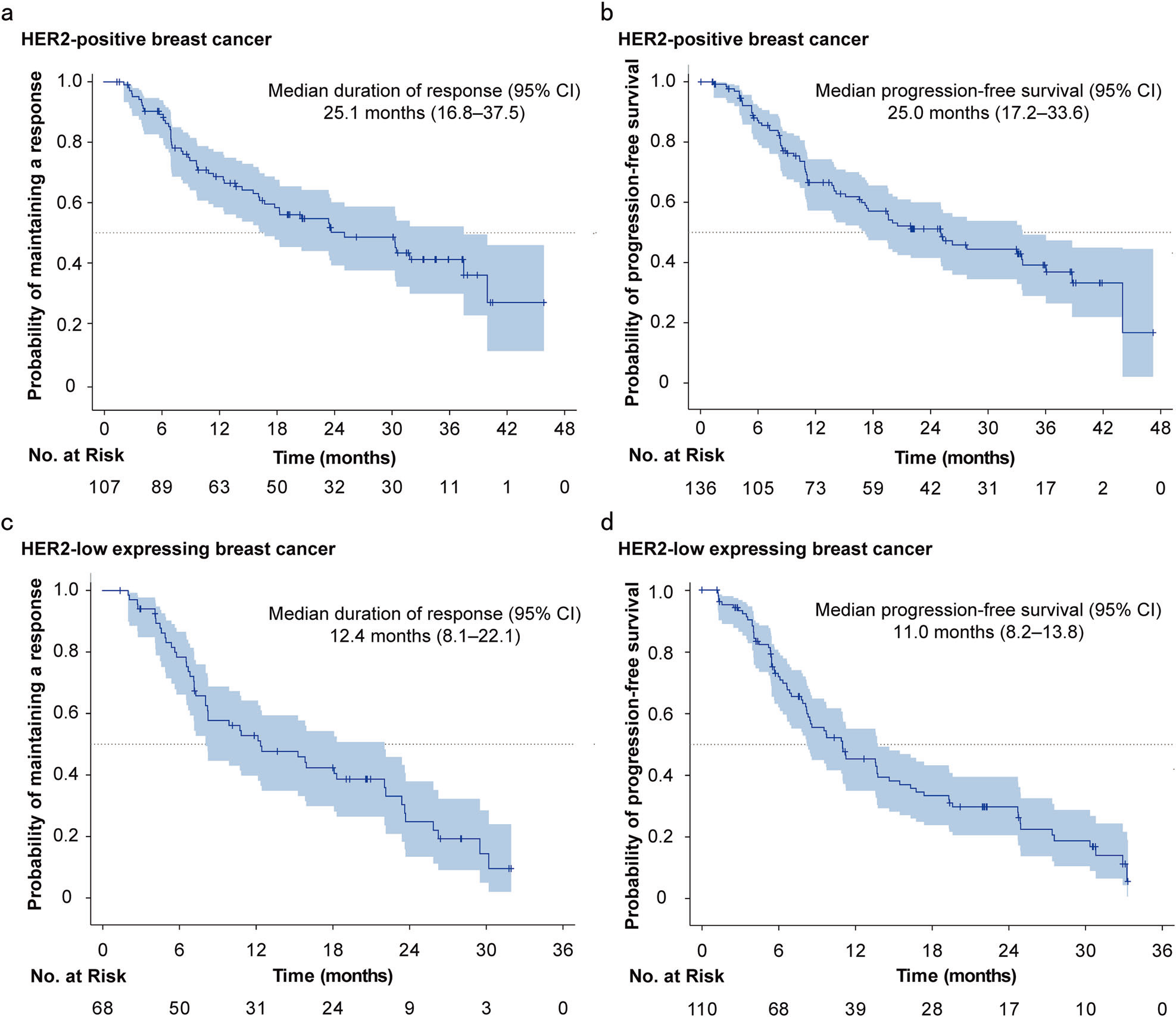
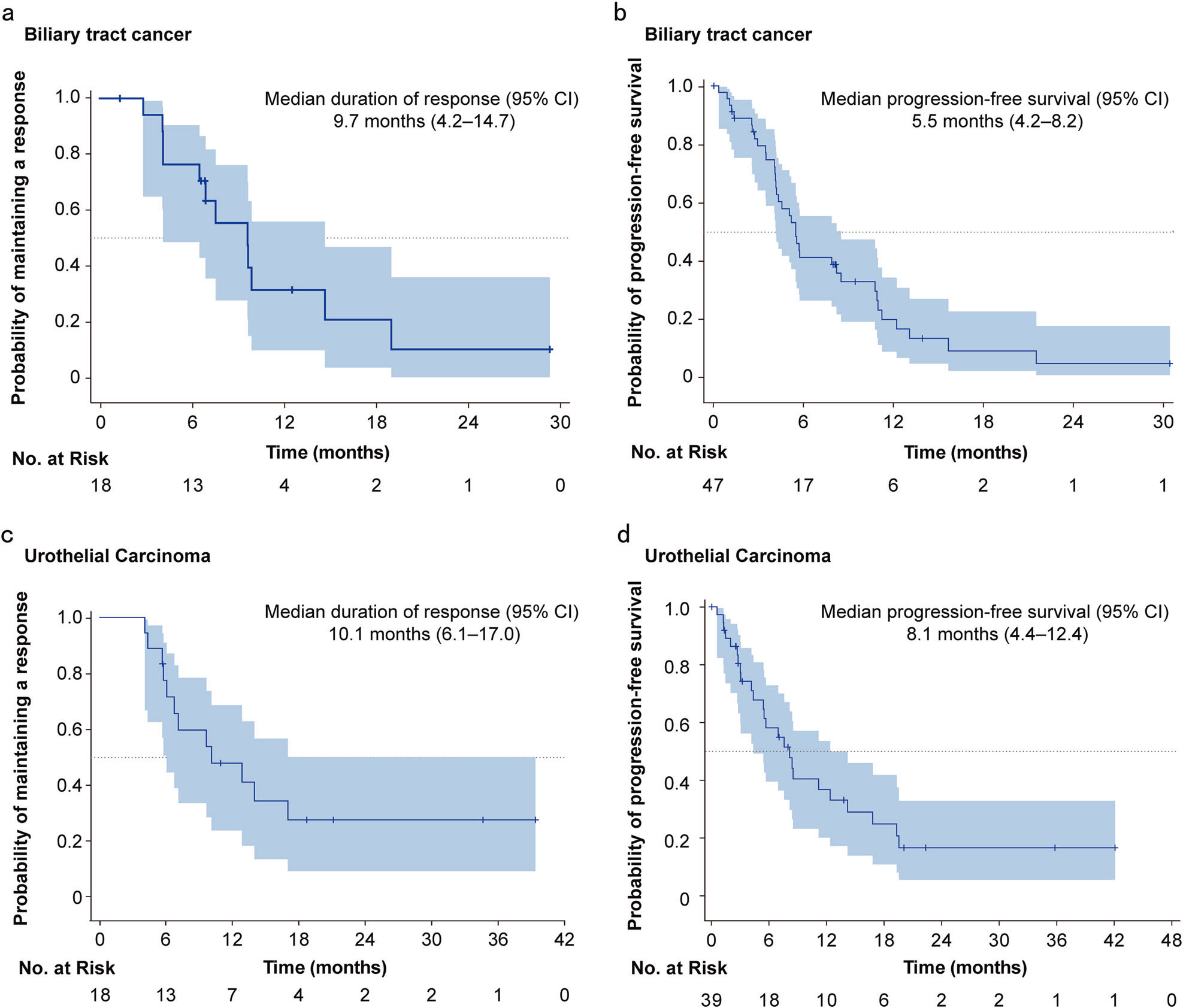
2020年9月7日-2024年6月4日,共588例患者接受筛选,最终396例符合标准的患者入组(中位既往治疗方案数为3线[IQR 2-5])。其中剂量递增阶段35例,扩展阶段361例(新纳入89例)。最终分析的肿瘤类型队列包括: HER2阳性乳腺癌(n=136) HER2低表达乳腺癌(n=110) 胆道癌(BTC, n=47) 尿路上皮癌(UC, n=39) 妇科肿瘤(GYN, n=22,含卵巢癌、宫颈癌、子宫内膜癌等) 结直肠癌(CRC, n=14) 胃/胃食管结合部腺癌(GC/GEJ, n=13) 非小细胞肺癌(NSCLC, n=4) 其他癌种(n=11) 各队列患者基线特征 截至2025年3月12日数据截止,HER2阳性乳腺癌患者的中位随访时间为17.1个月,HER2低表达乳腺癌为10.6个月,非乳腺癌为4.3-8.2个月。 安全性分析 SHR-A1811的中位药物暴露时间在HER2阳性乳腺癌中为13.9个月,HER2低表达乳腺癌为8.3个月,非乳腺癌为2.8-5.9个月。安全性特征与既往报告保持一致,延长随访未发现新的安全信号。 总体不良事件:395例(99.7%)患者出现不良事件。 治疗相关不良事件(TRAEs):391例(98.7%)患者报告了任意级别的TRAEs。最常见的是中性粒细胞计数降低(77.8%)、贫血(73.7%)和白细胞计数降低(68.9%)。 ≥3级TRAEs:发生在261例(65.9%)患者中。严重不良事件(SAEs)发生率为20.2%,主要为血小板计数降低(9.1%)、贫血(4.3%)和中性粒细胞计数降低(3.8%)。 剂量调整与停药:TRAEs导致138例(34.8%)患者剂量降低,162例(40.9%)患者治疗中断。仅有34例(8.6%)患者因SHR-A1811相关的TRAEs而永久停药。 间质性肺病(ILD):仅在10例(2.5%)患者中观察到ILD。其中7例为低级别(1-2级),2例为3级(分别在4.8 mg/kg和5.6 mg/kg剂量组),1例为致死性事件(在8.0 mg/kg剂量组)。 各队列不良事件 疗效分析 PFS: 总人群:中位PFS为11.1个月(95%CI 10.3-13.8)。 HER2阳性乳腺癌:中位PFS达25.0个月(95%CI 17.2-33.6)。 HER2低表达乳腺癌:中位PFS为11.0个月(95%CI 8.2-13.8)。 非乳腺癌:胆道癌为5.5个月,尿路上皮癌为8.1个月,妇科肿瘤为8.5个月,结直肠癌为7.4个月,胃/胃食管结合部腺癌为3.5个月,非小细胞肺癌为17.2个月。 ORR与DOR: 总人群:确定的ORR为58.6%(12例完全缓解,220例部分缓解)。中位DOR为16.2个月。 HER2阳性乳腺癌:ORR为78.7%(95%CI 70.8-85.2),中位DOR达25.1个月。 HER2低表达乳腺癌:ORR为61.8%(95%CI 52.1-70.9),中位DOR为12.4个月。 非乳腺癌:胆道癌为38.3%,尿路上皮癌ORR为46.2%,妇科肿瘤为31.8%,结直肠癌为28.6%,胃/胃食管结合部腺癌为46.2%,非小细胞肺癌为50.0%。 各队列疗效结果 Kaplan-Meier曲线:乳腺癌人群PFS和DOR Kaplan-Meier曲线:非乳腺癌人群PFS和DOR 特殊亚组分析: 肝转移患者:在伴肝转移的乳腺癌患者中,肿瘤缓解同样持久。HER2阳性乳腺癌肝转移患者的中位DOR为30.4个月,中位PFS为27.8个月;HER2低表达乳腺癌肝转移患者的中位DOR为10.8个月,中位PFS为10.9个月。 脑转移患者:在基线伴有脑转移的患者中,SHR-A1811在HER2阳性乳腺癌中实现了14.1个月的中位PFS,在HER2低表达乳腺癌中实现了8.5个月的中位PFS。 HER2超低/阴性表达(HER2-ultralow/null):探索性分析纳入了54例中心实验室确认为HER2超低/阴性(IHC 0)的患者。尽管HER2表达极低,SHR-A1811在该亚组中仍显示出令人鼓舞的疗效,确认的ORR为59.3%,中位PFS为9.8个月。 研究结论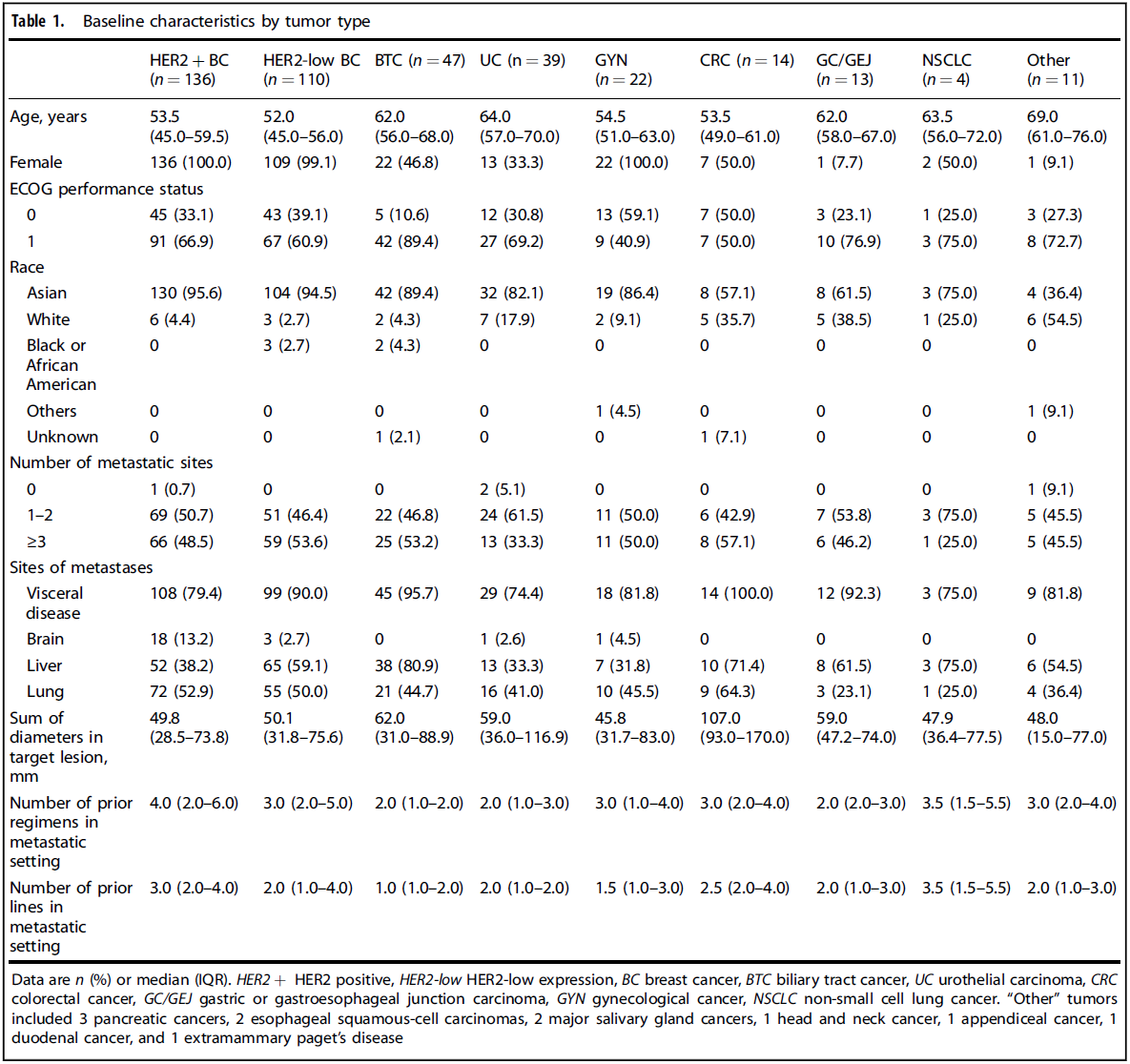

这项首次人体I期试验的最终分析再次证实了SHR-A1811作为HER2表达和HER2突变实体瘤患者的一种高效且安全的治疗选择的潜力。其良好的安全性特征,加上在多种实体瘤中令人鼓舞的疗效,使SHR-A1811成为现有HER2靶向疗法极具前景的替代方案。尽管本研究为单臂试验,缺乏直接对照,但其令人鼓舞的结果已为后续临床试验铺平了道路。目前,SHR-A1811在早期和晚期乳腺癌中的多项II/III期研究正在进行中。未来,如何优化其治疗策略、探索联合治疗模式以及通过生物标志物精准筛选获益人群,将是进一步的研究方向。
来源:肿瘤界