基于单中心医院肿瘤登记的2019年恶性肿瘤患者5年生存报告
周慧君, 魏丽娟, 王伟平, 王洪涛, 李海欣, 王丽娜, 黄鼎智, 郝继辉
(天津医科大学肿瘤医院)
引用本文:
周慧君, 魏丽娟, 王伟平, 王洪涛, 李海欣, 王丽娜, 黄鼎智, 郝继辉. 基于单中心医院肿瘤登记的2019年恶性肿瘤患者5年生存报告[J]. 中国肿瘤临床. DOI: 10.12354/j.issn.1000-8179.2026.20251746
版权声明:
本文为《中国肿瘤临床》原创文章,其他媒体、网站、公众号等如需转载本文,请在原文留言中获得授权,并在转载文章开头显示注明“原文刊发于《中国肿瘤临床》,卷(期):起止页码”。谢谢合作!
摘要
目的 分析以医院肿瘤登记为基础的全年恶性肿瘤患者的5年生存状况,以真实世界数据为肿瘤防治工作提供区域性参考。
方法 选取2019年1月至2019年12月于天津医科大学肿瘤医院初诊为恶性肿瘤并住院接受初治的28 111例患者进行回顾性随访。通过电话随访、病历资料查询及死因数据链接3种方式收集患者结局资料,随访截至2025年8月。使用Kaplan-Meier 法估计总生存率(overall survival rate,OS),并对不同癌种、性别和年龄组的生存率进行亚组分析,采用Log-rank检验比较生存曲线组间差异。
结果 收治患者数量前3位的恶性肿瘤依次为乳腺癌(7 246例)、甲状腺癌(5 527例)和肺癌(4 898例)。全部恶性肿瘤患者的1、3、5年OS分别为92.5%、83.6%和78.7%。不同癌种间生存率存在显著性差异,其中甲状腺癌、乳腺癌和子宫体癌的5年OS均超过90.0%,而胰腺癌仅为20.8%。分层分析显示,女性生存状况优于男性,且OS随年龄增长呈下降趋势。
结论 超过70%的患者经规范诊治可获得5年以上生存期,不同癌种、性别及年龄组间的生存状况有显著性差异。对于重点癌种、男性及高年龄组的恶性肿瘤患者要给予更多关注,进一步改善患者预后,持续降低恶性肿瘤疾病负担。
前言
恶性肿瘤是威胁中国居民健康的重大公共卫生问题[1]。患者生存率是评估肿瘤综合防治成效的重要指标,其准确获取依赖于人群和医院肿瘤登记体系。全球癌症生存监测计划(CONCORD-3)分析了71个国家322个登记处的3 750万例患者,为制订全球癌症防治政策提供了基于人群的真实世界数据[2]。在我国,国家癌症中心整合全国281个人群癌症登记处数据,报告2019年至2021年恶性肿瘤5年相对生存率为43.7%[3],各省市也曾发布区域性人群生存数据[4-5]。然而,基于医院登记的多癌种综合生存研究仍较有限,现有报道多集中于单一癌种[6-8]。
天津医科大学肿瘤医院作为首批国家恶性肿瘤临床医学研究中心,自建院之初便高度重视肿瘤随访工作,但既往研究多局限于单一病种或特定人群,缺乏对全院层面肿瘤患者生存状况的系统描述。2025年,医院正式成立随访中心,依托智慧化系统实现从部分癌种向全癌种、从特定人群向全院患者的覆盖。本研究回顾性分析了2019年于该院初诊并住院治疗的恶性肿瘤患者生存结局,报告1、3、5年总生存率(overall survival rate,OS),并按性别、年龄分层描述主要癌种生存状况,以期为肿瘤防治提供区域性参考。
01
流行病学
1.1 临床资料
选取2019年1月1日至2019年12月31日于天津医科大学肿瘤医院初诊为恶性肿瘤并住院治疗的患者,对应国际疾病分类编码第10版(ICD-10)中的C00-C76、C80-C97,通过人工审核排除住院后未接受抗肿瘤治疗或已在外院完成首次根治性治疗的患者,最终共纳入28 111例。
1.2 方法
1.2.1 资料收集方式
通过死因数据链接、电话随访和病历资料查询3种方式收集患者结局资料:1)通过与相关省市疾病预防控制中心的肿瘤登记系统和死因登记系统进行数据链接和匹配,获得患者死亡结局资料;2)对于未匹配到死亡记录的患者,由专职随访人员依次拨打其预留联系电话,向患者或家属了解生存状态与疾病进展,并记录末次随访时间;3)电话失访的患者则通过查询医院信息系统获取其末次就诊日期,并结合复诊记录判断生存状态。于2025年3月至8月对纳入随访对象完成回顾性随访。
1.2.2 数据质量评价
纳入28 111例恶性肿瘤患者进行生存分析,其中26 836例患者至少接受过1次随访,随访覆盖率为95.5%,整体中位随访时间为68.0个月。随访观察到死亡患者5 737例,占20.4%;随访5年仍生存患者17 021例,占60.6%;失访患者5 353例,占19.0%。
1.3 统计学方法
以全死因死亡作为生存分析的终点事件。对于未发生终点事件或终点事件状态未知的患者,以其末次随访日期或末次就诊日期作为截尾值,按删失数据处理。此外,接受手术治疗患者的起始时间为手术时间,新辅助治疗患者起始时间为首次开始新辅助治疗时间,其他治疗患者起始时间为入院时间。
使用SPSS 27.0和R 4.5.1软件进行统计学分析。采用Kaplan-Meier法估计1、3、5年观察生存率,即OS,并计算其点估计值和95%置信区间(confidence interval,CI),同时绘制各癌种生存曲线。采用Log-rank检验比较组间差异。中位随访时间通过反向Kaplan-Meier法估算。检验水准采用双侧α=0.05,以P<0.05为差异具有统计学意义。
02
结果
2.1 恶性肿瘤患者基线特征
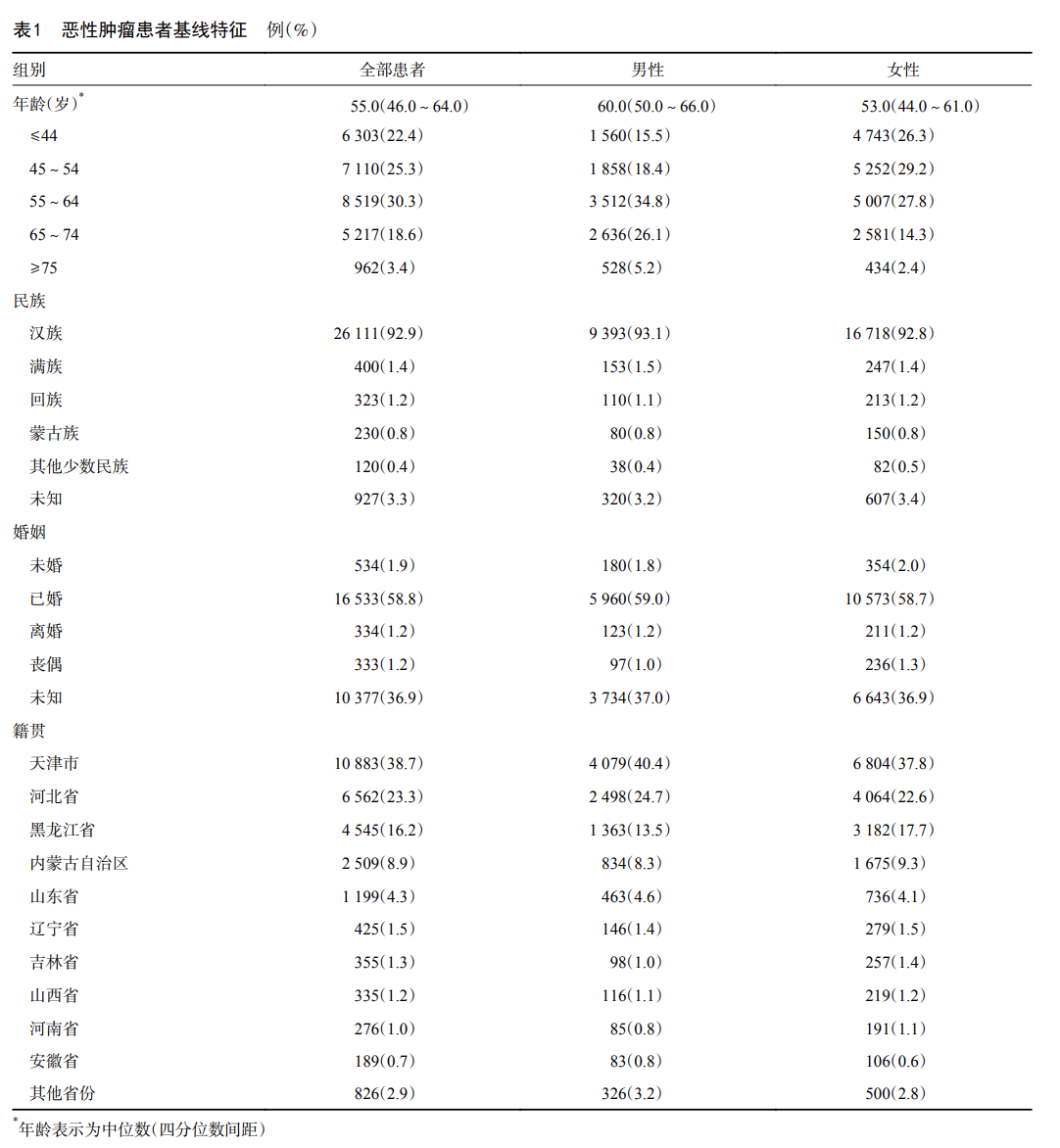
本研究共纳入28 111例患者,其中男性10 094例(35.9%),女性18 017例(64.1%)。全部患者中位确诊年龄55.0岁(四分位距:46.0~64.0岁),男性(60.0岁)高于女性(53.0岁)。年龄分布以55~64岁组为主,占总病例数的30.3%。
患者绝大多数是汉族(26 111例,92.9%)。患者户籍地覆盖全国31个省市自治区,前5位依次是:天津市10 883例(38.7%)、河北省6 562例(23.3%)、黑龙江省4 545例(16.2%)、内蒙古自治区2 509例(8.9%)和山东省1 199例(4.3%),见表1。
2.2 恶性肿瘤患者癌症部位分布
全部患者中,乳腺癌占比最高(7 246例,占25.8%),其次分别为甲状腺癌(5 527例,19.7%)、肺癌(4 898例,17.4%)、胃癌(1 583例,5.6%)和结直肠癌(1 431例,5.1%),见表2。
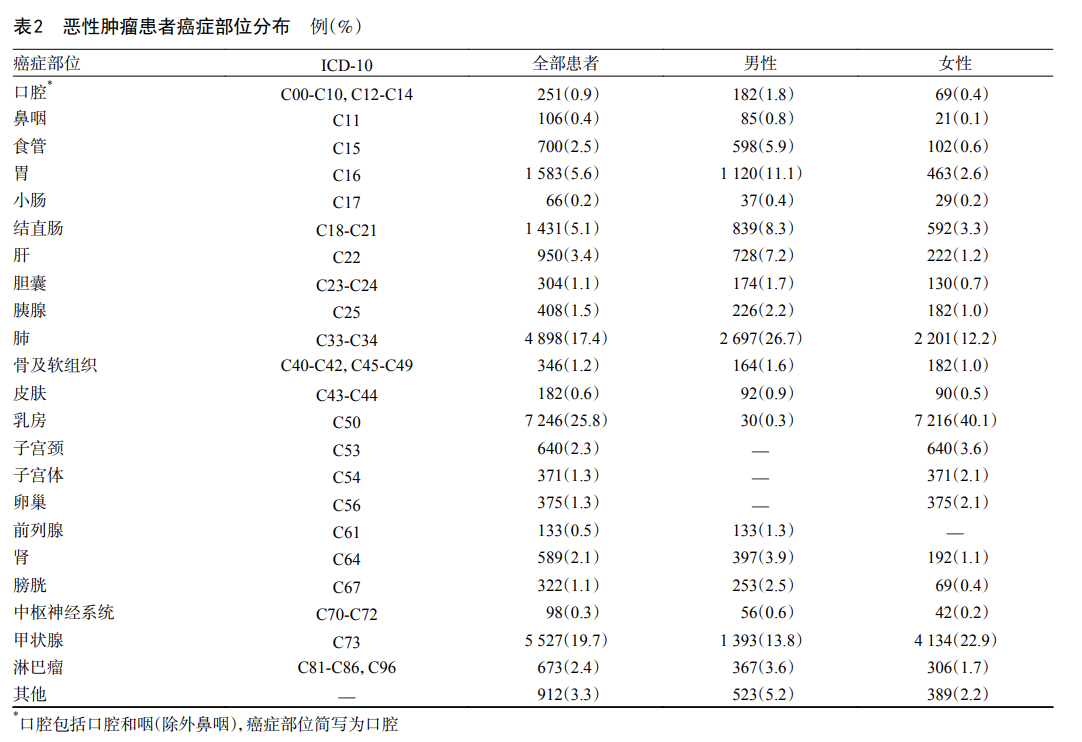
男性患者中,病例数排名前5位的依次是肺癌(2 697例,26.7%)、甲状腺癌(1 393例,13.8%)、胃癌(1 120例,11.1%)、结直肠癌(839例,8.3%)和肝癌(728例,7.2%),合计占男性病例的67.1%(表2)。
女性患者中,病例数排前5位的依次是乳腺癌(7 216例,40.1%)、甲状腺癌(4 134例,22.9%)、肺癌(2 201例,12.2%)、子宫颈癌(640例,3.6%)和结直肠癌(592例,3.3%),合计占女性病例的82.1%(表2)。
2.3 恶性肿瘤患者OS
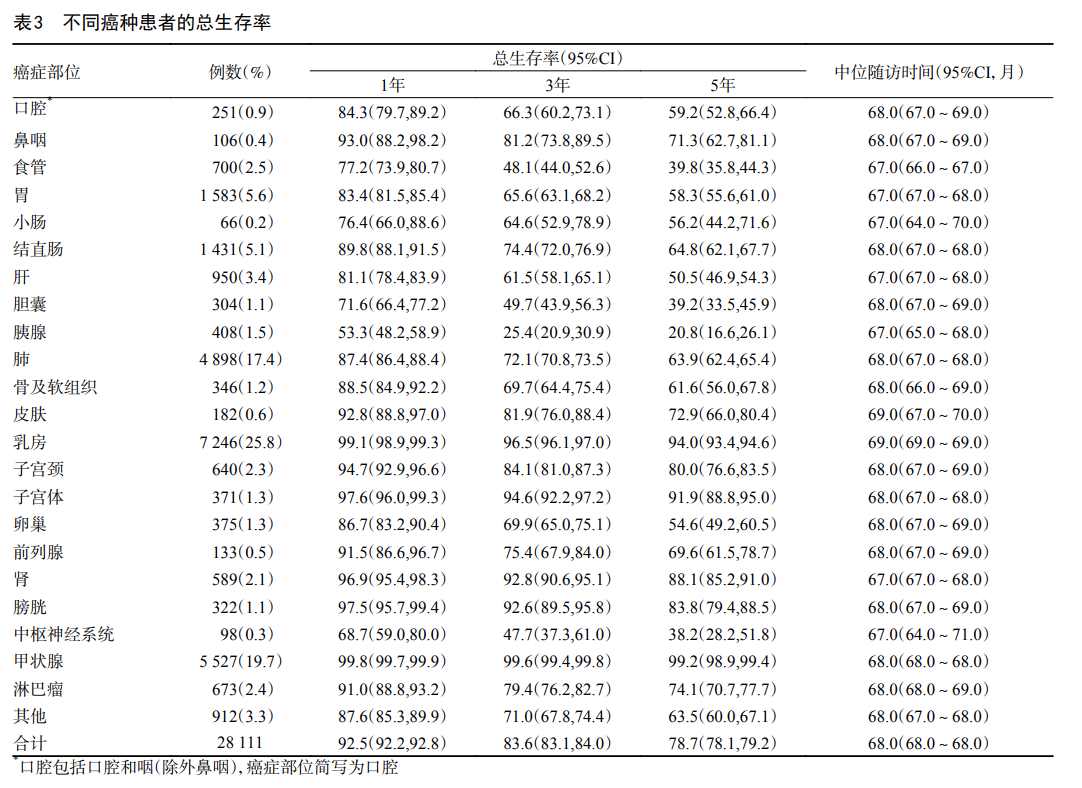
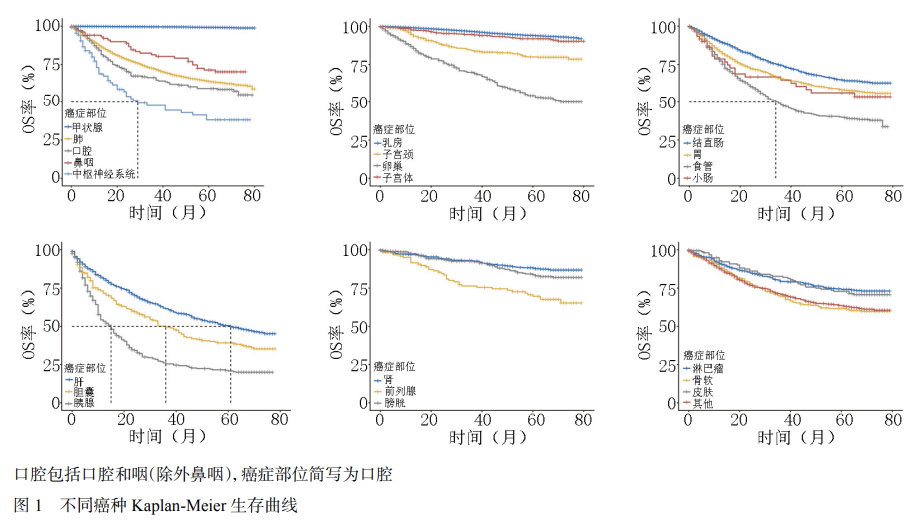
恶性肿瘤患者1、3、5年OS分别为92.5%、83.6%和78.7%。5年OS位于前10位的恶性肿瘤依次为:甲状腺癌(99.2%)、乳腺癌(94.0%)、子宫体癌(91.9%)、肾癌(88.1%)、膀胱癌(83.8%)、子宫颈癌(80.0%)、淋巴瘤(74.1%)、皮肤恶性肿瘤(72.9%)、鼻咽癌(71.3%)以及前列腺癌(69.6%)。相反,胰腺癌(20.8%)、中枢神经系统恶性肿瘤(38.2%)、胆囊癌(39.2%)和食管癌(39.8%)的5年OS则不足40.0%(表3,图2),各癌种生存曲线见图1。
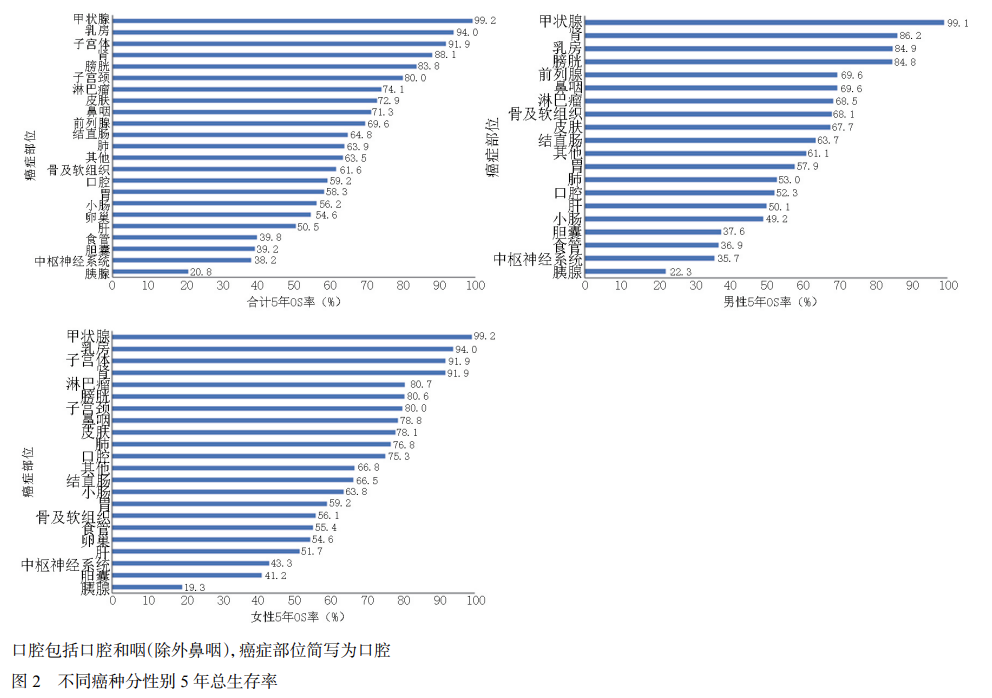
2.4 不同癌种分性别OS
女性患者总体生存状况优于男性,其中男性患者1、3、5年OS分别为86.2%、70.4%和63.2%,而女性患者分别为95.9%、90.6%和86.9%,显著高于男性(P<0.001)。在口腔癌和咽癌(除外鼻咽)、食管癌、肺癌、皮肤恶性肿瘤、乳腺癌及淋巴瘤中,男性、女性OS差异具有统计学意义(P<0.05)。其中肺癌的男性、女性生存率差异最显著,女性5年OS较男性高23.8个百分点。
不管在男性还是女性患者中,甲状腺癌的5年OS均为最高的,分别为99.1%和99.2%;胰腺癌均为最低的,分别是22.3%和19.3%。
除甲状腺癌外,男性恶性肿瘤患者中5年OS最高的是肾癌(86.2%),其次为乳腺癌(84.9%)和膀胱癌(84.8%)。生存率较低的恶性肿瘤除胰腺癌外,还包括中枢神经系统恶性肿瘤(35.7%)、食管癌(36.9%)和胆囊癌(37.6%),5年OS均未超过40.0%(图2)。
女性患者中除甲状腺癌外,5年OS以乳腺癌最高,可达94.0%,其后依次为子宫体癌(91.9%)和肾癌(91.9%)。除胰腺癌外,生存率较低的恶性肿瘤还包括胆囊癌(41.2%)、中枢神经系统恶性肿瘤(43.3%)和肝癌(51.7%),其5年OS均高于40.0%,优于男性患者(图2)。
2.5 不同癌种分年龄组OS
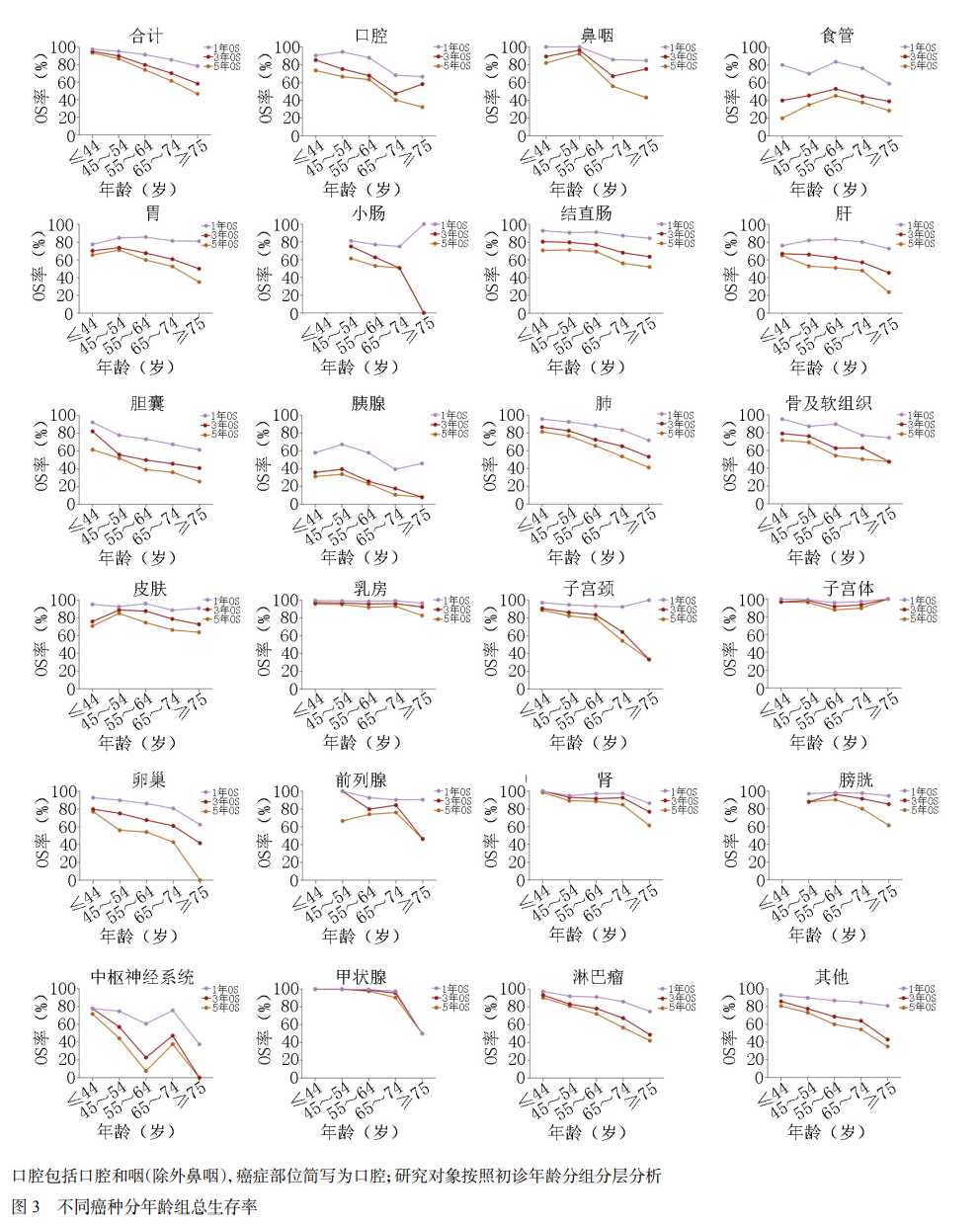
按初诊年龄组分层分析显示,除小肠癌、胆囊癌、皮肤恶性肿瘤、子宫体癌和前列腺癌以外,其余癌种的生存率在不同年龄组间均差异具有统计学意义(P<0.05)。恶性肿瘤患者5年OS随年龄增长呈下降趋势,75岁及以上年龄组最低(图3)。
03
结语
本研究基于2019年单中心真实诊疗数据,系统分析了恶性肿瘤患者的5年生存结局,其中乳腺癌、甲状腺癌和肺癌收治数量居前3位。目前国内基于医院登记的肿瘤生存报告多集中于南方及部分西部地区[9-12],而本研究首次呈现了北方地区泛癌种患者的长期生存结果,填补了区域生存分析的空缺,可为区域诊疗方案优化、高危人群筛查及公共卫生政策制定提供可靠依据。
随着肿瘤筛查及早诊早治指南的发布与推广,以及肿瘤诊断技术、治疗手段和全程管理模式的持续进步,中国恶性肿瘤生存率不断提高。国家癌症中心数据显示年龄标化5年相对生存率从2003年至2005年的30.9%提高至2019年至2021年的43.7%[3,13]。这一趋势在区域数据中也得到印证,如天津市恶性肿瘤患者5年相对生存率从2010年的41.9%提高至2016年的53.7%[4];江苏省盐城市由2012年至2014年的35.8%上升至2018年至2020年的52.0%[5]。同时也有少量研究报道了基于医院肿瘤登记患者的生存结局。复旦大学附属肿瘤医院2008年至2017年住院患者的5年OS为71.0%[11];广西医科大学附属肿瘤医院2011年至2020年住院患者的5年OS为51.4%[9];新疆医科大学附属肿瘤医院2010年至2021年住院患者的5年OS为60.3%[12];云南省肿瘤医院2014年至2023年住院初治患者的5年OS为49.0%[10]。本研究基于医院肿瘤登记数据分析显示,患者5年OS为78.7%,在全国处于较高水平。但需指出,医院与人群肿瘤登记数据在来源上存在本质差异,不宜直接进行横向比较。此外,生存率受多种因素影响,包括纳入患者的诊断时期、癌种构成、患者经济状况及受教育程度等。本中心收治患者中甲状腺癌和乳腺癌合计占比达45.5%,这两类肿瘤预后普遍较好,可能导致生存率偏高。
不同癌种患者的生存率呈现显著性差异。本研究中5年OS排名前5位的依次为:甲状腺癌(99.2%)、乳腺癌(94.0%)、子宫体癌(91.9%)、肾癌(88.1%)和膀胱癌(83.8%),其5年OS均超过80.0%,提示这些癌种预后相对较好,与多数既往研究趋势一致。复旦大学附属肿瘤医院2005年至2021年间住院治疗的甲状腺癌患者5年OS为98.5%[8],2003年至2017年乳腺癌患者5年OS为92.5%[14]。新疆医科大学附属肿瘤医院研究发现2015年至2019年新发女性乳腺癌患者的5年OS为85.0%[15]。此外,北京某三级甲等肿瘤专科医院统计的2009年至2018年间收治且获得完整随访资料的子宫体癌与肾癌患者的5年OS分别为83.2%和89.4%[6-7]。广西医科大学附属肿瘤医院2011年至2020年确诊并住院治疗的膀胱癌患者5年OS为64.6%,在17种恶性肿瘤中位列第7位[9]。相比之下,胰腺癌患者的预后仍非常严峻,其生存率在本研究所涵盖的23类恶性肿瘤中最低。未来应采取多维度策略,包括高危人群的识别与预防,早期筛查诊断技术及新型药物、治疗方法的研发与应用,以改善胰腺癌患者的生存结局。
本研究还发现不同性别恶性肿瘤患者的生存率存在显著性差异,女性患者OS高于男性,与基于人群或医院病例的报道结果均一致[3,10]。性别间生存差异可能源于生理特征与行为因素的综合影响,尤其男性较高的吸烟率可能是导致生存差异的重要原因[4],本研究中女性肺癌患者的5年OS高出男性23.8个百分点。此外,癌种构成也可能是导致本研究男女生存率差异的重要原因。本中心男性患者中肺癌(26.7%)、甲状腺癌(13.8%)和胃癌(11.1%)占比较高,而女性患者中乳腺癌(40.1%)和甲状腺癌(22.9%)合计占比达63.0%,可能在一定程度上拉高了女性的整体生存水平。
从不同年龄段生存分析结果来看,随着患者年龄增长,生存率总体呈下降趋势,其中年龄≥75岁组的生存状况最差。这可能与老年患者确诊时分期较晚、合并症较多、治疗依从性相对较低以及社会经济水平等多重因素有关[10,12]。
综上所述,本研究显示超过70%的患者经过规范诊疗可实现5年以上生存,但不同癌种、年龄组及性别之间的生存率存在显著性差异。需要指出的是,本研究为首次对5年前确诊病例开展的回顾性随访,仍存在一定比例的失访,且未能按肿瘤分期、组织学类型等关键临床变量进行更细致的分层分析。未来将进一步提高随访资料的完整性和准确性,使生存研究更加精细化,从而更加客观、准确地评估恶性肿瘤患者生存状况,为改善患者的生存结局提供更坚实的循证依据。
志谢:本文谨向就诊于天津医科大学肿瘤医院且积极配合随访工作的每一位患者致以诚挚谢意。此外,特别感谢张涛、陈万青、陈可欣教授以及天津医科大学肿瘤医院各位专家(王珂、王旭东、史业辉、任秀宝、李慧、李祥春、杨吉龙、张瑾、张会来、张真发、高春涛、袁智勇、强万敏、潘战宇、魏玺)提出的宝贵意见与指导。
来源:中国肿瘤临床