
通信作者:武爱文
引用本文:孙婷婷, 张洁, 姚云峰, 等. 重视结直肠癌从疾病诊治到患者健康的全程化管理[J]. 中华胃肠外科杂志, 2026, 29(3): 305-311. DOI: 10.3760/cma.j.cn441530-20251226-00478.
作者:孙婷婷 张洁 姚云峰 武爱文
作者单位:北京大学肿瘤医院暨北京市肿瘤防治研究所胃肠肿瘤中心三病区,恶性肿瘤发病机制及转化研究教育部重点实验室 北京大学肿瘤医院暨北京市肿瘤防治研究所胃肠肿瘤中心三病区,消化系肿瘤整合防治全国重点实验室
通信作者:武爱文,Email:wuaw@hsc.pku.edu.cn
摘要
随着结直肠癌治疗技术的不断进步,患者生存期显著延长,疾病逐渐呈现慢病化趋势。传统的“以疾病为中心”的诊疗模式已难以满足患者对功能保留、心理支持和社会回归的综合需求。本文系统梳理了结直肠癌全程化管理的必要性、可行性与现实挑战,提出以患者为中心,覆盖院前、院中和院后的连续性照护体系。通过整合多学科协作、个案管理、数字化平台与人工智能辅助决策,构建以“个案管理师—出院准备服务护理师—伤口造口专科护士”模式为代表的创新管理路径,实现从“治病”到“治人”的理念转变。未来,智能化、个性化、协同化的全程管理新模式将成为推动结直肠癌诊疗高质量发展的关键方向。
纵观结直肠肿瘤外科的发展,从18世纪尝试“减状手术”的探索,到19~20世纪追求“极致根治”的实践,21世纪已演进至关注“根治和功能”的平衡[1]。手术技术精进和诊疗手段创新让大多数结直肠癌患者有机会进入长期生存状态,也同时面临着漫长而复杂的康复过程。根据中共中央国务院2016年发布的《“健康中国2030”规划纲要》要求,我国2030年要实现全人群、全生命周期的慢性病健康管理[2]。2021—2022年,《国务院办公厅关于推动公立医院高质量发展的意见》和《“十四五”国民健康规划》也提出,坚持以人民健康为中心,推进公立医院医疗服务模式优化创新,推广多学科诊疗、日间手术和延续护理等高质量发展内容,强化患者需求导向,实现公立医院运行模式从粗放管理向精细化管理转变[3-4]。在此背景下,覆盖院前准备、院中服务、出院准备和院后随访的连续性照护全程即全程化管理模式逐渐在各中心结直肠癌诊疗单元中展开实践。本文旨在为外科医生和医院管理人员提供一个系统性的框架,探讨结直肠癌全程化管理模式的内涵、方法及其价值。
一
结直肠癌全程化管理的必要性
1.全程化管理是肿瘤慢病化趋势下管理范式转型的必然:据GLOBOCAN 2022数据显示,结直肠癌居全球发病第3位,死亡居第2位的恶性肿瘤,新发病例超过190万,死亡病例超过90万[5]。目前中国和美国结直肠癌患者5年总生存率可分别达56%[6]和64%[7];Ⅰ期、Ⅱ~Ⅲ期患者5年总生存率在93%和70%以上[8],疾病呈现慢病化趋势。直肠前切除术后患者常面临肠道功能紊乱[9-10]、泌尿功能[11]和性功能障碍[12]等问题,而造口患者则存在身体意象改变、污名化感受和生活满意度低等心理社会挑战[13-14]。这些障碍和挑战共同构成了对患者回归社会的系统性冲击。因此,结直肠癌诊疗模式有必要从“以疾病为中心”向“以患者为中心”完成转变。通过全程化管理,医疗机构可在不同阶段为患者提供精准且连贯的医疗照护,这是对患者的人文关怀,也是顺应生物-心理-社会医学模式的必然要求。
2.精细化和全程化患者管理是疾病诊疗的有机组成:加速康复外科(enhanced recovery after surgery,ERAS)路径的临床实践和传统辅助治疗后的运动康复干预在改善患者预后方面已显示积极意义,为全程化管理奠定了价值基础。早在2016年,瑞士一项回顾性队列研究即显示遵循ERAS方案与结直肠癌手术后5年生存率提升相关[15]。2019年发表的一项西班牙多中心、前瞻性队列研究结果也显示,与传统治疗模式相比,ERAS显著缩短了住院时间并降低了术后并发症发生率,且ERAS依从性越高,并发症发生率和死亡率越低[16]。2025年波兰的一项回顾性队列研究也发现,在Ⅰ~Ⅱ期(AJCC分期)结直肠癌患者中,ERAS依从率高于80%的患者,其5年总生存率显著优于依从率低于80%的患者[17]。CHALLENGE研究则提示,对于接受结直肠癌手术及辅助治疗的患者,为期3年的结构化运动干预相比仅发放健康教育材料可显著改善患者无病生存[18]。良好的全程化管理体系有望通过提高ERAS依从性和传统辅助治疗外“运动辅助治疗”的参与度,进一步降低并发症发生率、改善患者预后。
3.结直肠外科器官保留和功能保护对长期随访管理的新要求:结直肠肿瘤外科发展呈现手术范围缩小和器官功能保留的趋势,对患者管理的系统性和持续性提出全新要求。以直肠癌诊疗中的“等待观察”策略为例,对于新辅助治疗后达到临床完全缓解的直肠癌患者,该策略虽能实现器官功能保全,但其成功实施依赖于长期、严密的多项检查监测体系,需整合胸腹CT、直肠MRI、肠镜、直肠指诊和肿瘤标志物检测等结果,其复杂性远超过传统随访模式的承载能力[19]。功能保留手术也面临患者管理模式的挑战,以低位直肠癌的极限保肛手术经括约肌间切除术(intersphincteric resection,ISR)为例,术后患者更容易出现大便失禁、肛门静息压下降或控便能力下降等困扰[20-23]。这些问题多于患者回归家庭后逐渐显现,而非在住院期间集中暴露。若无系统化的术前评估和术后康复指导,保留的器官往往难以实现其应有的功能价值[24]。全程化管理为结直肠癌诊疗的技术创新匹配了管理创新,从个体化决策、动态评估到功能重建,为安全、有效、优质的器官保留提供了全周期保障。
4.医疗支付方式改革和老龄化趋势对医疗安全的要求提高:在疾病诊断相关分组(diagnosis related groups,DRG)/按病种分值付费(diagnosis intervention packet,DIP)支付方式改革的推动下,中国三级医院的平均住院日已从2018年的9.6 d[25]降至2024年的7.8 d[26]。2024年,本中心结肠癌、直肠癌患者平均住院日分别降至7.7 d和8.3 d。在我国人口老龄化加剧、医疗负担逐年加重的背景下,结直肠癌住院日的压缩虽可提升医疗资源利用效率并有助于控制费用,却也将部分术后康复和风险监测工作转移至院外,增加了患者院外治疗负担。若被动等待患者复诊,可能导致院外并发症发现与干预延迟,反而增加再入院风险和长期医疗成本。上述情况要求医疗服务模式必须从住院片段式诊疗转向院后随访干预的连续照护,以覆盖患者快速出院后的管理真空。
结直肠癌全程化管理的可行性
1.结直肠癌治疗目标的迭代提升:结直肠癌围手术期安全受手术和非手术并发症影响。中国胃肠肿瘤外科联盟发起的胃肠外科手术后腹部并发症现状研究数据库结果显示,结直肠癌患者术后并发症发生率14.8%,严重并发症发生率仅为3.0%。手术相关的并发症包括出血、漏和感染,尤其是手术时长、出血量、住院时间都显著降低[27]。手术安全性的提升让外科医生有了更多的认知资源分配到患者的功能预后、心理健康、生活质量和社会回归等高层次治疗目标。当生存不再是唯一的焦点,外科医生的角色就从“生命的拯救者”扩展为“健康的重建者”,这为全程化管理提供了理念基础和医护协作空间。
2.患者主动参与意识的兴起:在患者层面,信息化时代的知识平权促进了患者及家属群体主体意识的觉醒,使其从被动接受治疗的“客体”转变为主动参与决策的“合作者”。当患者理解治疗意义、掌握自我监测技能并能获得及时支持时,他们更有可能执行治疗计划、主动报告不良事件和积极参与康复训练。研究显示,超过40%的癌症患者在诊疗中参与了医患共同决策[28]。提升医务人员沟通技巧、了解患者对疾病与治疗信息的需求、理解患者价值观并引导家庭成员参与,这些路径有利于胃肠肿瘤患者医患共同决策的落地实施[29]。新型医患关系的形成及其实现路径的探索,为全程化管理奠定了重要的社会心理基础。
3.健康领域数智化技术的爆发式发展:移动通信技术的进步为远程医疗和长期随访提供了技术保障,这一突破地域限制和单模态数据瓶颈的高效率信息传送方式,促成了上下级医疗机构之间和医患之间多模态信息的实时共享和讨论,不仅有利于优质医疗资源下沉,还有利于节约就诊成本[30-31];人工智能技术则可以从影像、病理、基因组学等多模态数据中提取深层特征,用于辅助结直肠癌术前、术中和术后各阶段疗效预测、决策生成和并发症风险管理[32-35]。集成多模态数据的临床信息管理系统,成为结直肠癌全程化管理的核心赋能平台,为多学科团队(multidisciplinary team,MDT)的质量控制与持续优化提供了数据基石与流程支撑[36]。与医院信息系统互联的个案管理系统则是全程化管理的关键工具,不仅可作为“智能工作台”集成患者全周期数据,辅助个案管理师进行高效、精准的患者管理,还可通过实时分析任务完成率及患者结局等指标,成为医院管理者质控全程化管理工作的“动态仪表盘”[37]。
结直肠癌全程化管理的挑战
医护团队工作负担过重,是制约全程化管理有效实施的首要障碍。据中国医师协会2017年发布的《中国医师执业状况白皮书》结果显示,我国二、三级医院的医师平均每周工作时间分别为51.05 h和51.13 h,26~35岁组平均每周工作52.43 h,在所有年龄组中工作时间最长[38]。中国医学科学院杜听昱对143所三甲公立医院的30 125例临床医师调查结果显示,医生的情绪耗竭发生率达14.41%[39]。结直肠肿瘤外科医生面临着手术量增长、科研压力大和教学任务重等多重负担,要求医生投入额外时间进行系统性的患者全程管理往往难以实现。从护理人力资源视角审视,全程化管理的推行意味着护士需在繁重的临床任务之外,承担起健康教育、个案管理及随访协调等连续性照护职责,这一转变对护理团队的角色定位、人力配置与工时分配构成了系统性挑战。在我国护理人力资源总体短缺且分布不均的背景下,上述矛盾难以避免[40]。具体到结直肠肿瘤专科,护士是实施术前定位、造口护理、并发症管理与患者随访的核心力量[41]。如何有效赋能该群体,并通过清晰的医护协作机制明确权责,是破解护理团队从被动执行医嘱的操作者到主导连续性照护的专科协作者这一管理掣肘的关键。
再者,结直肠癌患者在诊断时普遍伴有至少一种重要共病,如高血压、糖尿病、慢性阻塞性肺病、消化性溃疡、心血管疾病、脑血管疾病或肾病等[42-43]。尤其是伴有心血管疾病的结直肠癌患者,其治疗决策和管理异常复杂。40~74岁的结直肠癌患者中约1/4同时罹患心血管疾病[44];65岁以上老年结直肠癌患者中该比例甚至可高达1/3[45]。在人口老龄化加剧的今天,面对这类伴有共病的结直肠癌患者,如何权衡治疗利弊、协调干预优先是极具挑战的临床难题。其全程化管理涵盖多项评估和干预内容,不仅需要外科、心内科、内分泌科、肾内科、麻醉科等专科打破学科界限进行协同诊疗,也离不开临床药师、营养师和心理治疗师的技术支持[46]。但在现实医疗环境中,受限于专科协作机制及付费体系,以患者为中心的整合医疗模式落地执行仍存在一定阻力。
此外,结直肠癌患者随访周期长达5年、10年甚至终身,随访工作量大,指南中关于随访内容和强度的建议也存在差异[47]。有研究显示,依据患者量身定制的随访模式有助于提高患者随访满意度[48];但如何确定最优的随访策略,怎样在医疗价值和资源约束之间找到平衡,还需基于真实世界数据的持续研究。新型随访模式如微信平台远程随访、基于区域医联体的智慧护理服务等需要结合具体情境进行选择和优化[49-51]。在依赖互联网技术开展的随访和照护工作中,如何保护数据隐私和维持线上医患关系的人文温度,都是需要深入思考的问题。
结直肠癌全程化管理的实践路径
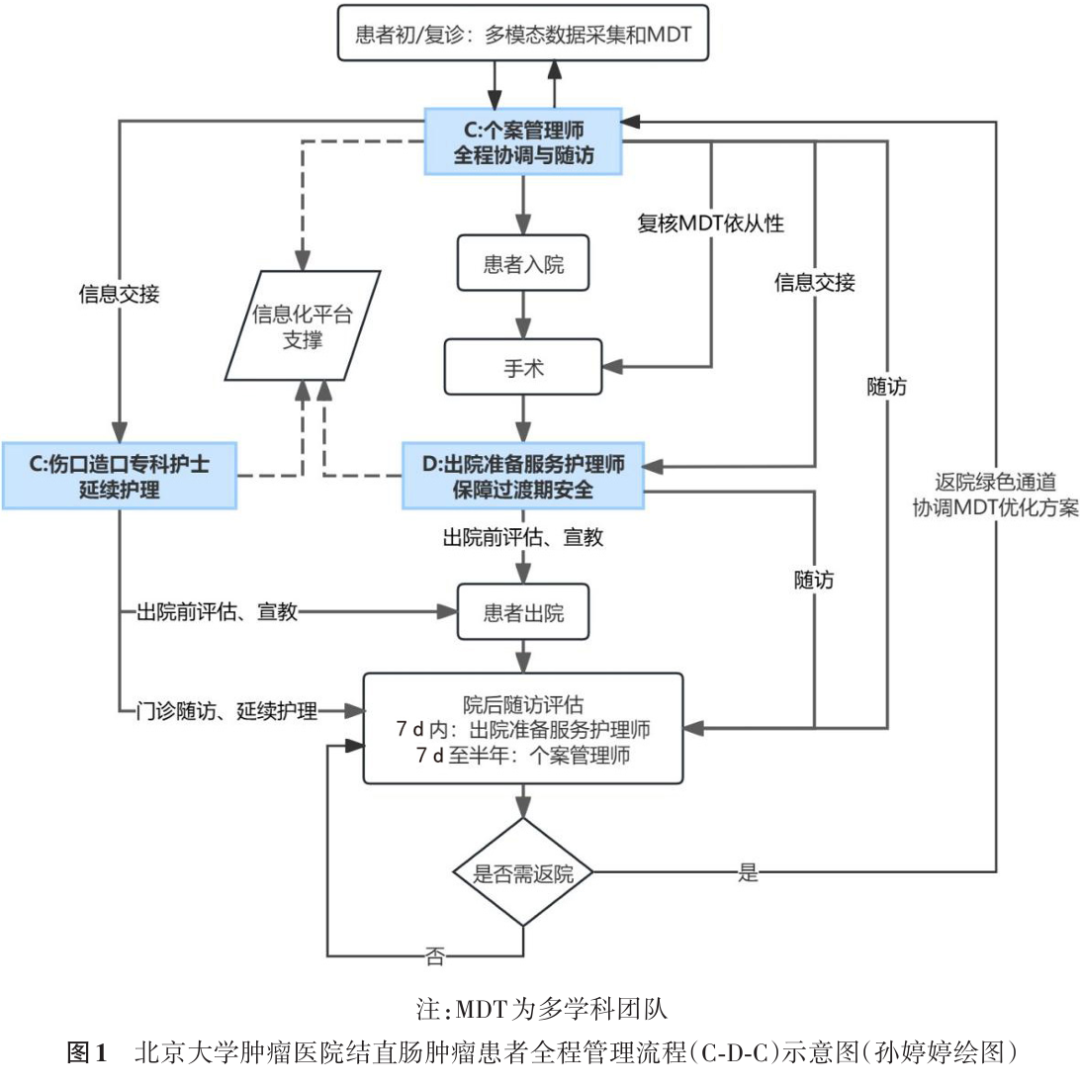
在实践结直肠癌全程化管理的工作中,我们深刻体会到医护协同和充分发挥医护两方优势是至关重要的。自2021年起,在传统MDT基础上,北京大学肿瘤医院胃肠肿瘤中心三病区整合医疗、护理、造口治疗师等,创建“C-D-C模式”为直肠癌患者提供全程化管理服务,该模式的核心在于构建一个以个案管理师(case manager,C)、出院准备服务护理师(discharge planning nurse,D)和伤口造口专科护士(wound/ostomy specialist nurse-based continuing care,C)为主导的多学科整合照护团队(图1),以更好地配合和协助完成全程化管理的目标。个案管理师作为核心协调者,负责整合资源、优化就诊流程以确保MDT良好运行,全程跟踪管理诊疗信息和协调各阶段治疗,并进行出院后7 d至半年的长期随访,向主诊医师反馈病情并为需返院患者开通绿色通道;出院准备服务护理师专注于解决因ERAS实施导致的住院时间短、出院准备不足的问题,在患者出院前进行充分评估和宣教以提升患者出院准备度,在出院后7 d内进行随访以保障过渡期安全;伤口造口专科护士提供专业的伤口和造口护理指导、并发症处理及产品推荐,在门诊随访和出院前评估中发挥着关键作用,也满足了患者术后伤口护理和造口管理的特殊需求。为支撑这一模式,医院整合开发了造口信息管理系统和个案管理信息系统,并通过线上宣教、官方微信咨询和线上护理门诊的路径为患者提供优质、可及的全程化管理服务。该模式显著优化了就诊流程,全面提升了康复质量、安全性和患者满意度[52]。
未来展望
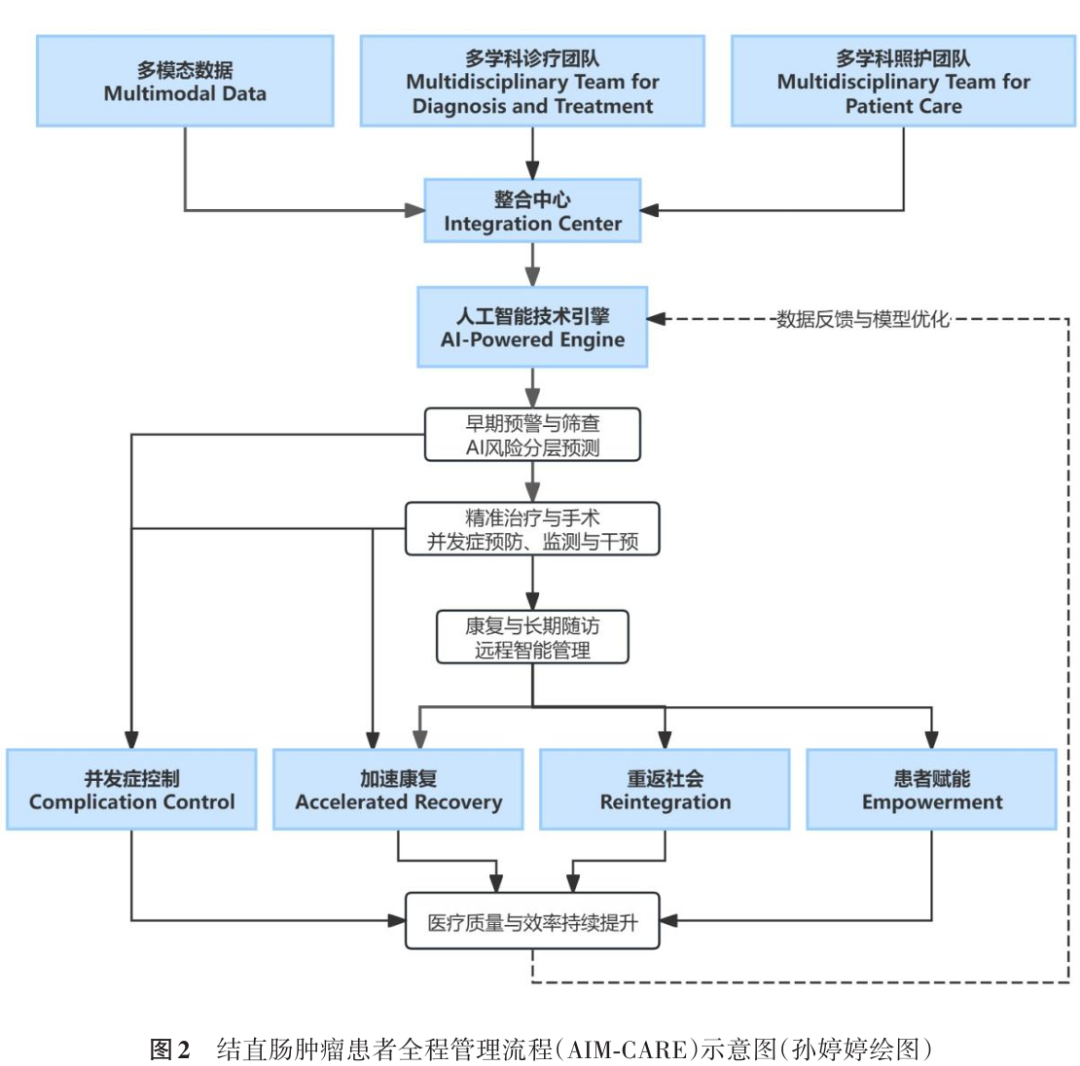
在人工智能技术快速发展的今天,基于人工智能构建的结直肠癌风险预测模型已被验证可用于临床实践并实现了风险分组、辅助医生决策和指导个性化干预,降低了术后并发症率和节约人均近3 000美元的成本[53]。结合全程化管理的重要价值和诸多挑战,笔者认为,有必要构建面向未来的智能化结直肠癌全程化管理新范式(artificial intelligence、integration、multimodal data & multidisciplinary team、complication control、accelerated recovery、reintegration、empowerment,AIM-CARE)(图2)。新模式的核心在于,利用人工智能技术作为引擎,整合多学科团队和多源异构数据,以实现对并发症的精准防控和改进术后患者随访管理,最终达成加速康复、助力患者重返社会并赋予其长期自我管理能力的目标。新模式将实现将人的智慧与机器的智能相结合,将标准化流程与个性化照护相统一。未来的结直肠癌全程化管理不再仅仅是一个标准化的临床管理路径,而是一个持续学习和优化的智能生态系统,让患者掌握健康主动权,让医护团队从繁琐事务性工作中解放出来以专注于核心决策和人文关怀,让医疗机构实现医疗质量和运营效率的持续提升。
总结
结直肠癌诊疗从“以病为纲”的技术导向迈向“以人为本”的价值导向,这是外科技术成熟后的必然升华,而全程化管理是承载了这一转型的具体实践。北京大学肿瘤医院的“C-D-C”模式提供了良好范例,实施中虽面临人力、系统整合的挑战,但也迎来了医工技术赋能、患方意识觉醒、国家政策支持等契机。人工智能的快速发展为未来的全程化管理新模式描绘了可行的方向。对结直肠肿瘤外科医生而言,拥抱上述转型既是责任也是机遇,需在精进手术、关注病灶和治愈疾病的同时拓展管理思维、关怀整体的人和帮助患者重建有意义的生活,这是对医疗本质的新时代洞见,也是对“健康中国”的积极响应。
利益冲突 所有作者均声明不存在利益冲突
滑动阅读参考文献
[1]石一航,王锡山. 结直肠外科的发展历程解析[J/OL]. 中华结直肠疾病电子杂志, 2025,14(1):29-39. DOI:10.3877/cma.j.issn.2095-3224.2025.01.003.
[2]印发«"健康中国2030"规划纲要»[N].人民日报, 2016-10- 26(001).
[3]国务院办公厅关于推动公立医院高质量发展的意见[J].中华人民共和国国务院公报,2021,(17):174-178.
[4]国务院办公厅关于印发"十四五"国民健康规划的通知[J].中华人民共和国国务院公报,2022,(16):17-31.
[5]Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2024,74(3):229-263. DOI: 10.3322/caac.21834.
[6]Zeng H, Zheng R, Sun K, et al. Cancer survival statistics in China 2019-2021: a multicenter, population-based study[J]. J Natl Cancer Cent, 2024,4(3):203-213. DOI: 10.1016/j.jncc.2024.06.005.
[7]Siegel RL, Kratzer TB, Giaquinto AN, et al. Cancer statistics, 2025[J]. CA Cancer J Clin, 2025,75(1):10-45. DOI: 10.3322/caac.21871.
[8]Miller KD, Nogueira L, Devasia T, et al. Cancer treatment and survivorship statistics, 2022[J]. CA Cancer J Clin, 2022,72(5):409-436. DOI: 10.3322/caac.21731.
[9]Bryant CL, Lunniss PJ, Knowles CH, et al. Anterior resection syndrome[J]. Lancet Oncol, 2012,13(9):e403- e408. DOI: 10.1016/S1470-2045(12)70236-X.
[10]Keane C, Fearnhead NS, Bordeianou L, et al. International consensus definition of low anterior resection syndrome[J]. Colorectal Dis, 2020,22(3):331-341. DOI: 10.1111/codi.14957.
[11]Kwaan MR, Fan Y, Jarosek S, et al. Long-term risk of urinary adverse events in curatively treated patients with rectal cancer: a population-based analysis[J]. Dis Colon Rectum, 2017,60(7):682-690. DOI: 10.1097/DCR.000000 0000000788.
[12]Hendren SK, O'Connor BI, Liu M, et al. Prevalence of male and female sexual dysfunction is high following surgery for rectal cancer[J]. Ann Surg, 2005,242(2):212-223. DOI: 10.1097/01.sla.0000171299.43954.ce.
[13]Neuman HB, Patil S, Fuzesi S, et al. Impact of a temporary stoma on the quality of life of rectal cancer patients undergoing treatment[J]. Ann Surg Oncol, 2011,18(5):1397-1403. DOI: 10.1245/s10434-010-1446-9.
[14]Smith DM, Loewenstein G, Rozin P, et al. Sensitivity to disgust, stigma, and adjustment to life with a colostomy[J]. J Res Pers, 2007,41(4):787-803. DOI: 10.1016/j.jrp.2006.09.006.
[15]Gustafsson UO, Oppelstrup H, Thorell A, et al. Adherence to the ERAS protocol is associated with 5-year survival after colorectal cancer surgery: a retrospective cohort study[J]. World J Surg, 2016,40(7):1741-1747. DOI: 10.1007/s00268-016-3460-y.
[16]Ripollés-Melchor J, Ramírez-Rodríguez JM, Casans- Francés R, et al. Association between use of enhanced recovery after surgery protocol and postoperative complications in colorectal surgery: the postoperative outcomes within enhanced recovery after surgery protocol (POWER) study[J]. JAMA Surg, 2019,154(8):725-736. DOI: 10.1001/jamasurg.2019.0995.
[17]Pisarska-Adamczyk M, Zawadzka K, Torbicz G, et al. Does high compliance with the enhanced recovery after surgery protocol improve 5-year survival? A cohort study of 468 nonmetastatic colorectal cancer patients[J]. Pol Arch Intern Med, 2025,135(5):16960. DOI: 10.20452/pamw.16960.
[18]Courneya KS, Vardy JL, O'Callaghan CJ, et al. Structured exercise after adjuvant chemotherapy for colon cancer[J]. N Engl J Med, 2025,393(1):13-25. DOI: 10.1056/NEJ Moa2502760.
[19]中国直肠癌新辅助治疗后等待观察数据库研究协作组,中华医学会外科学分会结直肠外科学组,中国医师协会结直肠肿瘤医师专业委员会,等. 直肠癌新辅助治疗后等待观察策略中国专家共识(2024版)[J]. 中华胃肠外科杂志,2024,27(4):301-315. DOI:10.3760/cma.j.cn441530-20240227- 00075.
[20]Köhler A, Athanasiadis S, Ommer A, et al. Long-term results of low anterior resection with intersphincteric anastomosis in carcinoma of the lower one-third of the rectum: analysis of 31 patients[J]. Dis Colon Rectum, 2000,43(6):843-850. DOI: 10.1007/BF02238025.
[21]Saito N, Ono M, Sugito M, et al. Early results of intersphincteric resection for patients with very low rectal cancer: an active approach to avoid a permanent colostomy[J]. Dis Colon Rectum, 2004,47(4):459-466. DOI: 10.1007/s10350-003-0088-4.
[22]Bretagnol F, Rullier E, Laurent C, et al. Comparison of functional results and quality of life between intersphincteric resection and conventional coloanal anastomosis for low rectal cancer[J]. Dis Colon Rectum, 2004,47(6):832-838. DOI: 10.1007/s10350-004-0523-1.
[23]Takahashi M, Sakamoto K, Tsukada Y, et al. A multicentre prospective study of anal function after laparoscopic ultra-low rectal cancer surgery using a mixed-effects model[J]. Colorectal Dis, 2025,27(5):e70129. DOI: 10. 1111/codi.70129.
[24]中国医师协会肛肠医师分会. 低位前切除综合征诊治中国专家共识(2025版)[J]. 中国普通外科杂志, 2025, 34(8):1603-1617.DOI:10.7659/j.issn.1005-6947.250357.
[25]中华人民共和国国家卫生健康委员会. 2018年我国卫生健康事业发展统计公报 [R/OL]. (2019-05-22) [2025- 12-14]. https://www.nhc.gov.cn/guihuaxxs/c100136/201905/893b4fd8d515420b802b6557fd3c2033.shtml.
[26]中华人民共和国国家卫生健康委员会. 2024年我国卫生健康事业发展统计公报 [R/OL]. (2025-12-02) [2025- 12-14]. https://www.nhc.gov.cn/guihuaxxs/c100133/202512/f1c3a3c617484a27a1a26a468afbaeee.shtml.
[27]张书勤,吴舟桥,霍博文,等. 一项基于全国多中心前瞻性登记队列研究(PACAGE)的中国胃癌和结直肠癌患者术后并发症现状分析[J]. 中华胃肠外科杂志,2024,27(3):247-260. DOI:10.3760/cma.j.cn441530-20240218-00067.
[28]胡婵,左丙丽,王沙沙,等.癌症患者参与医患共同决策影响因素的Meta分析[J].中华肿瘤防治杂志,2022,29(3):217-222. DOI: 10.16073/j.cnki.cjcpt.2022.03.11.
[29]Li M, Fu G, Mo W, et al. Analysis of influencing factors and strategies of implementing shared decision-making among patients with gastrointestinal cancer: a systematic review and meta-analysis of qualitative studies[J]. Ann Surg Oncol, 2025,32(7):5183-5199. DOI:10.1245/s10434- 025-17317-6.
[30]马惠娟,王安春,王燕,等. 远程医疗会诊系统在医疗匮乏地区的应用探索[J]. 中国数字医学,2018,13(1):88-90. DOI:10.3969/j.issn.1673-7571.2018.01.029.
[31]Gentili A, Failla G, Melnyk A, et al. The cost-effectiveness of digital health interventions: a systematic review of the literature[J]. Front Public Health, 2022,10:787135. DOI: 10.3389/fpubh.2022.787135.
[32]Feng L, Liu Z, Li C, et al. Development and validation of a radiopathomics model to predict pathological complete response to neoadjuvant chemoradiotherapy in locally advanced rectal cancer: a multicentre observational study[J]. Lancet Digit Health, 2022,4(1):e8-e17. DOI: 10.1016/S2589-7500(21)00215-6.
[33]Cahill RA, O'Shea DF, Khan MF, et al. Artificial intelligence indocyanine green (ICG) perfusion for colorectal cancer intra-operative tissue classification[J]. Br J Surg, 2021,108(1):5-9. DOI: 10.1093/bjs/znaa004.
[34]Park SH, Park HM, Baek KR, et al. Artificial intelligence based real-time microcirculation analysis system for laparoscopic colorectal surgery[J]. World J Gastroenterol, 2020,26(44):6945-6962. DOI: 10.3748/wjg.v26.i44.6945.
[35]Kiehl L, Kuntz S, Höhn J, et al. Deep learning can predict lymph node status directly from histology in colorectal cancer[J]. Eur J Cancer, 2021,157:464-473. DOI: 10.1016/j.ejca.2021.08.039.
[36]孙婷婷, 王林, 姚云峰, 等. 多学科协作的I-PDCA模式在结直肠癌学科建设中的实践与思考[J].医院管理论坛, 2024,41(1):3-7. DOI: 10.3969/j.issn.1671-9069.2024.01.001.
[37]张红, 张悦, 王立军, 等. 肿瘤专科医院个案管理信息系统的构建与实施 [J] . 中国实用护理杂志, 2020,36(3):205- 209. DOI: 10.3760/cma.j.issn.1672-7088.2020.03.009.
[38]中国医师协会. 中国医师执业状况白皮书 [R/OL]. (2017-12) [2025-12-26]. https://www.cmda.net/u/cms/www/201807/06181247ffex.pdf.
[39]杜昕昱. 我国三级公立医院医生情绪耗竭现状及其影响因素研究[D]. 北京:中国医学科学院,2024.
[40]苏彬彬,杜鹃,贾金忠,等. 中国护理人力资源现状及其配置研究[J]. 中国卫生政策研究,2018,11(12):56-61. DOI:10.3969/i.issn.1674-2982.2018.12.010.
[41]张洁,王丹丹,陈楠,等. 伤口造口失禁专科护士对造口患者管理的现况调查[J]. 中国护理管理,2023,23(11):1647- 1651. DOI: 10.3969/j.issn.1672-1756.2023.11.010.
[42]Gheybi K, Buckley E, Vitry A, et al. Occurrence of comorbidity with colorectal cancer and variations by age and stage at diagnosis[J]. Cancer Epidemiol, 2022,80:102246. DOI: 10.1016/j.canep.2022.102246.
[43]Qiu H, Wang L, Zhou L, et al. Comorbidity patterns in patients newly diagnosed with colorectal cancer: network-based study[J]. JMIR Public Health Surveill, 2023,9:e41999. DOI: 10.2196/41999.
[44]Al-Kindi SG, Oliveira GH. Prevalence of preexisting cardiovascular disease in patients with different types of cancer: the unmet need for onco-cardiology[J]. Mayo Clin Proc, 2016,91(1):81-83. DOI: 10.1016/j.mayocp.2015. 09.009.
[45]贾王平,寇福银,徐洪丽,等. 老年结直肠癌患者心血管代谢性疾病的患病情况及影响因素[J].中华肿瘤杂志, 2022,44(2):173-177. DOI:10.3760/cma.j.cn112152-20200227- 00140.
[46]中国医师协会结直肠肿瘤专业委员会. 中国老年结直肠肿瘤患者围手术期管理专家共识(2020版)[J/OL]. 中华结直肠疾病电子杂志,2020,9(4):325-334. DOI:10.3877/cma.j.issn.2095-3224.2020.04.001.
[47]Bastiaenen VP, Hovdenak Jakobsen I, Labianca R, et al. Consensus and controversies regarding follow-up after treatment with curative intent of nonmetastatic colorectal cancer: a synopsis of guidelines used in countries represented in the European Society of Coloproctology[J]. Colorectal Dis, 2019,21(4):392-416. DOI: 10.1111/codi.14503.
[48]Srikumar G, McLaughlin S, McGuinness MJ, et al. Follow-up strategies in colorectal cancer: What do patients prefer?[J]. ANZ J Surg, 2025,95(9):1820-1827. DOI: 10.1111/ans.70269.
[49]宋琴芬,刘春娥,尹光啸. 结直肠癌造口患者微信平台自我管理项目的构建及应用研究[J]. 中国实用护理杂志,2017,33(2):120-125. DOI:10.3760/cma.j.issn.1672-7088. 2017.02.011.
[50]卢先枝, 程方园, 王红丽. 基于微信平台的护理干预对结肠造口患者自护能力及并发症的影响[J].护理学报, 2018,25 (14):58-61. DOI:10.16460/j.issn1008-9969.2018.14.058.
[51]兰文霞,白伟利,闫慧楠. 区域医联体内结直肠癌患者延续性智慧护理服务模式的效果评估[J]. 中国医药导报, 2025,22(4):183-188. DOI:10.20047/j.issn1673-7210. 2025.04.33.
[52]张洁,王丹丹,张悦,等. C-D-C模式在直肠癌患者病程管理中的探索与实践[J]. 医院管理论坛,2025,42(1):68-72. DOI: 10.3969/j.issn.1671-9069.2025.01.017.
[53]Rosen AW, Ose I, Gögenur M, et al. Clinical implementation of an AI-based prediction model for decision support for patients undergoing colorectal cancer surgery[J]. Nat Med, 2025,31(11):3737-3748. DOI: 10.1038/s41591-025-03942-x.
来源:中华胃肠外科杂志