2026年4月10日,由复旦大学附属肿瘤医院吴小华教授、复旦大学附属妇产科医院鹿欣教授领衔中国团队,携手全球学者完成的的ENGOT-ov65/KEYNOTE-B96研究结果正式发表于The Lancet,题为“Pembrolizumab plus weekly paclitaxel in platinum-resistant recurrent ovarian cancer (ENGOT-ov65/KEYNOTE-B96): a multicentre, randomised, double-blind, phase 3 study”。该研究纳入了来自全球25个国家、187个中心的643例铂耐药复发性卵巢癌患者。研究结果显示,帕博利珠单抗联合节拍紫杉醇±贝伐珠单抗可显著改善患者的无进展生存期和总生存期,成为首个在卵巢癌中证实免疫检查点抑制剂联合方案带来总生存获益的随机对照III期研究,具有里程碑式意义。
研究背景
上皮性卵巢癌是全球第三大常见且致死率最高的妇科恶性肿瘤。大多数晚期卵巢癌患者在接受初始治疗后会经历疾病复发,并最终发展为铂耐药复发性卵巢癌。尽管目前有非铂类化疗(常联合贝伐珠单抗)等标准治疗,以及近年来取得突破的抗体偶联药物(ADC)等新型疗法,但此类患者的预后依然较差,临床上迫切需要新的治疗策略来改善患者的长期生存。 近年来,免疫检查点抑制剂在多种实体瘤中取得了巨大成功,但在卵巢癌中的探索却屡屡受挫。在KEYNOTE-028和KEYNOTE-100研究中,帕博利珠单抗(pembrolizumab)单药治疗复发性卵巢癌的客观缓解率(ORR)仅为8%-12%。此前两项III期随机研究(AGO-OVAR 2.29/ENGOT-ov34评估阿替利珠单抗[atezolizumab],JAVELIN Ovarian 200评估avelumab)在铂耐药卵巢癌中均未能证实ICI联合化疗在无进展生存或总生存方面的显著获益。 然而,临床前和早期临床数据表明,化疗(如紫杉醇[paclitaxel])特别是采用低剂量每周一次的“节拍式”给药时,可以通过增加肿瘤免疫原性、减少肿瘤微环境中的免疫抑制细胞来增强抗肿瘤免疫反应。基于这一理论基础,研究者开展了这项III期临床研究,旨在评估帕博利珠单抗联合节拍紫杉醇±贝伐珠单抗,对比单纯节拍紫杉醇±贝伐珠单抗,治疗既往1-2线系统治疗的铂耐药复发性卵巢癌患者的疗效与安全性。
研究设计
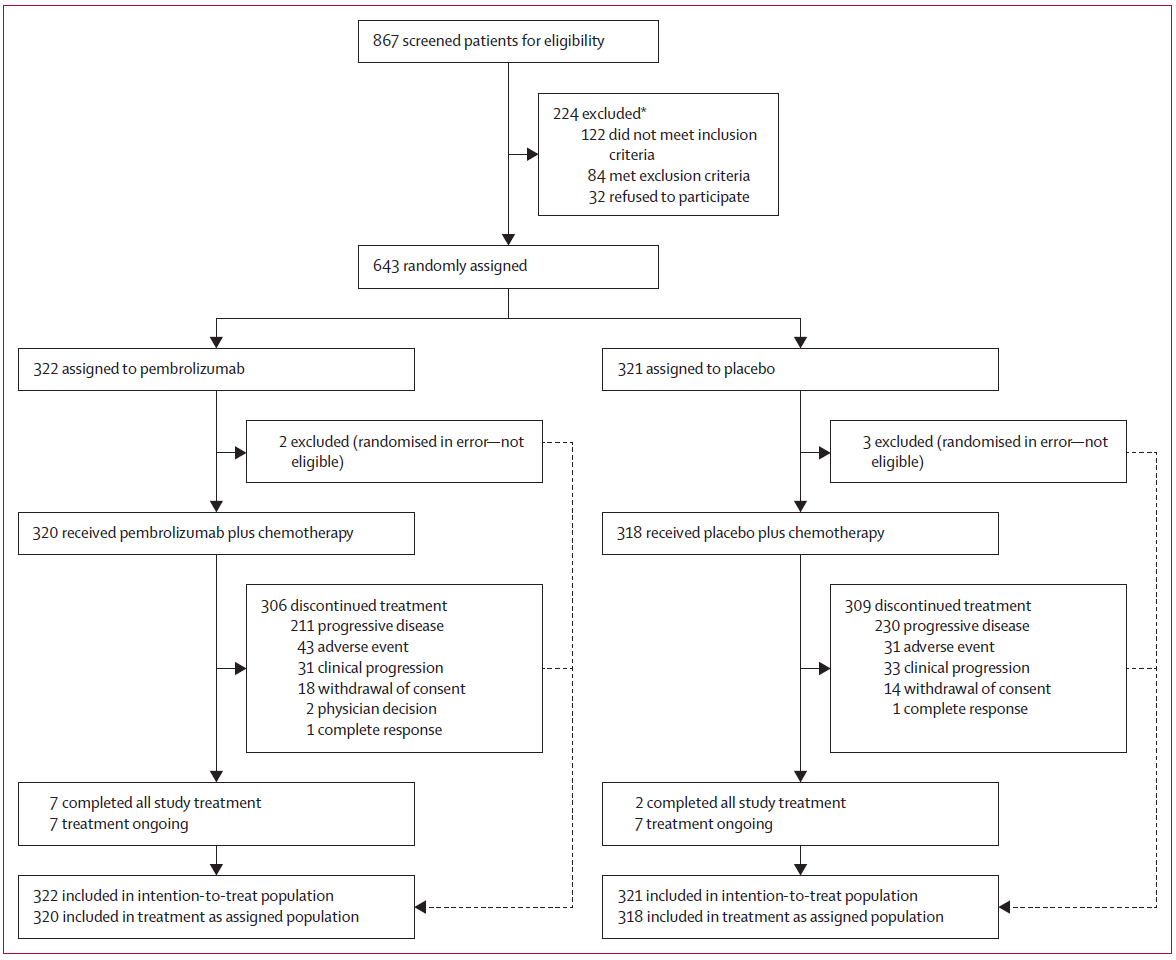
ENGOT-ov65/KEYNOTE-B96(NCT05116189)是一项随机、双盲、安慰剂对照的III期研究,在全球25个国家的187个妇科肿瘤中心开展。入组患者为经组织学确诊、既往接受过1-2线全身治疗(至少含一个铂类方案)且在末次铂类治疗后6个月内进展的铂耐药复发性卵巢癌成年女性。 2021年12月13日-2023年7月3日,共纳入643例患者,按1:1随机分配至: 试验组(n=322):帕博利珠单抗(Q6W,最多18个周期)+紫杉醇(第1、8、15天给药,每21天为一个周期,Q3W)±贝伐珠单抗(研究者决定是否使用,Q2W)。 对照组(n=321):安慰剂(Q6W,最多18个周期)+紫杉醇(第1、8、15天给药,每21天为一个周期,Q3W)±贝伐珠单抗(研究者决定是否使用,Q2W)。 随机化分层因素包括:是否使用贝伐珠单抗、地区、PD-L1表达水平等。 研究主要终点为研究者评估的基于RECIST 1.1版的无进展生存期(PFS);关键次要终点为总生存期(OS)。其他次要终点包括盲法独立中心评估PFS、ORR、缓解持续时间(DOR)以及患者报告结局。 研究设计 患者流程图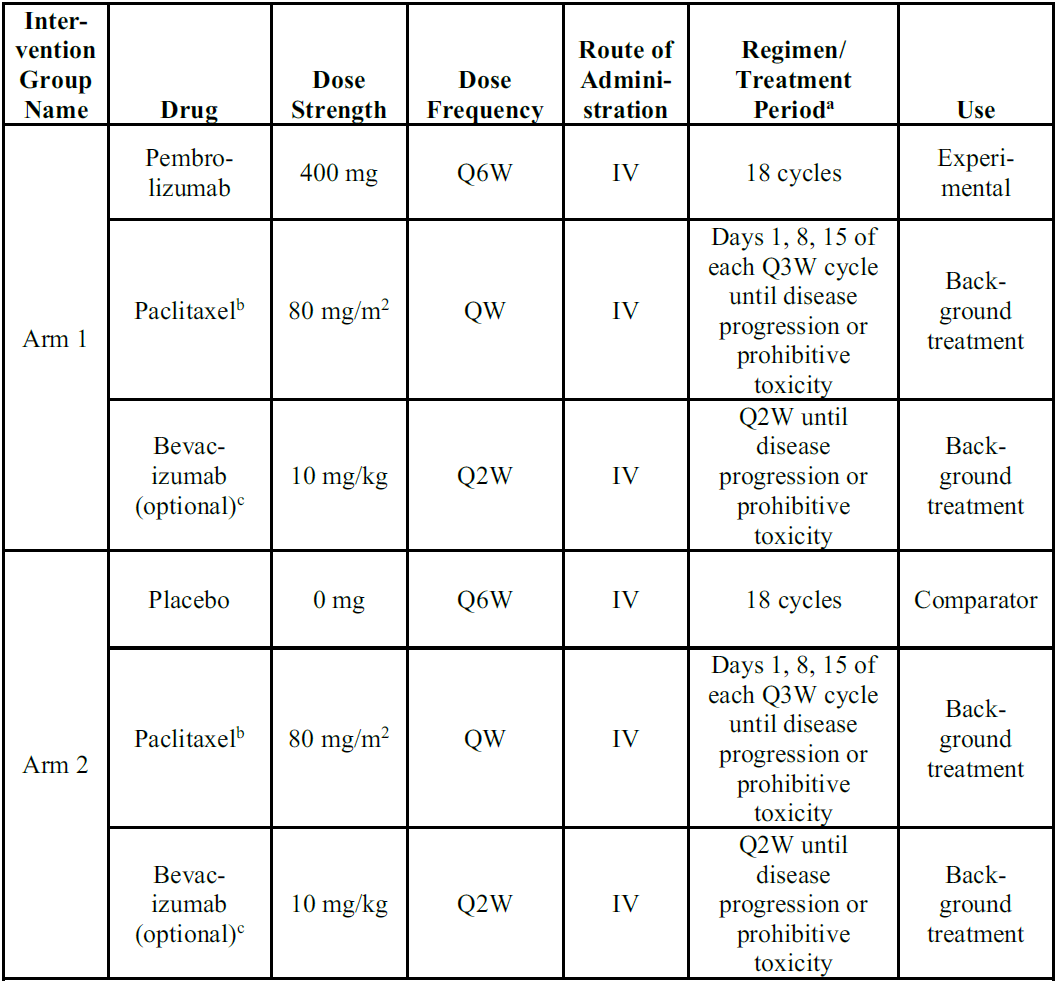
研究结果
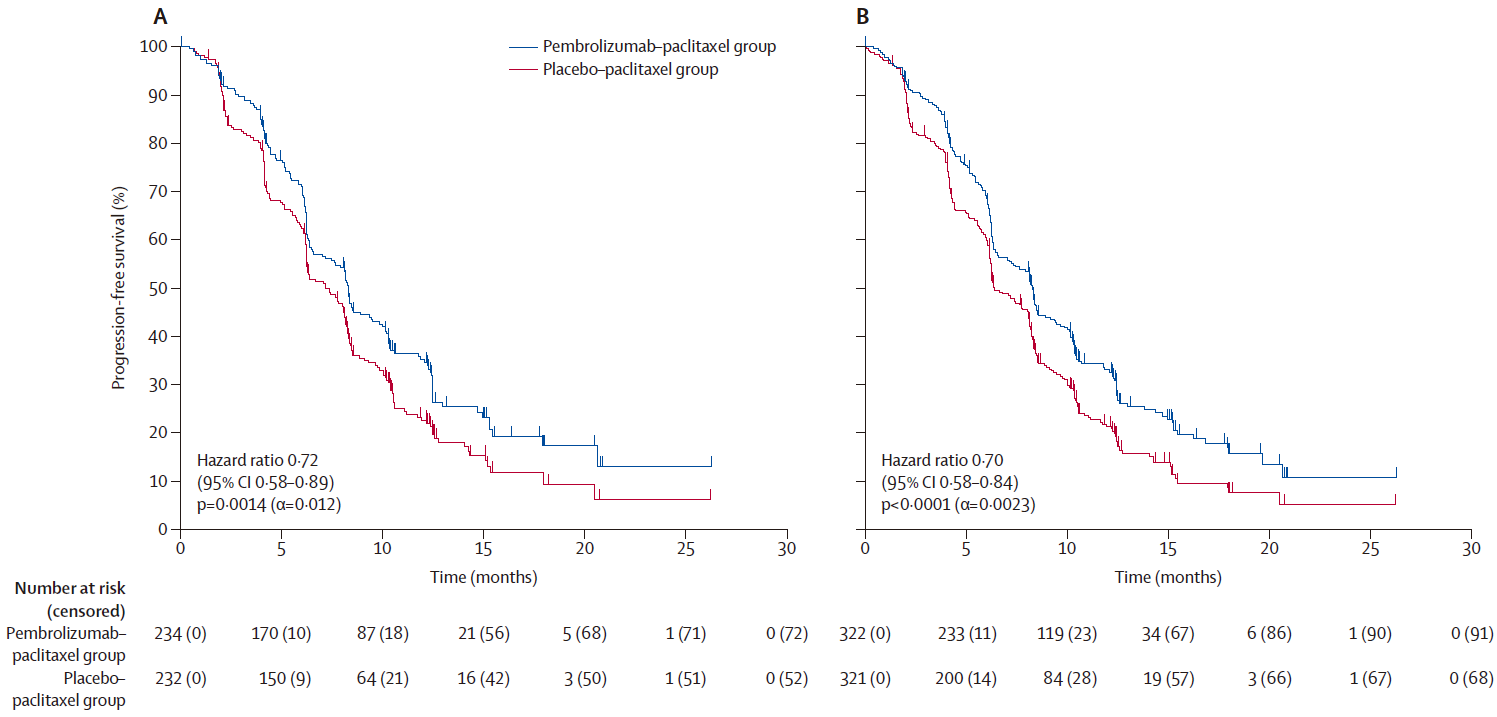
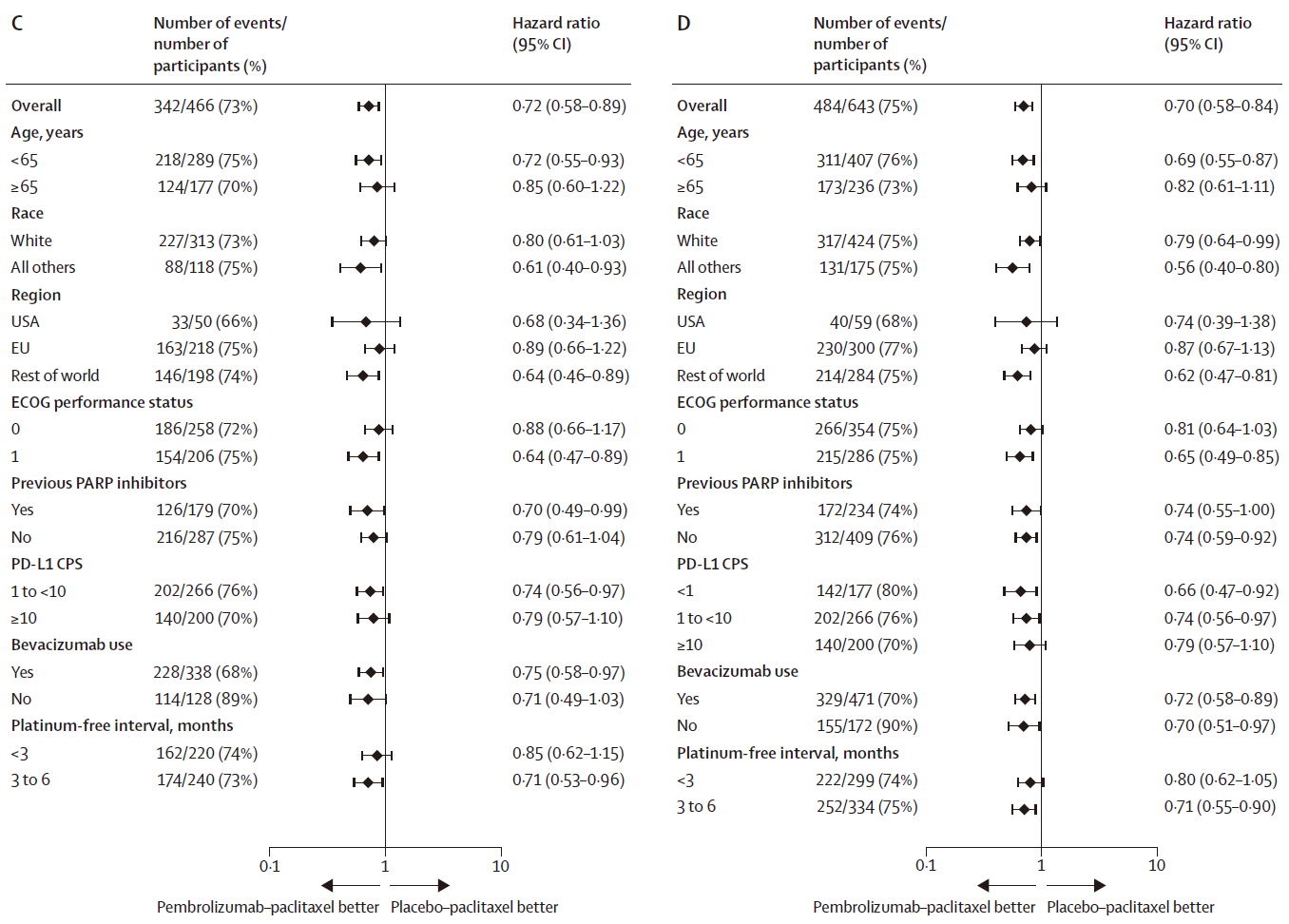
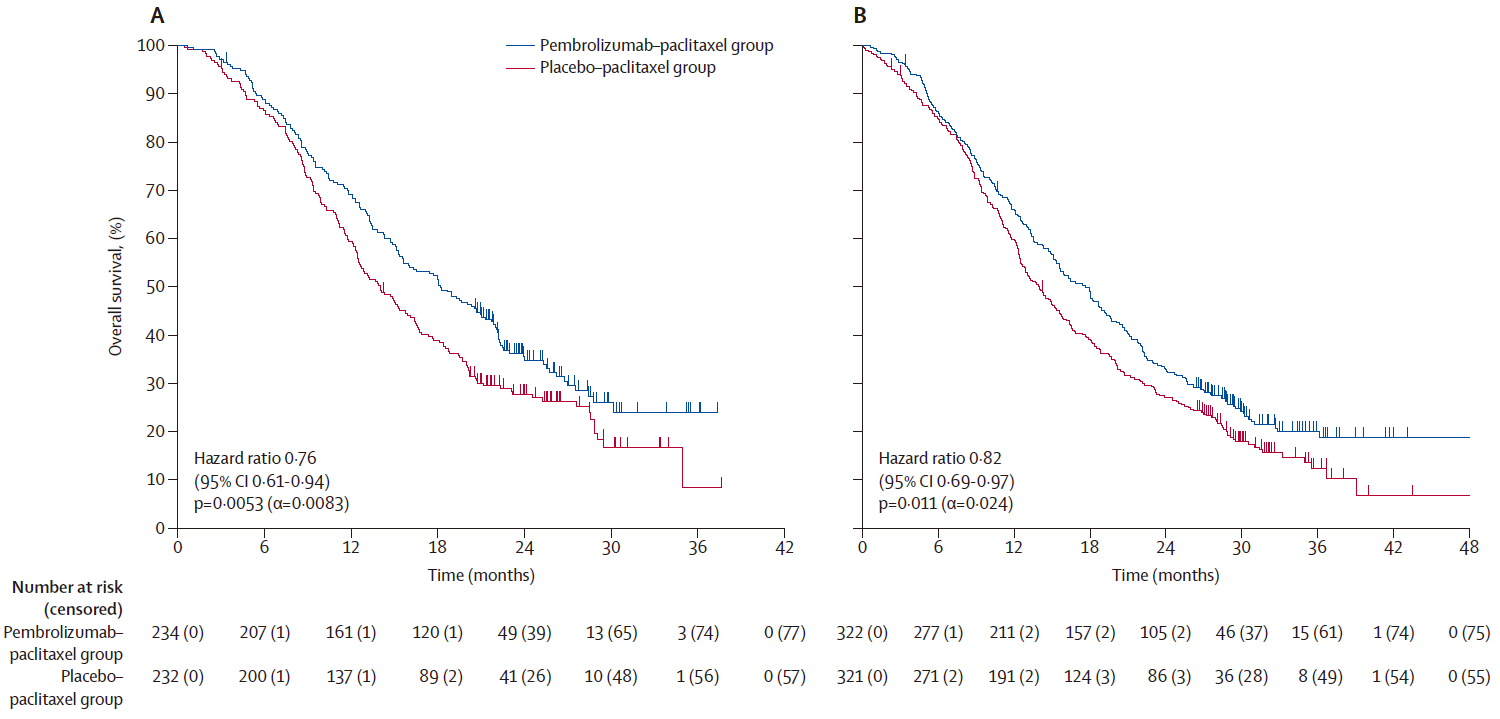
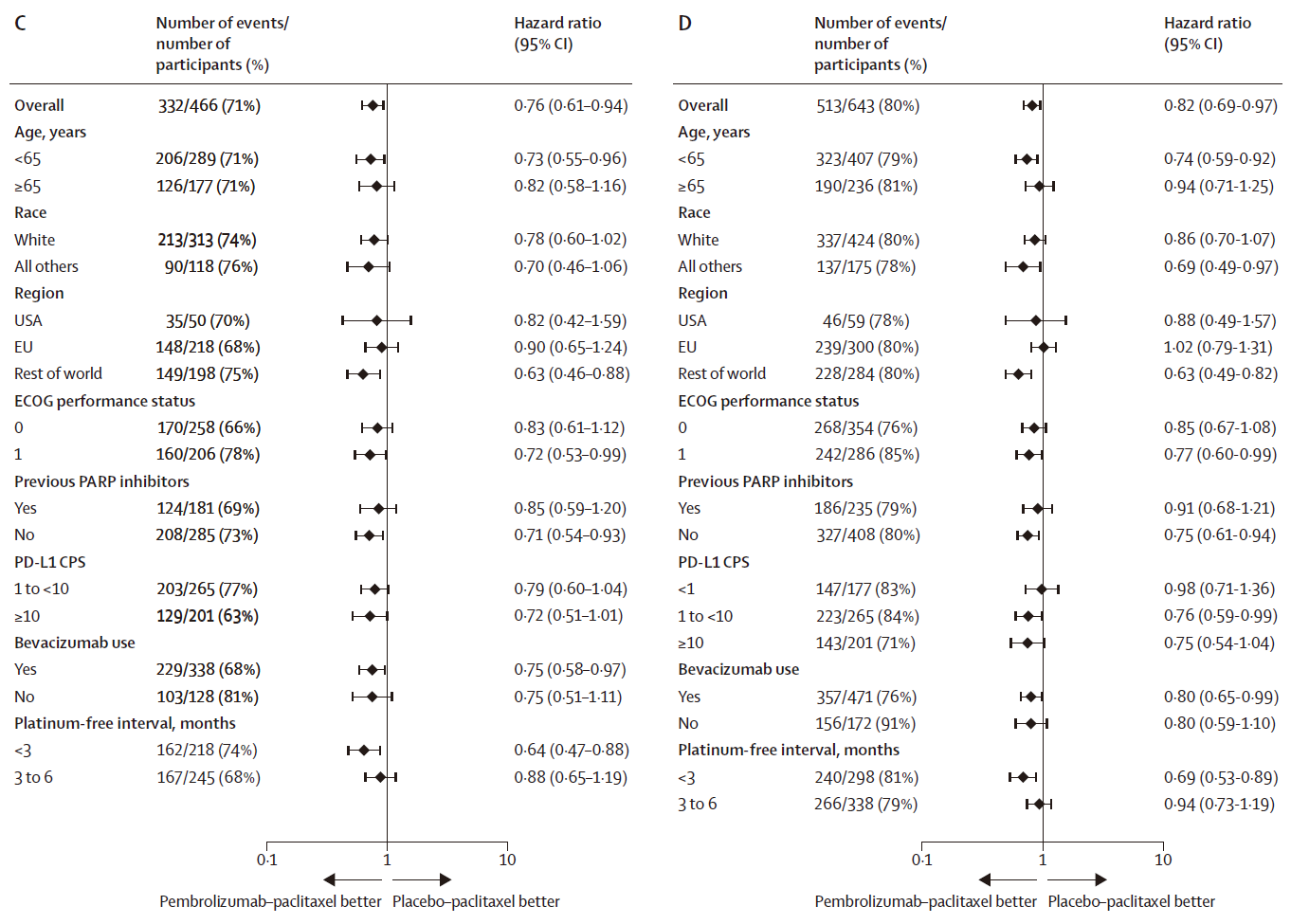
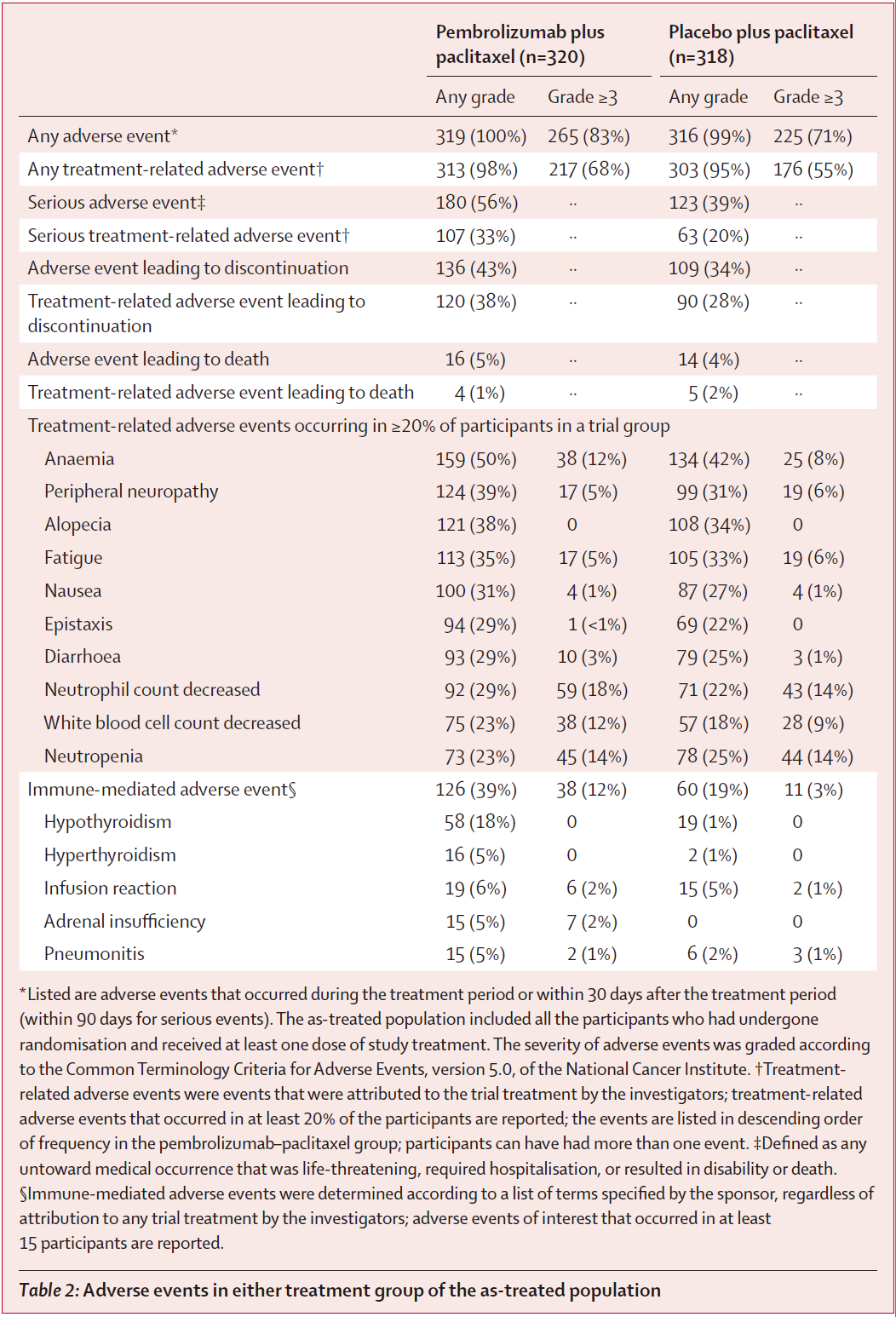
研究共纳入643例患者,两组基线特征均衡。 基线特征 疗效结果 PFS: 在首次中期分析(数据截止日期2024年4月3日,中位随访15.6个月)时,试验组PFS在PD-L1 CPS≥1人群及总人群中均达到预设的确证性疗效标准: PD-L1 CPS≥1人群:试验组与对照组中位PFS分别为8.3个月 vs 7.2个月(HR=0.72,95%CI 0.58-0.89,P=0.0014); 总人群:试验组与对照组中位PFS分别为8.3个月 vs 6.4个月(HR=0.70,95%CI 0.58-0.84,P<0.0001)。 Kaplan-Meier图:首次中期分析的PFS (A: PD-L1 CPS≥1人群;B: 总人群) 在包括年龄、既往PARP抑制剂暴露、无铂间期以及是否联合贝伐珠单抗等各个预设亚组中,PFS的获益具有高度一致性。BICR评估的PFS结果与研究者评估结果高度一致。 PFS亚组分析 (C: PD-L1 CPS≥1人群;D: 总人群) OS(里程碑突破点): 第二次中期分析(数据截止2025年3月5日,中位随访26.6个月)中,PD-L1 CPS≥1人群的中位OS已达到统计学显著性差异:试验组与对照组中位OS分别为18.2个月 vs 14.0个月(HR=0.76,95%CI 0.61-0.94,P=0.0053)。 最终分析(数据截止2025年9月5日,中位随访32.7个月)中,总体人群OS达到统计学显著性:两组中位OS分别为17.7个月 vs 14.0个月(HR=0.82,95%CI 0.69-0.97,P=0.011)。 Kaplan-Meier图:OS (A: PD-L1 CPS≥1人群[二次中期分析];B: 总人群[最终分析]) OS同样在各个亚组中均显示获益趋势。 OS亚组分析 (C: PD-L1 CPS≥1人群;D: 总人群) ORR: PD-L1 CPS≥1人群:试验组与对照组ORR分别为53% vs 47%; 总人群:50% vs 41%。 DOR: PD-L1 CPS≥1人群:试验组与对照组中位DOR分别为10.4个月 vs 8.1个月;DOR≥12个月分别为47% vs 30%; 总人群:中位DOR 10.4个月 vs 7.9个月;DOR≥12个月47% vs 28%。 安全性结果 安全性分析纳入638例接受至少1次治疗的患者(试验组320例,对照组318例): 不良事件发生率:试验组和对照组的全因不良事件发生率分别为100%和99%。≥3 级治疗相关不良事件(TRAEs)在试验组更常见(68% vs 55%); 最常见TRAEs(任意级别,≥20%):贫血、周围神经病变、脱发、疲劳、恶心,这与紫杉醇已知毒性谱一致; 免疫相关不良事件:试验组39%,≥3级12%;对照组19%,≥3级3%,以甲状腺功能减退/亢进、输液反应、肾上腺皮质功能不全、肺炎最为常见,均为可控性不良反应; 致死性事件:治疗相关死亡事件两组分别为试验组4例(1%),对照组5例(2%)。 不良事件 患者报告结局方面,第24周时两组总体健康状况/生活质量稳定或改善的比例相当(试验组59% vs 对照组61%),腹部及胃肠道症状量表评分亦相近(74% vs 68%),提示联合帕博利珠单抗未显著影响患者的生活质量。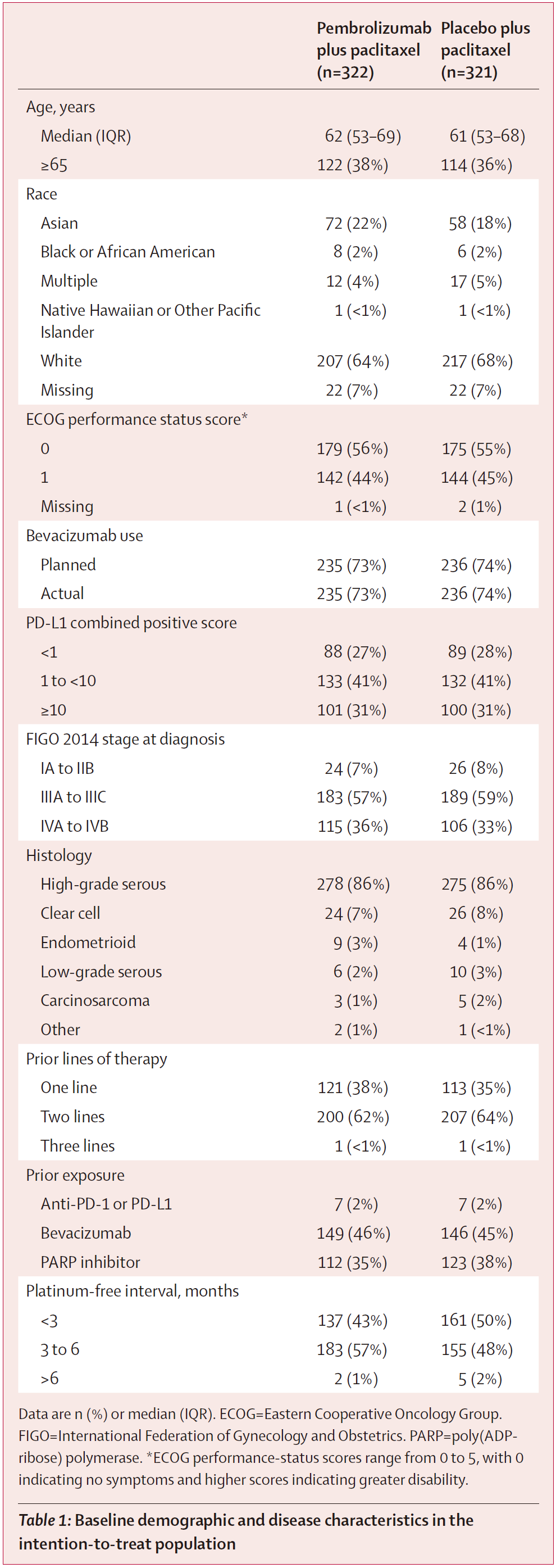
研究结论
综上所述,ENGOT-ov65/KEYNOTE-B96研究以坚实的循证医学证据表明:在既往接受过1-2线全身治疗的铂耐药复发性卵巢癌患者中,帕博利珠单抗联合节拍紫杉醇±贝伐珠单抗能够带来具有统计学意义和临床意义的PFS与OS双重改善。该方案的安全性特征与已知单药的安全性一致,未增加不可控的毒性风险。 这一成果不仅为临床医生提供了一种有效的新治疗方案,更重要的是,它验证了“节拍化疗联合免疫治疗”这一策略在卵巢癌中的科学合理性,为未来更深入的探索指明了方向。该方案已被确立为符合条件患者的新标准治疗。
来源:肿瘤界