2026年4月9日,中国医学科学院肿瘤医院孙永琨教授、北京市朝阳区三环肿瘤医院吴贵福教授、淮安市第一人民医院仲小敏教授团队在Signal Transduction and Targeted Therapy发表了题为“Irinotecan with trifluridine/tipiracil and bevacizumab for second-line metastatic colorectal cancer: a phase II multicenter study”的临床研究。该研究首次在中国人群中系统评估了伊立替康联合TAS-102及贝伐珠单抗三药方案作为转移性结直肠癌二线治疗的疗效与安全性。尽管主要终点客观缓解率未达预设的30%,但研究显示出可管理的安全性特征及具有临床意义的生存获益,为转移性结直肠癌二线治疗策略的优化提供了重要循证参考。

研究背景
结直肠癌(CRC)是全球第三大最常见恶性肿瘤,也是癌症相关死亡的第二大原因。在中国,CRC的发病率和死亡率近十年来显著上升,分别位列第二和第四。对于不可切除的转移性结直肠癌(mCRC),绝大多数患者的分子特征为微卫星稳定(MSS),治疗核心仍以化疗联合靶向治疗为主。一线及二线标准化疗骨架通常包括氟尿嘧啶类药物联合奥沙利铂、伊立替康或两者组合,并可叠加贝伐珠单抗等抗血管生成靶向药物或(针对RAS野生型肿瘤)表皮生长因子受体(EGFR)抑制剂(西妥昔单抗或帕尼单抗)进一步改善预后。尽管如此,mCRC的整体预后仍不容乐观,五年生存率仅约12%,新型有效治疗策略的开发迫在眉睫。 TAS-102是一种口服细胞毒性药物,由曲氟尿苷(trifluorothymidine,FTD)与替匹嘧啶(tipiracil,TPI)组成,后者为强效胸苷磷酸化酶抑制剂,可阻止FTD降解。TAS-102的抗肿瘤机制与传统细胞毒药物不同,临床前研究已证实其对5-氟尿嘧啶(5-FU)耐药的肿瘤仍具活性。RECOURSE及TERRA两项III期临床研究奠定了TAS-102单药用于难治性mCRC的地位,但单药疗效有限,亟需探索更有效的联合治疗策略。 临床前研究表明,TAS-102与伊立替康或贝伐珠单抗联合,在CRC细胞系及人源异种移植模型中均显示出协同抗肿瘤活性。SN-38(伊立替康的活性代谢产物)与FTD协同作用可诱导DNA损伤,并使细胞周期阻滞于G2/M期,为TAS-102与伊立替康联合提供了充分的机制支撑。SUNLIGHT III期研究进一步在临床层面验证了TAS-102联合贝伐珠单抗优于TAS-102单药,使该方案获批用于mCRC三线治疗。 该研究团队此前已完成了一项探索性II期研究,评估伊立替康+TAS-102+贝伐珠单抗三药联合用于mCRC三线及以上治疗的疗效与安全性,结果显示ORR达25.8%,中位无进展生存期(PFS)为9.2个月,提示该方案具有良好的抗肿瘤活性。在此基础上,研究者进一步开展了本研究,首次在中国评估该三药方案用于mCRC二线治疗的疗效与安全性。
研究设计
本研究为开放标签、单臂、多中心II期临床试验(NCT06202001),在中国四家中心开展(中国医学科学院肿瘤医院、三环肿瘤医院、淮安第一人民医院、运城中心医院)。研究纳入一线氟尿嘧啶联合奥沙利铂方案治疗进展或辅助化疗结束后6个月内复发的不可切除mCRC患者。 给药方案依据前期I期剂量爬坡试验确定的推荐II期剂量(RP2D): 诱导期:伊立替康150 mg/m²(第1天,静脉滴注)+ TAS-102 30 mg/m²(第1~5天,每日两次口服)+贝伐珠单抗5 mg/kg(第1天,静脉滴注),每14天为一周期,最多12周期。 维持期:TAS-102联合贝伐珠单抗继续治疗,直至疾病进展、出现不可耐受毒性或患者撤回知情同意。 主要终点为客观缓解率(ORR)。次要终点包括无进展生存期(PFS)、总生存期(OS)及安全性。基于历史数据约15% ORR为参照,本研究预设目标ORR为30%,纳入约58例患者可提供80%检验效能(双侧α=0.05)。
研究结果
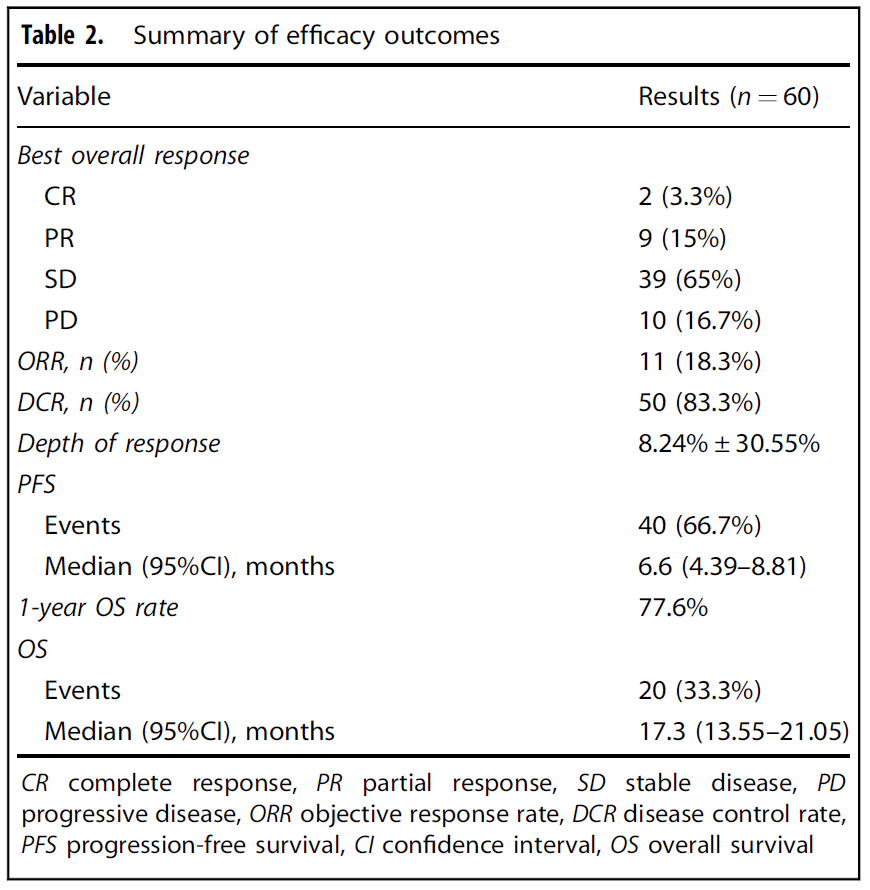
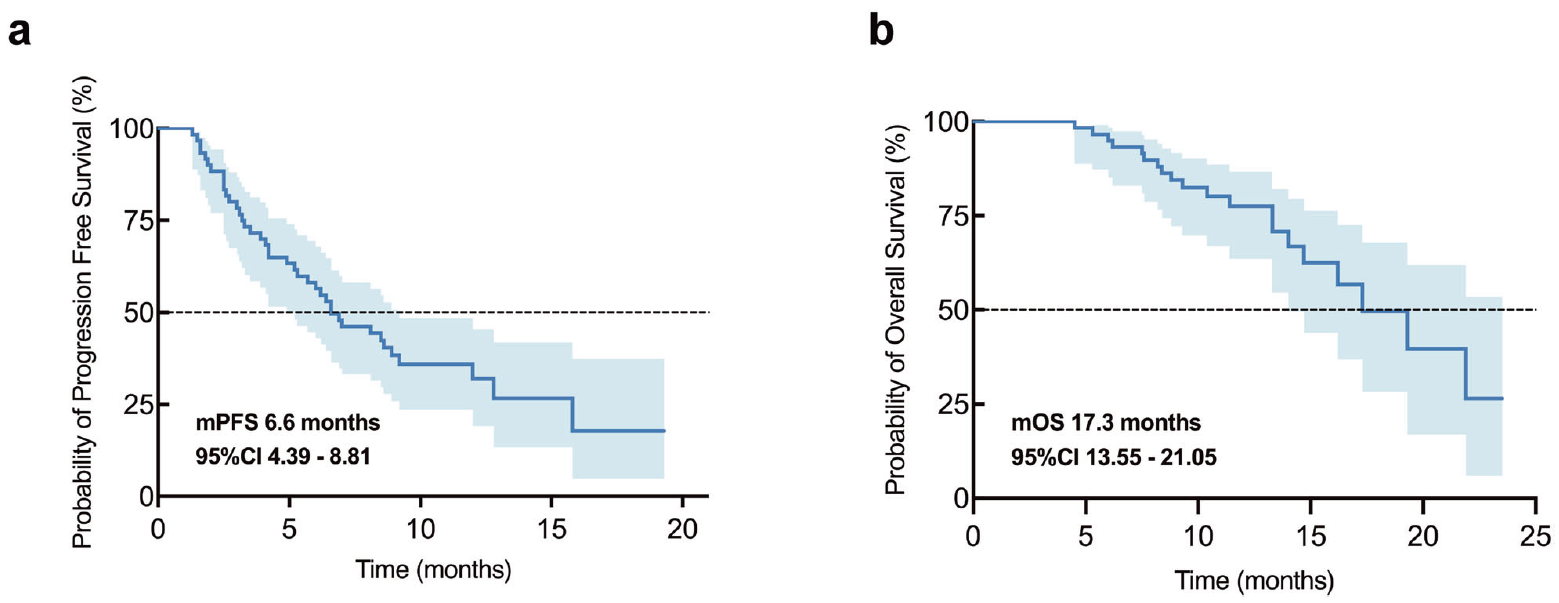
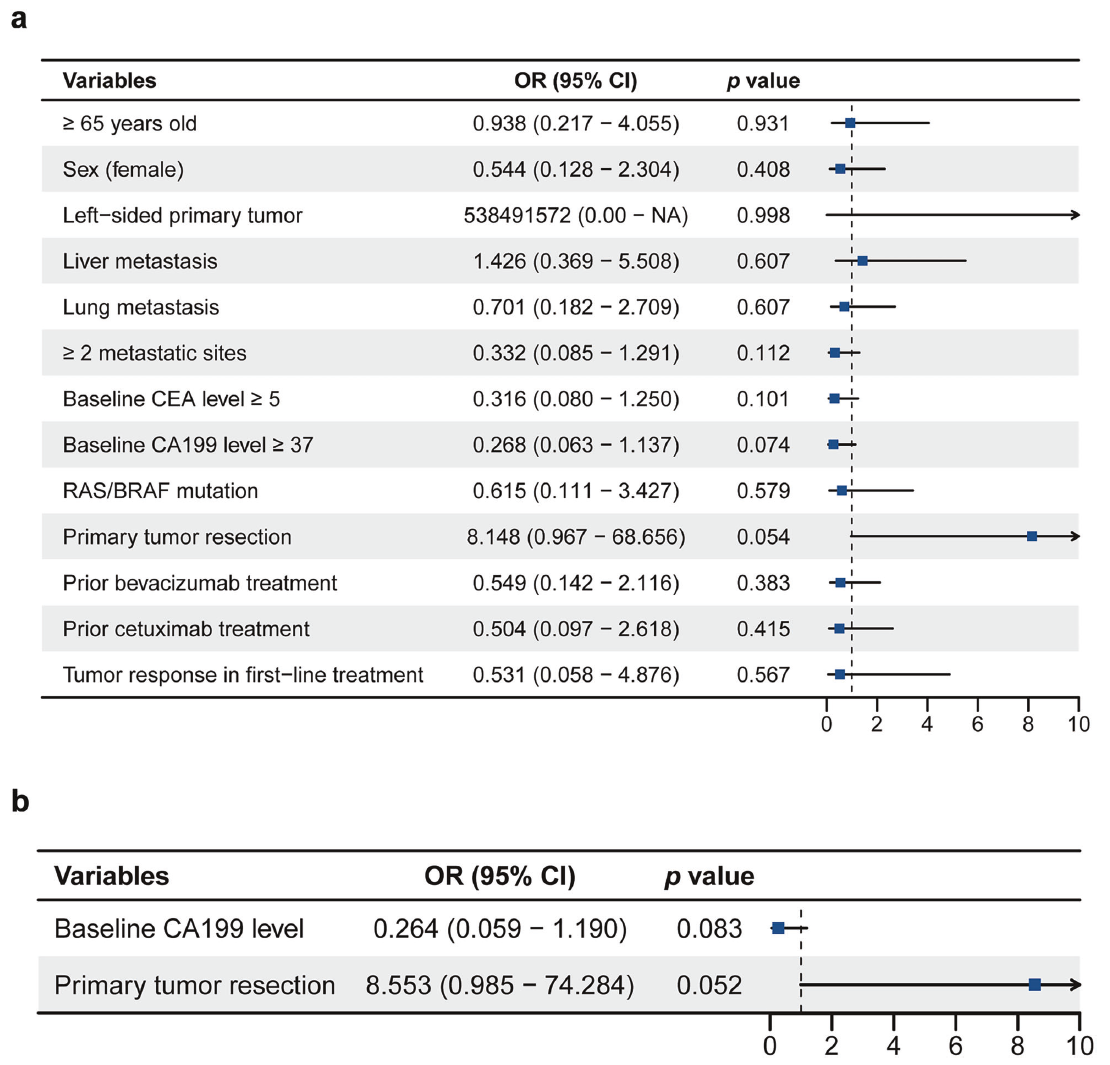
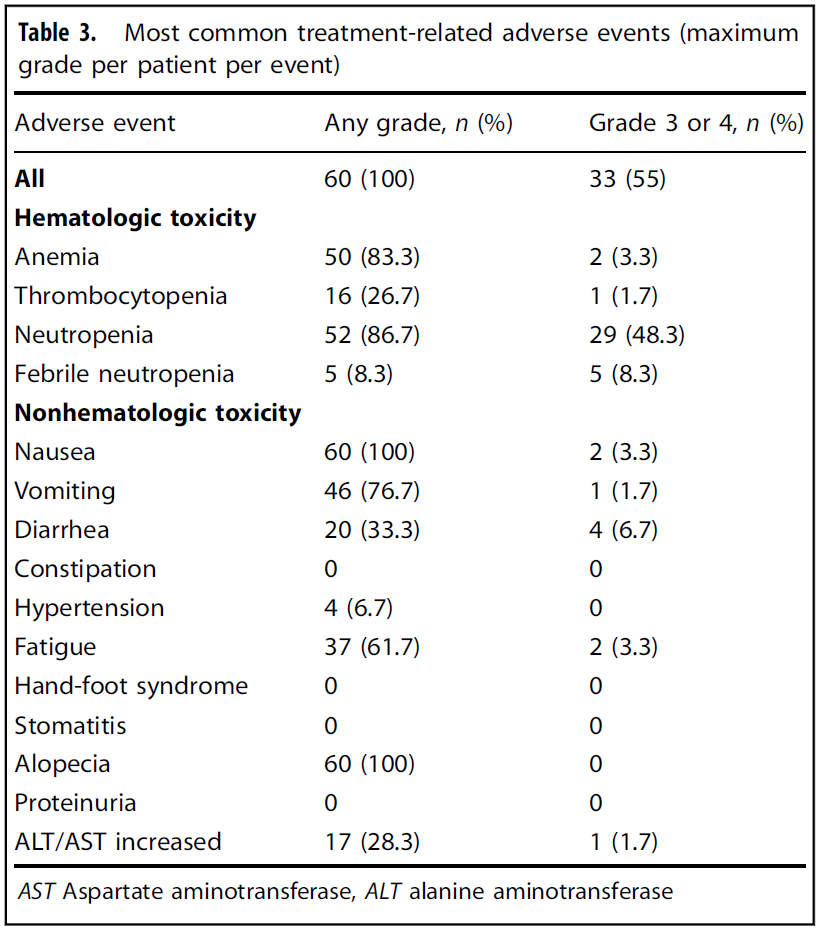
2023年10月-2024年8月,研究共纳入60例患者,所有患者均接受至少一次研究药物治疗。 基线特征 疗效结果 截至数据截止日(2024年12月31日),中位随访时间为13.3个月(95%CI 11.07-15.53),40例(66.7%)患者仍存活。全部60例入组患者均接受了至少一次基线后肿瘤评估,纳入疗效分析。中位治疗周期数为6个周期(范围:3~20)。 最佳总体疗效评估显示,2例达到完全缓解(CR),9例达到部分缓解(PR),ORR为18.3%(11/60),未达到预设的30%主要终点目标。疾病控制率(DCR)达83.3%(50/60),其中39例评估为疾病稳定(SD)的患者中,28例观察到不同程度的肿瘤缩小。平均缓解深度(DpR)为8.24%(标准差±30.55%)。 疗效结果 距靶病灶最佳变化比 中位PFS为6.6个月(95%CI 4.39-8.81),40例(66.7%)患者出现PFS事件。中位OS为17.3个月(95%CI 13.55-21.05),20例(33.3%)患者发生了OS事件;OS数据尚未成熟,最终结果需延长随访获取。1年总生存率为77.6%。 Kaplan‒Meier生存图(a:PFS;b:OS) 亚组分析中,年龄、性别、体能状态、原发肿瘤位置、转移部位数量、基线CEA/CA19-9水平均未显示出对PFS或OS的显著影响。值得关注的是,即使在RAS/BRAF突变及伴肝转移的患者亚组中,治疗疗效依然得到了保持。此外,既往原发肿瘤切除(含根治或姑息手术)的患者显示出显著更优的生存获益:中位OS为21.9个月 vs 16.2个月(P=0.048),中位PFS为8.9个月 vs 5.2个月(P=0.004)。此外,左侧原发肿瘤患者在OS(19.3 vs 16.2个月,P=0.155)和PFS(8.1 vs 5.05个月,P=0.143)方面均观察到改善趋势,但未达统计学显著性。既往贝伐珠单抗或西妥昔单抗治疗史对OS和PFS无显著影响。 ORR亚组分析(a:单因;b:多因) 安全性结果 全部60例患者均纳入安全性分析。任意级别治疗相关不良事件(TRAEs)发生率为100%,3/4级TRAEs发生率为55%(33/60例)。全组无治疗相关死亡。毒性谱以血液学及胃肠道毒性为主,与伊立替康和TAS-102的已知毒性特征一致。 TRAEs 历史数据显示,基于伊立替康的二线化疗方案ORR在4%~12.5%之间,联合VEGF抑制剂后mPFS为5.7~7.2个月,mOS为11.2~18.1个月。本研究ORR 18.3%、mPFS 6.6个月、mOS 17.3个月的结果与历史对照相当,但未达到预设ORR 30%的主要终点,按预设统计标准属于阴性研究。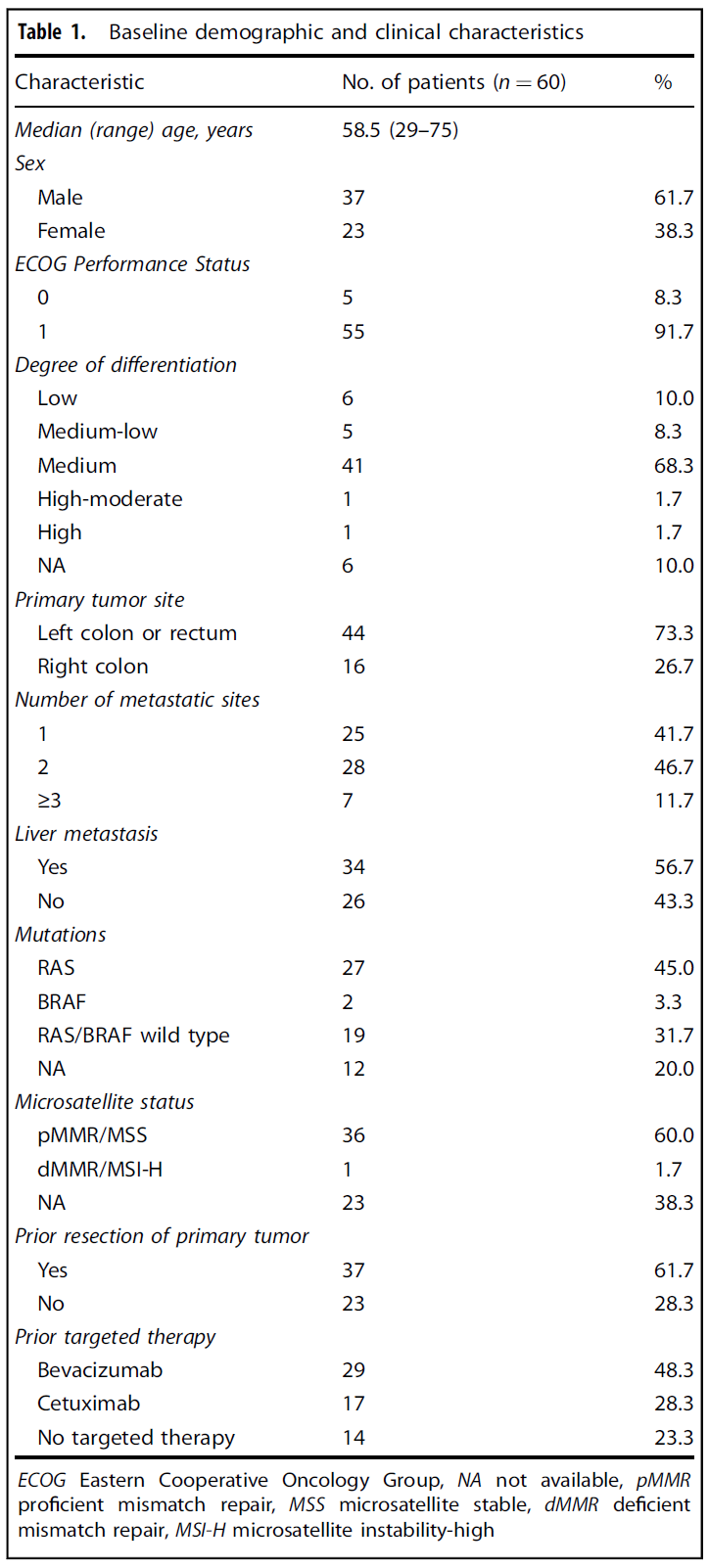
研究结论
本研究作为首个在中国人群评估伊立替康+TAS-102+贝伐珠单抗三药联合用于mCRC二线治疗的多中心前瞻性临床研究,初步证明了该方案在一线氟尿嘧啶及奥沙利铂化疗失败后mCRC患者中的可行性和可接受的安全性,尤其对于原发灶已切除的患者可能获益更显著。尽管未能达到预设的ORR主要终点,但其长达17.3个月的中位OS为临床提供了重要参考。未来,有必要在更同质化的患者群体中开展前瞻性随机对照试验,以获取更可靠的数据来指导临床实践。 来源:肿瘤界