2026年4月15日,广东省人民医院吴一龙教授、涂海燕教授,河南省肿瘤医院赵艳秋教授等在《新英格兰医学杂志》(NEJM)上发表了题为“First-Line Zongertinib in Advanced HER2-Mutant Non–Small-Cell Lung Cancer”的研究。这是一项基于Beamion LUNG-1研究的多队列临床试验结果,首次报告了宗艾替尼(zongertinib)在HER2突变晚期非鳞非小细胞肺癌初治患者中的疗效与安全性。研究显示,宗艾替尼一线治疗的客观缓解率高达76%,中位缓解持续时间15.2个月,中位无进展生存期14.4个月,且不良反应总体可控,为HER2突变NSCLC患者带来了首个一线靶向治疗新选择。

研究背景
肺癌仍是全球癌症相关死亡的首要原因。人表皮生长因子受体2(HER2;亦称ERBB2)突变发生于约2%~4%的非小细胞肺癌(NSCLC)中,主要位于酪氨酸激酶结构域,与其他HER2改变(如扩增、过表达)有本质区别。 HER2突变NSCLC是一种高度侵袭性疾病,预后差,脑转移发生率高。尽管EGFR突变、ALK重排等驱动基因阳性NSCLC已相继获得高效靶向药物,HER2突变NSCLC的靶向治疗进展却明显滞后。在本研究发表之前,德曲妥珠单抗(Trastuzumab Deruxtecan,T-DXd)是唯一获批用于经治患者的HER2靶向药物,但其为静脉注射的抗体药物偶联物(ADC),且存在间质性肺疾病等严重毒性风险。对于初治患者,标准方案仍为含铂化疗±免疫治疗,中位无进展生存期(PFS)不足7个月,疗效十分有限。因此,一线HER2靶向治疗的缺失是该领域最迫切的临床未满足需求之一。 宗艾替尼(zongertinib,BI1810631)是一种口服、不可逆、HER2选择性酪氨酸激酶抑制剂(TKI),其关键特点在于选择性抑制HER2的同时保留野生型表皮生长因子受体(EGFR)的正常信号传导,从而在理论上降低与EGFR抑制相关的毒副反应。基于Beamion LUNG-1研究的前期数据(队列1、3、5,经治患者),宗艾替尼已先后获美国(加速批准)、中国(附条件批准)及日本批准用于经治HER2突变晚期NSCLC患者。本文重点报告了Beamion LUNG-1研究中队列2与队列4的结果。
研究设计
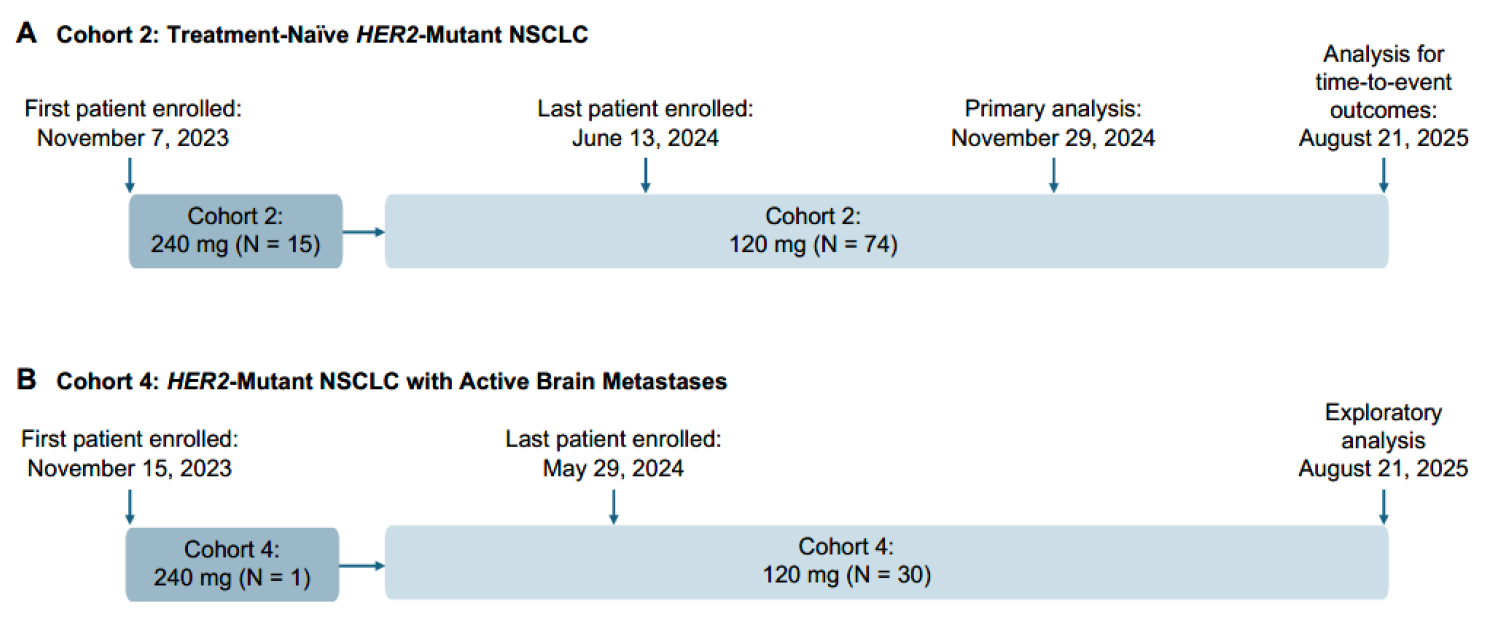
Beamion LUNG-1研究(NCT04886804)是一项1a-1b期多队列开放标签临床试验,旨在评估宗艾替尼在HER2突变晚期或转移性非鳞NSCLC患者中的疗效与安全性。研究纳入年龄≥18岁、经组织学或细胞学确诊为晚期/转移性NSCLC、伴HER2酪氨酸激酶结构域突变、且具有至少一个可测量病灶的患者。 本次报告重点聚焦以下两个队列: 队列2:初治晚期非鳞NSCLC患者,主要评估一线宗艾替尼120 mg剂量的疗效与安全性;同时纳入了在剂量选择分析前已入组、接受240 mg剂量的15例患者作为参考。主要终点为经盲态独立中心评审(BICR) 根据RECIST 1.1标准评估的客观缓解率(ORR)。 队列4:伴活动性脑转移的HER2突变NSCLC患者(初治或经治),为探索性队列。主要终点为经BICR根据神经肿瘤脑转移疗效评估标准(RANO-BM)评估的颅内ORR。 Beamion LUNG-1研究设计 Beamion LUNG-1研究队列2和队列4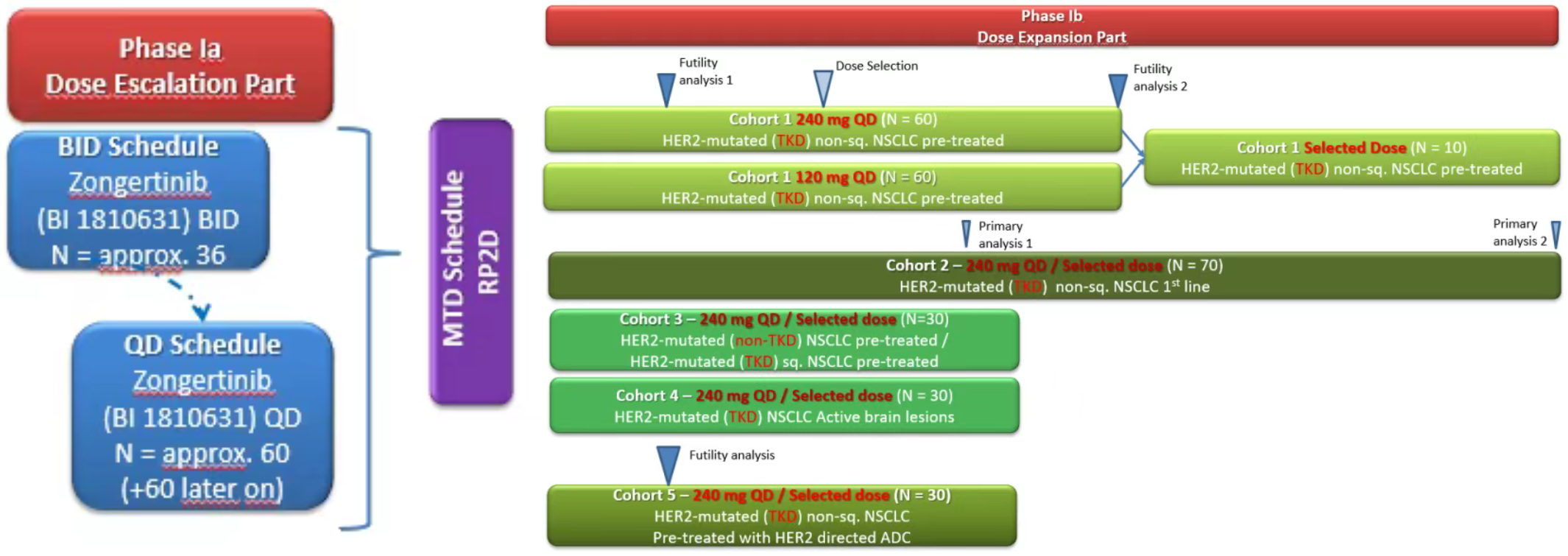
研究结果
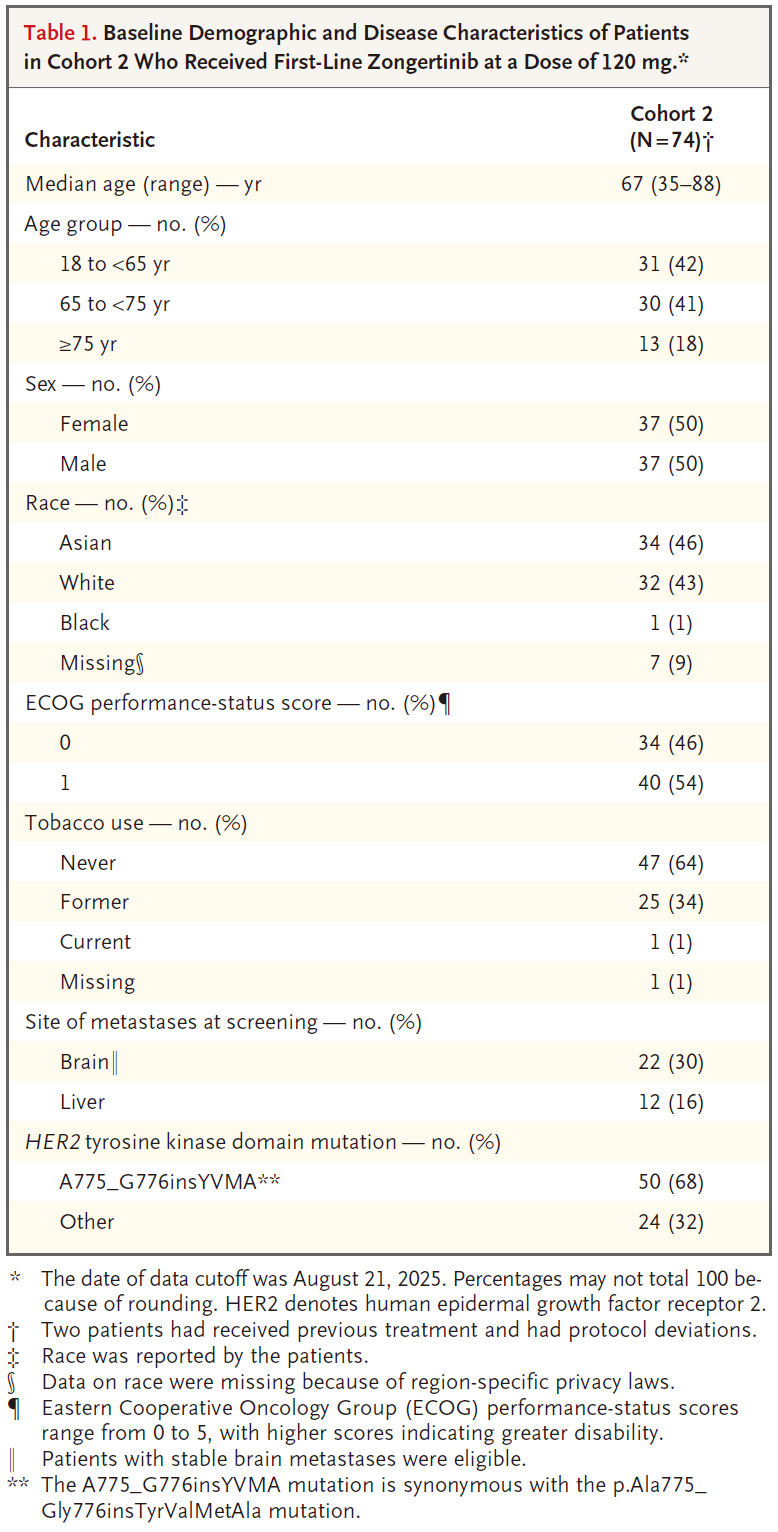
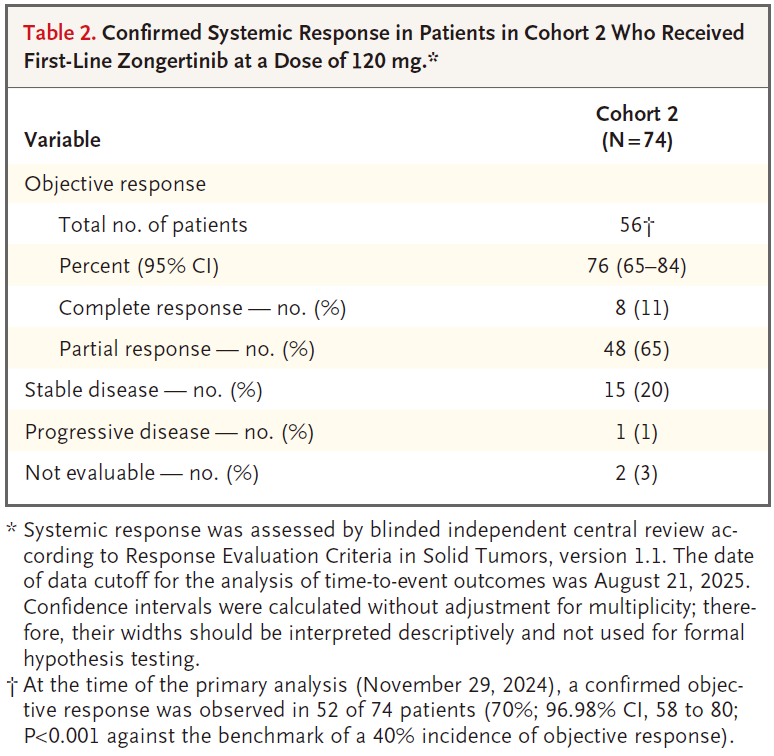
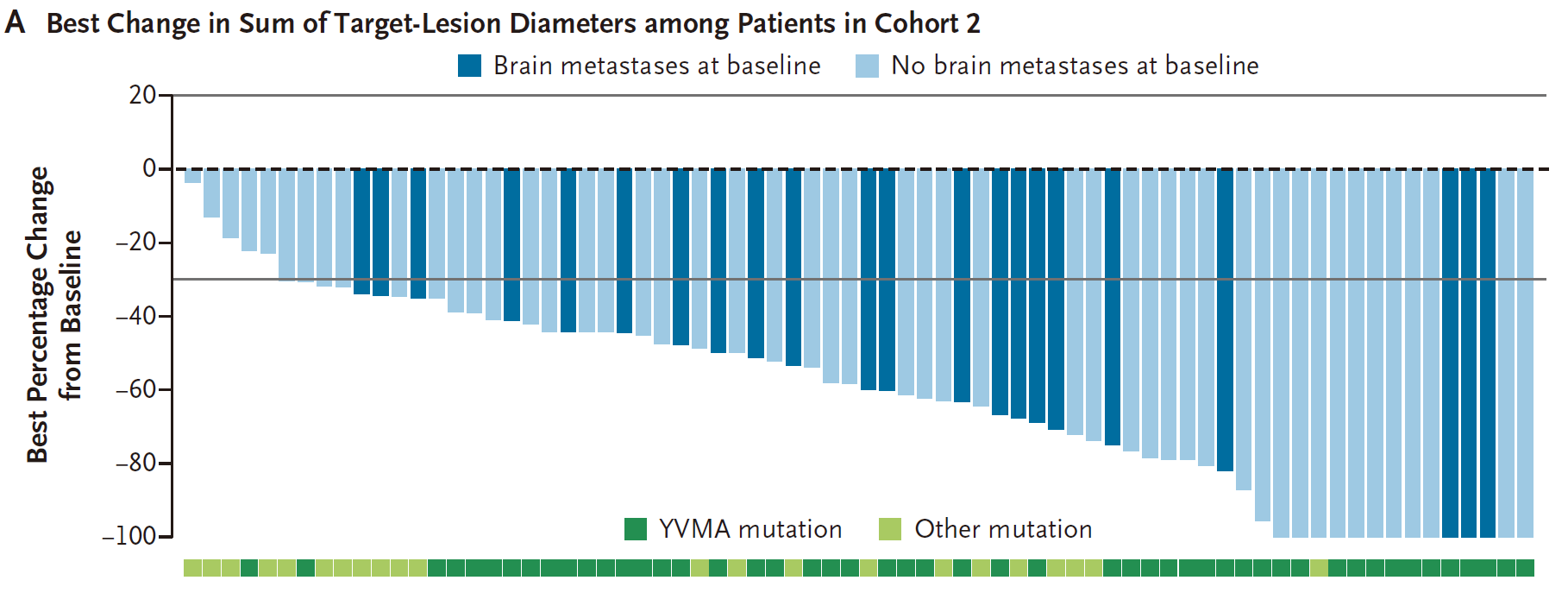
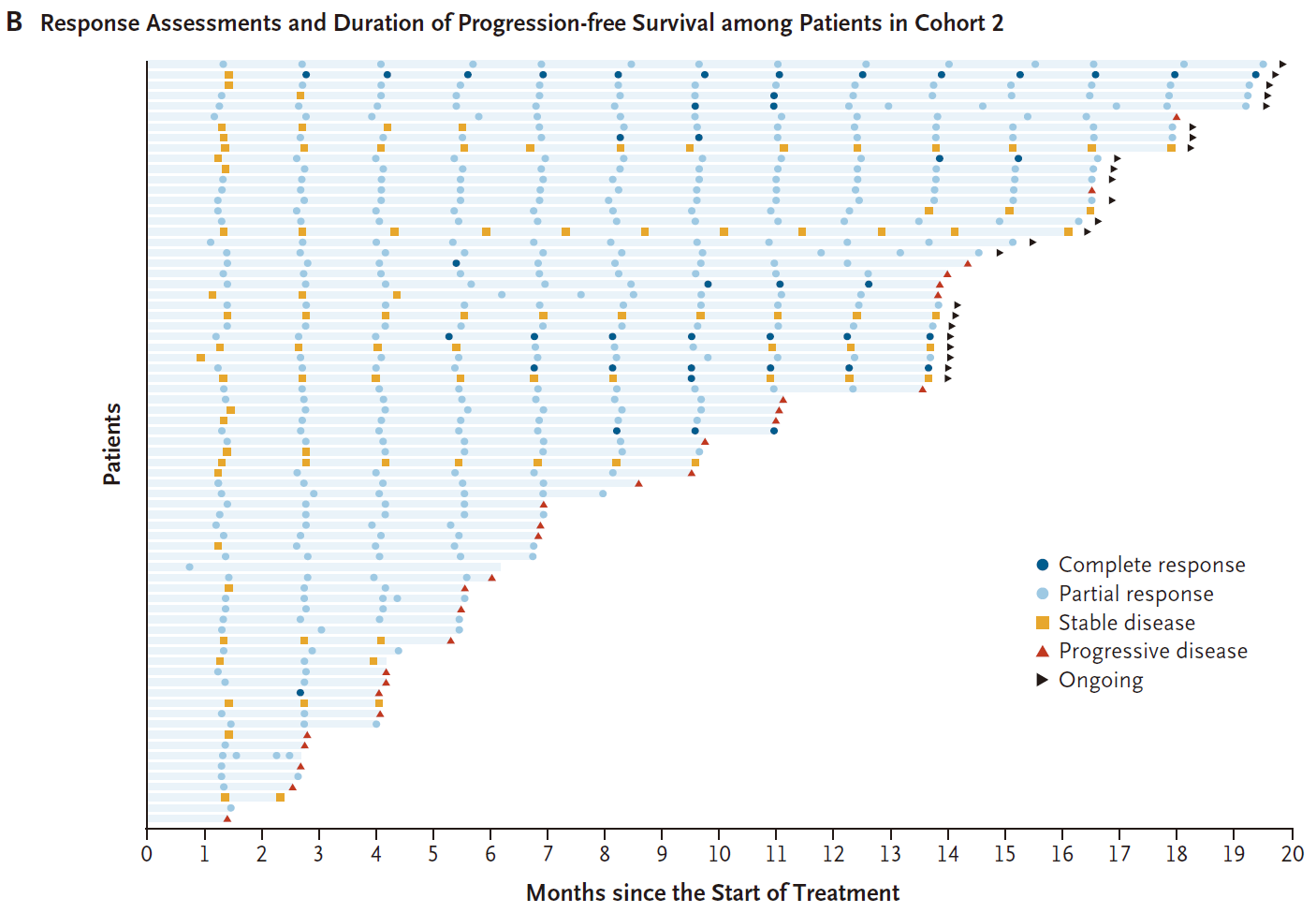
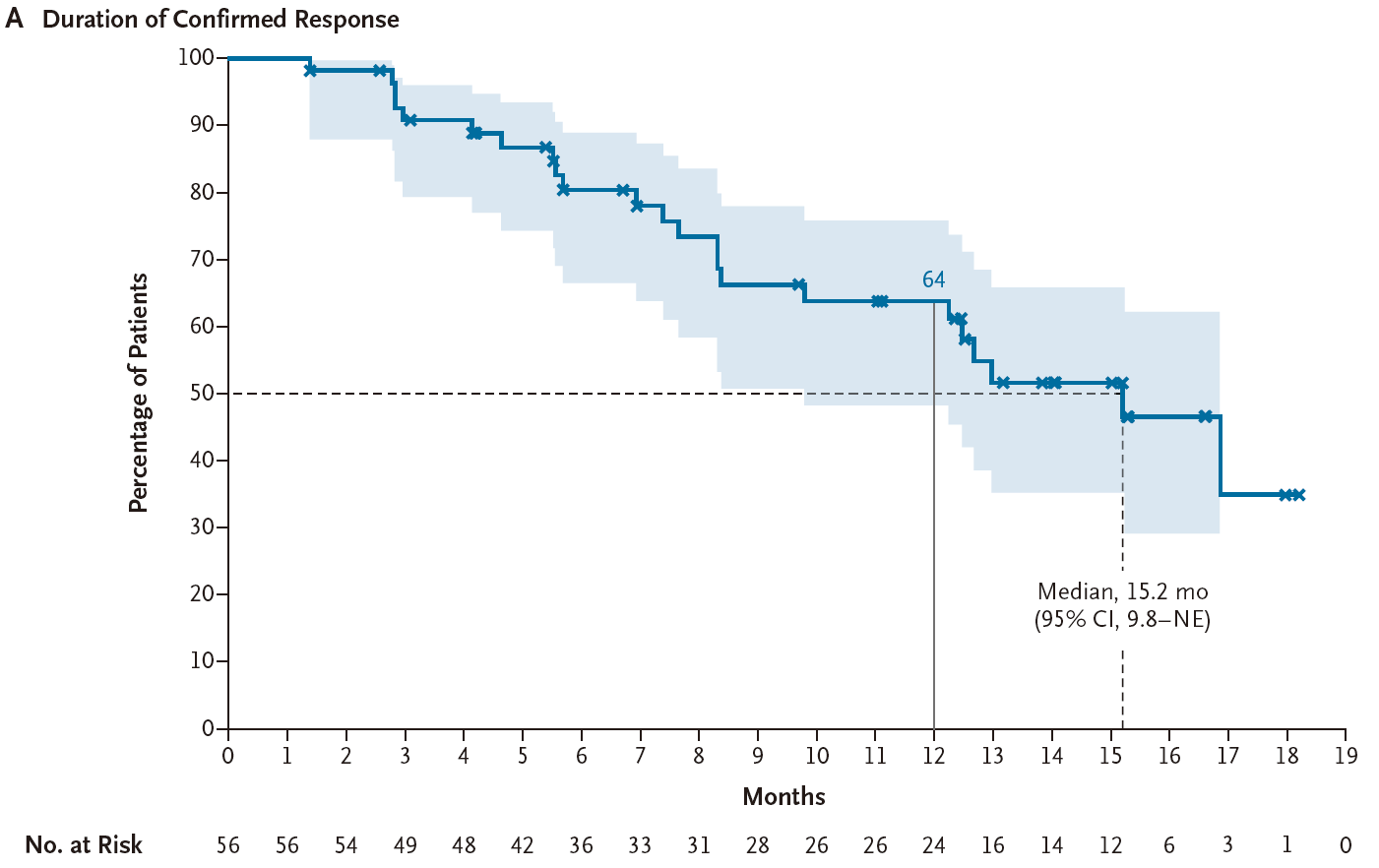
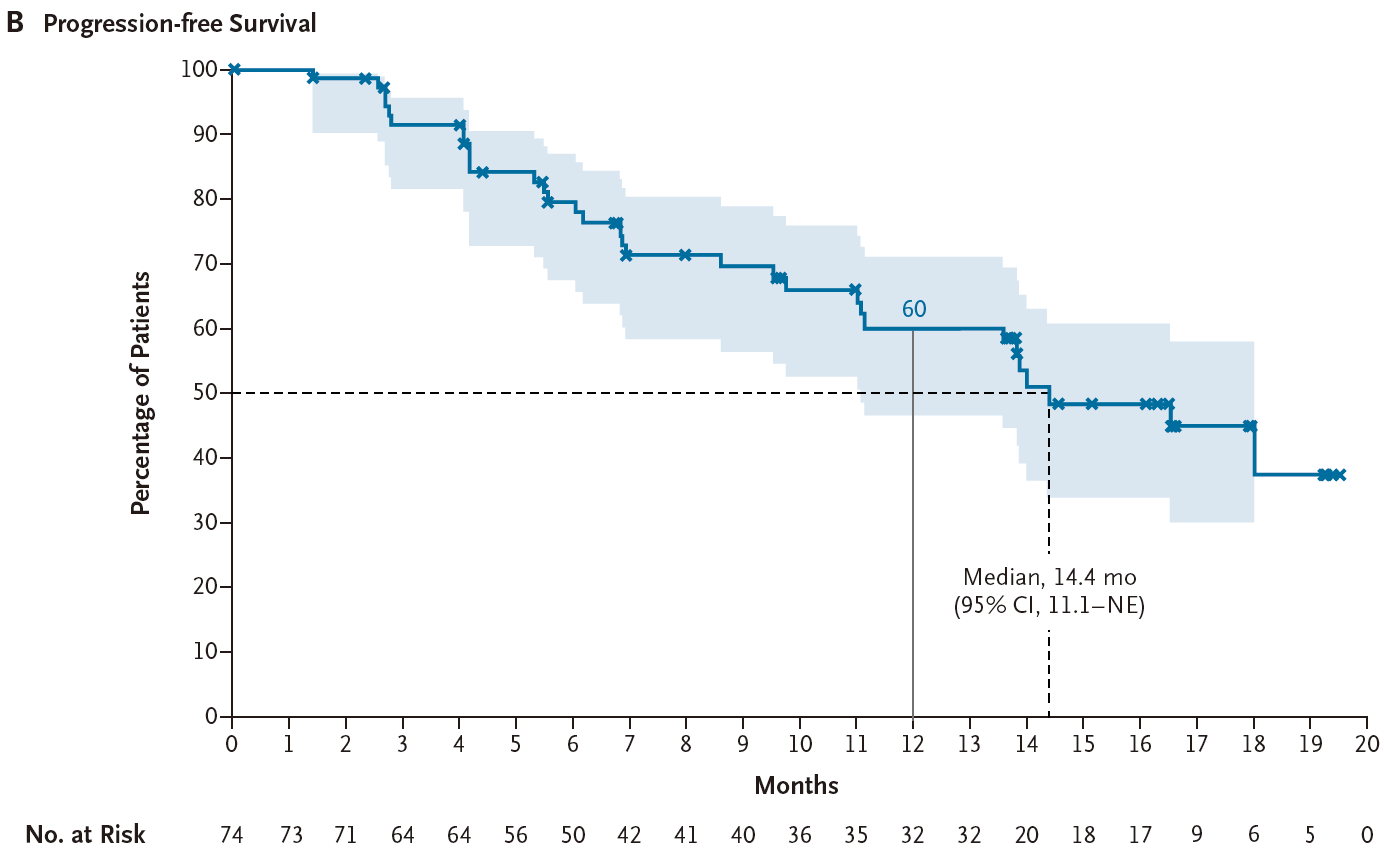
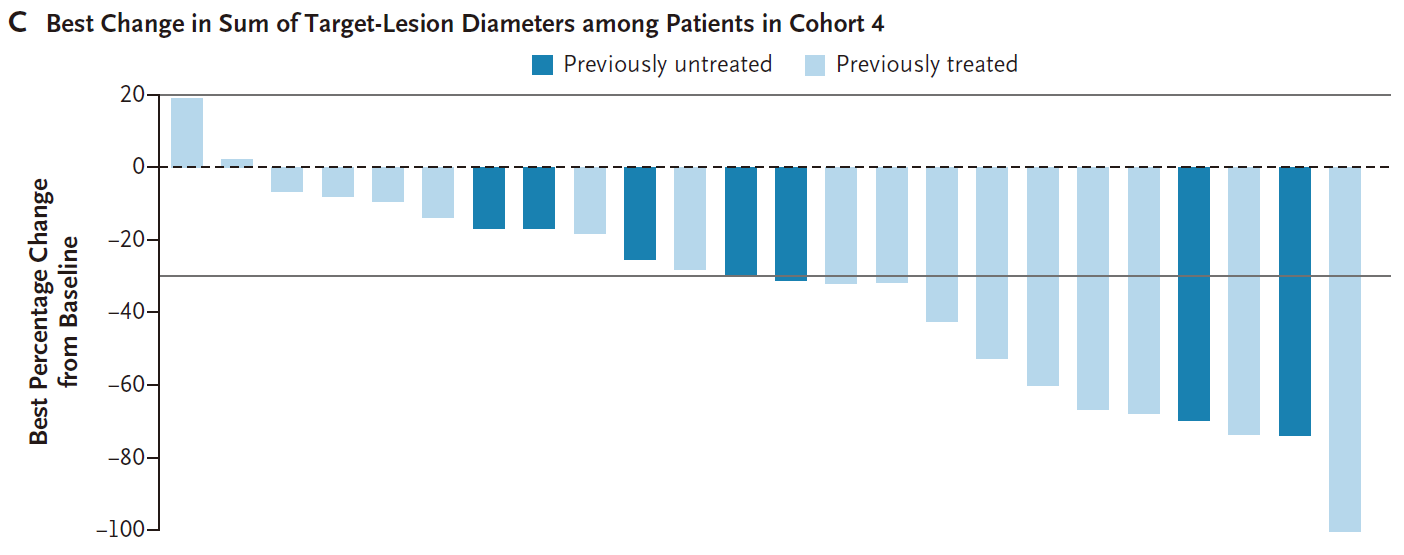
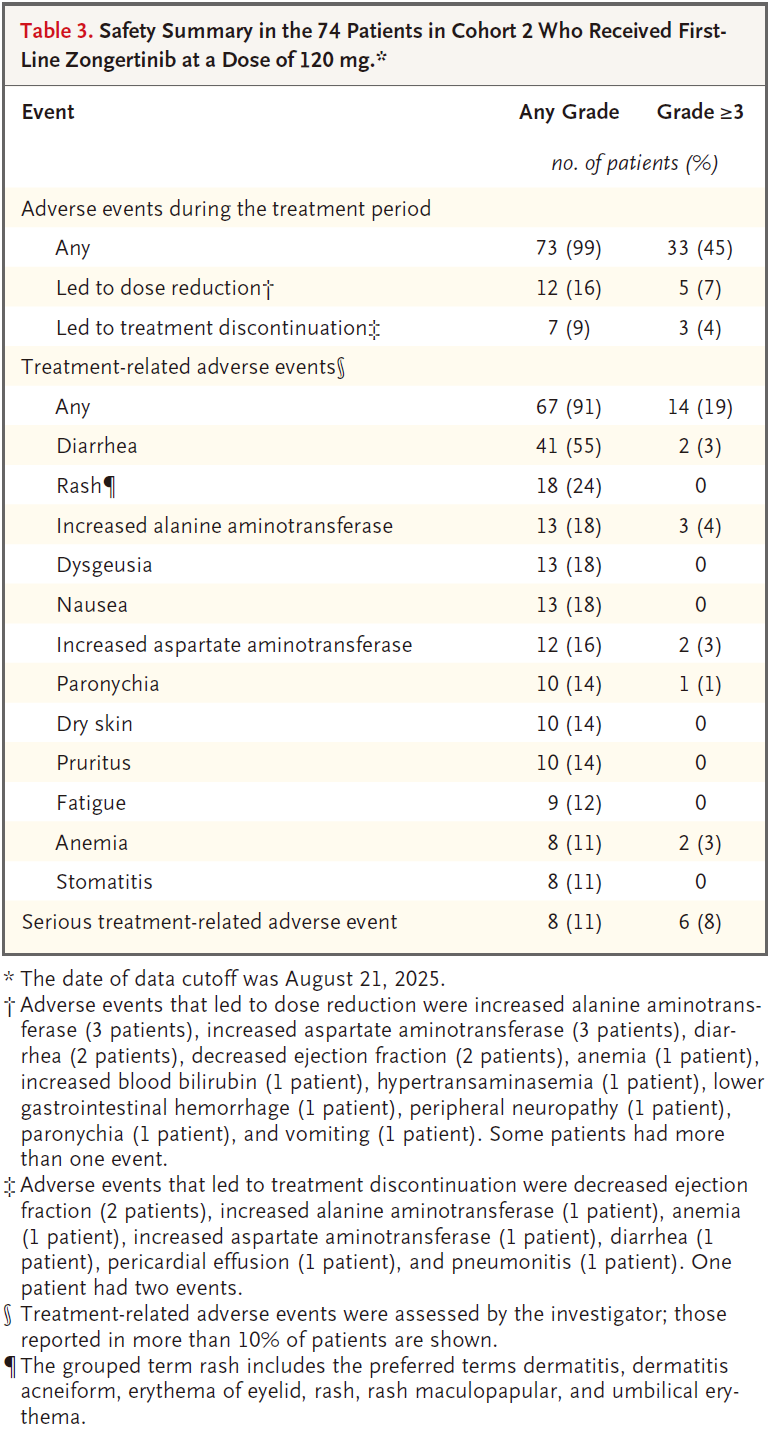
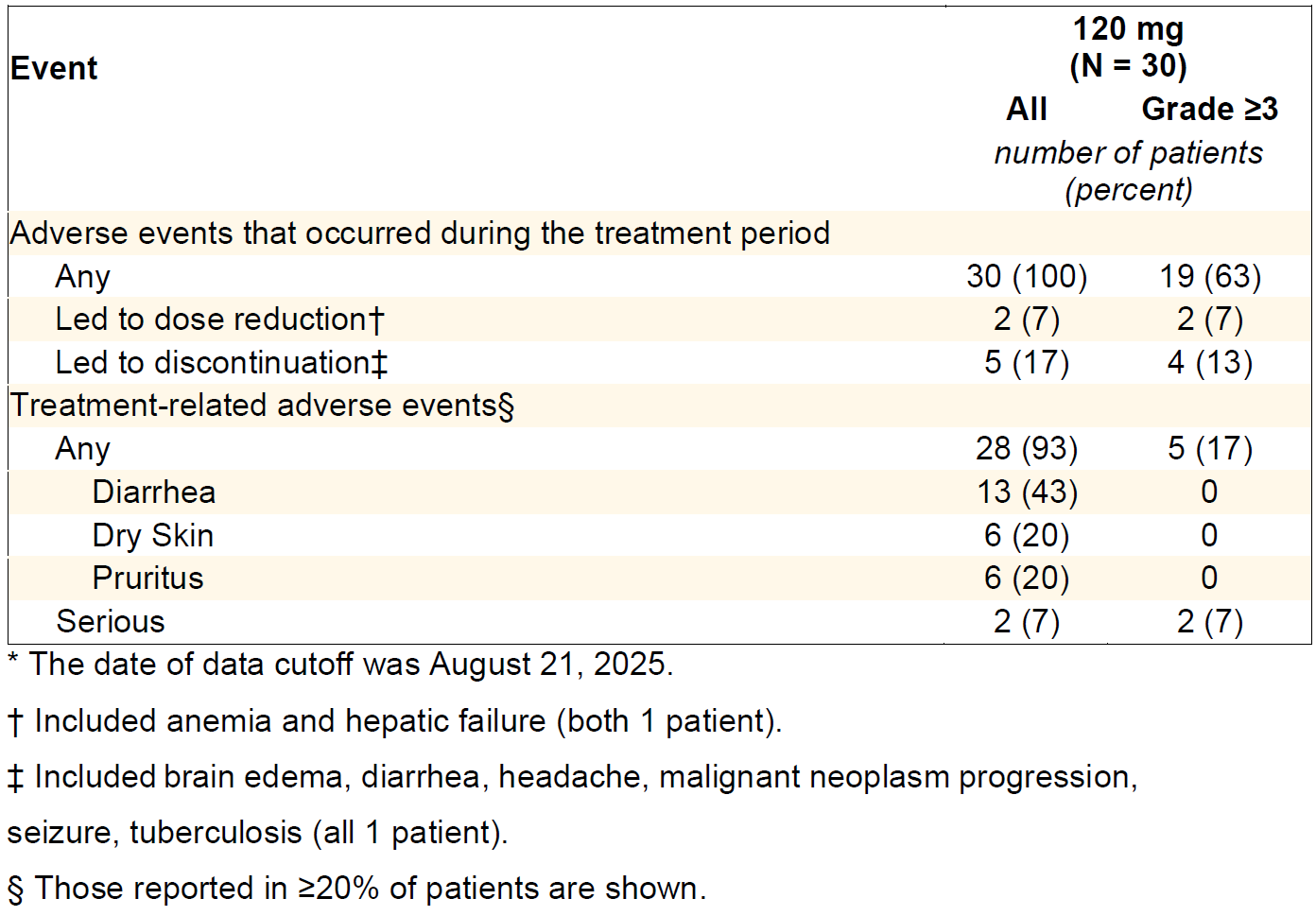
2023年11月7日-2025年8月21日,共有74例未经治疗的患者(队列2)和30例活动性脑转移患者(队列4)接受了剂量为120 mg的宗艾替尼。在剂量选择之前,15例初治患者(队列2)和1例活动性脑转移患者(队列4)接受了剂量为240 mg的宗艾替尼治疗。 队列2和队列4患者流程图 队列2入组患者中位年龄为67岁(范围:35-88岁),其中65岁以上患者占比58%;ECOG PS 1分患者占54%;30%的患者在基线筛查时即存在脑转移(均为稳定或无症状);最常见的突变为A775_G776insYVMA外显子20插入突变,占比68%(50/74)。主要基线特征如下: 队列2基线特征 疗效结果 队列2: 截至2025年8月21日数据截止,经BICR确认的ORR(cORR)为76%(95%CI 65%-84%),其中完全缓解(CR)8例(11%),部分缓解(PR)48例(65%)。在更早的数据截止点(2024年11月29日),cORR为70%(96.98%CI 58%-80%,P<0.001,对比40%的无效假设基准)。 亚组分析中:A775_G776insYVMA突变患者(50例)的ORR达84%。其他突变类型患者(24例)的ORR为58%。基线伴稳定脑转移患者(22例)的ORR为77%,与总人群一致。 队列2疗效数据 靶病灶直径之和的基线变化最佳百分比中位值为−59%(范围:−4%至−100%),提示绝大多数患者均出现明显的肿瘤缩小。中位至缓解时间仅1.4个月(95%CI 1.1-6.9),说明缓解出现迅速。 靶病灶直径之和的最佳变化(队列2) 缓解评估及无进展生存评估(队列2) 在缓解持久性方面,中位缓解持续时间(DOR)为15.2个月(95%CI 9.8个月-不可评估);中位PFS为14.4个月(95%CI 11.1个月-不可评估),DOR和PFS的中位随访时间分别为13.8个月和15.2个月。在数据截止时,治疗仍持续进行的患者占46%。 DOR(队列2) PFS(队列2) 队列4: 在23例既往未接受过脑部放疗的患者中,颅内ORR提升至57%(95%CI 37-74)。 一线治疗患者:在8例一线接受治疗的患者中,颅内ORR为50%。 颅内疗效持久性:中位颅内DOR为6.9个月,中位颅内PFS为8.2个月。 靶病灶直径之和的最佳变化(队列4) 安全性结果 安全性特征与预期一致,其EGFR野生型规避特性在临床上得到了验证,EGFR相关典型毒性的发生率低且严重程度较轻。 队列2: 在74例初治患者中,任意级别不良事件(AE)的发生率为99%(73例),其中≥3级AE占45%(33例)。治疗相关不良事件(TRAE)发生率为91%(67例),≥3级TRAE为19%(14例)。无5级(死亡)治疗相关不良事件发生。 最常见的TRAE为腹泻(55%,其中仅3%为3级)、皮疹(24%,均为1/2级)、ALT升高(18%,4%为3级)、AST升高(16%,3%为3级)等。特别值得关注的是,3级皮疹发生率为0%。 队列2安全性数据 队列4: 安全性特征与总体人群一致,治疗期间任意AE发生率为100%,≥3级AE为63%;TRAE发生率为93%(28例),其中≥3级TRAE为17%(5例)。最常见TRAE为腹泻(43%)、干皮肤(20%)、瘙痒(20%)。1例患者发生4级TRAE(ALT升高),无5级治疗相关死亡。因AE导致剂量下调和停药分别为7%(2例)和17%(5例),停药原因包括脑水肿、腹泻、头痛、疾病进展、癫痫发作和结核病(各1例)。 队列4安全性数据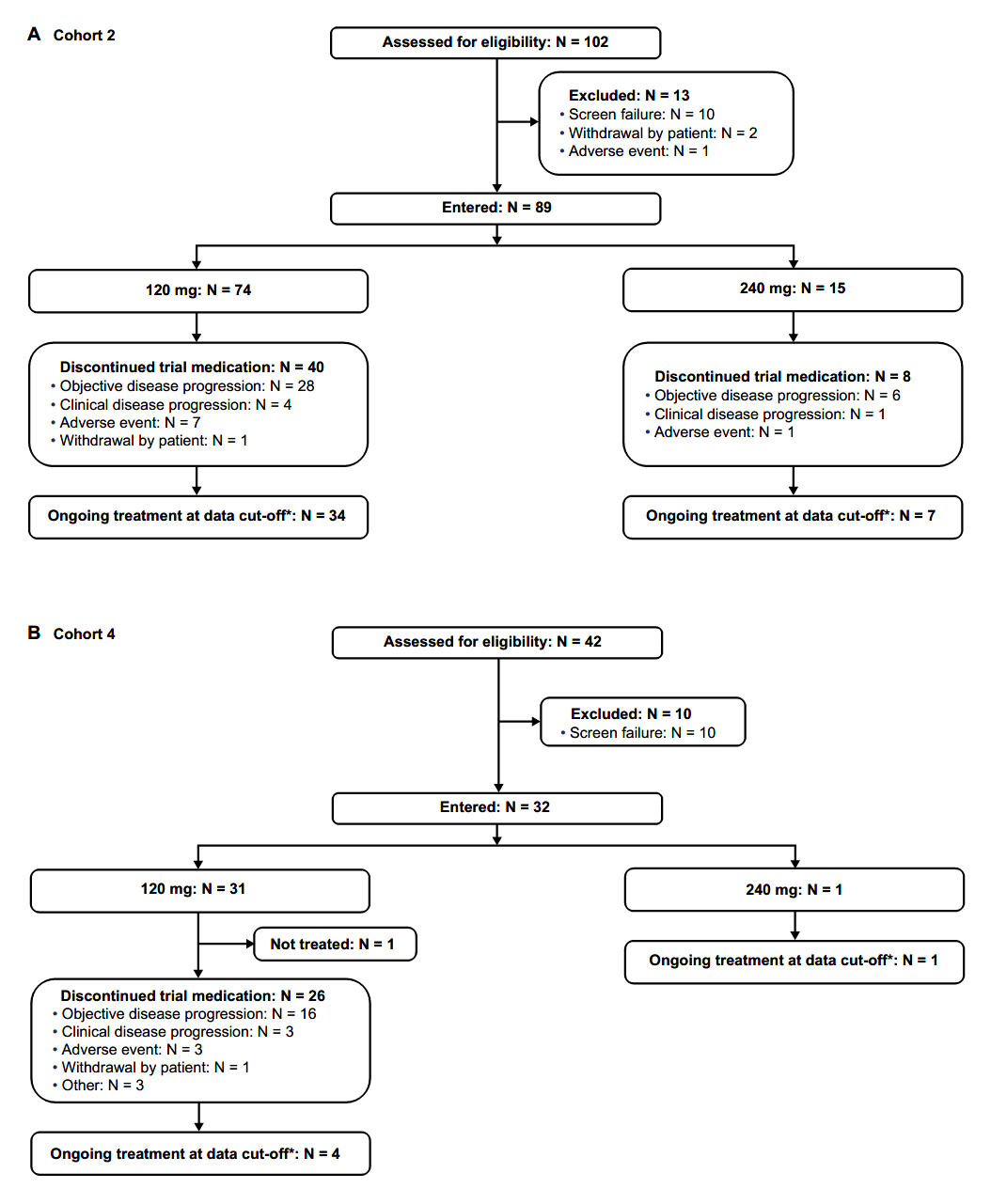
研究结论
综上所述,一线宗艾替尼为HER2突变晚期或转移性NSCLC患者提供了一种有效的靶向治疗新选择,有望取代化疗成为该亚型患者的一线标准方案。期待Beamion LUNG-2研究的III期数据进一步确认其生存获益,推动宗艾替尼最终实现广泛的一线应用。
来源:肿瘤界