引用本文
上海市抗癌协会类器官专业委员会,中国医师协会临床精准医疗专业委员会,中国医药生物技术协会组织生物样本库分会,等. 肿瘤类器官构建通用规范专家共识(2026年版)[J]. 中国癌症杂志, 2026, 36 (3): 299-312.
基金项目:国家自然科学基金(82473011,82273370,U21A20376)。
利益冲突:作者声明无利益冲突。
伦理批件:不需要。
知情同意:不需要。
院士点评

季加孚,中国工程院院士,北京大学博雅讲席教授,北京大学肿瘤研究中心主任,中国医学科学院学术咨询委员会学部委员,国家卫生健康委突出贡献专家,北京学者,美国约翰·霍普金斯大学医学院兼职教授。现任北京大学肿瘤医院胃肠肿瘤中心首席专家,消化系肿瘤整合防治全国重点实验室副主任,国务院特殊津贴专家,政协十三、十四届全国委员会委员,民盟中央常委。兼任北京抗癌协会理事长、中国医疗保健国际交流促进会副会长、中华医学会外科学分会副主任委员、国家肿瘤质控中心胃癌质控专家委员会主任委员等。是国际胃癌学会(IGCA)执委(Council Member)、亚洲外科学会(ASA)常委、英国皇家外科学院院士(FRCS)、英国皇家生物学会会士(FRSB)。主持国家科技支撑计划、国自然重大集成项目等30余项。以第一或通信作者在Lancet、Science、Cell、JAMA、Nature Medicine和PNAS等高水平期刊发表论文400余篇。以第一完成人获国家科技进步二等奖1项、省部级一等奖4项,获光华工程科技奖、何梁何利科技进步奖、吴阶平·保罗杨森医学医药奖、中源协和生命医学成就奖等科技奖项。
季加孚院士:从临床角度看,肿瘤类器官的价值,不只是把模型培养出来,更重要的是它是否可信、稳定,能否真正服务于药物筛选和精准诊疗。长期以来,不同中心在样本处理、培养体系、质量控制和管理流程上的差异,影响了类器官结果的可重复性和临床应用价值。《肿瘤类器官构建通用规范专家共识(2026年版)》的重要意义,就在于围绕这些关键问题提出了全流程规范。特别是对三级质控体系的强调,把日常培养监测、病理表型验证和遗传保真度评估有机结合起来,有助于提高模型的可信度和可比性。同时,这份共识也充分考虑了活检、穿刺和体液等低起始量临床样本的建模需求,并把实验室质量管理和信息追溯纳入规范框架,这对推动类器官从科研模型走向临床转化非常关键。总体而言,这份共识立足临床需求,强化了肿瘤类器官从“能建模”走向“可信、可比、可用”的关键基础。未来随着更多临床一致性验证、前瞻性研究和特异癌种规范的完善,类器官有望在个体化药敏检测、新药研发和精准诊疗中发挥更大价值。

曾木圣,研究员,博士研究生导师,中国科学院院士。现任中山大学肿瘤防治中心副主任/副院长、“国际EB病毒及相关疾病研究协会”主席、广东省肿瘤免疫与疫苗工程技术研究中心主任及2024 Gordon Research Conference鼻咽癌国际会议主席。入选长江学者特聘教授、“南粤百杰”和第九届国家卫生健康突出贡献中青年专家等。获国家杰出青年科学基金、国家重点研发计划2项及多项国自然重点项目。长期专注于EB病毒致癌机制与靶向干预研究,首次发现EB病毒感染上皮细胞特异性受体,以及B细胞和上皮细胞通用受体,提出多受体序贯协同介导EB病毒跨细胞感染新理论,建立EB病毒创新疫苗体系,研发出多个候选疫苗并成功转让给国内龙头企业。以通信或共同通信作者在Nature(2)、Nat Microbiol(2)、Cell Host & Microbe、Cell Res、Cancer Cell、Lancet DH、PNAS、J Clin Invest等国际主流期刊发表论文100多篇。以第一完成人分别获国家自然科学二等奖(2023)、高等学校科学研究优秀成果奖(2022)、广东省自然科学奖(2018和2023)和中国抗癌协会科技奖一等奖。
曾木圣院士:近年来,肿瘤类器官技术发展迅速,已成为连接基础研究、新药研发与精准诊疗的核心桥梁。然而,国内各机构在类器官构建全周期中缺乏统一规范,操作流程差异显著,导致模型质量参差不齐、数据可比性不足,严重制约了技术向临床的转化。在此关键节点,《肿瘤类器官构建通用规范专家共识(2026年版)》正式发布,具有里程碑式意义。共识系统构建了从样本采集、培养扩增到分级质控、全流程管理的完整规范,突出全流程质控理念和模型保真性验证,确保模型可靠、结果可信,为一线工作者提供了清晰指引,也为多中心协作与成果转化奠定了统一基础。这份共识推动我国肿瘤类器官领域从“建得成”迈向“建得规范、建得可靠”的高质量发展阶段。期待其在实践中不断完善,行业同仁携手,让技术在机制研究、新药创制与精准诊疗中发挥更大价值,惠及更多患者。
第一作者简介

王琦,复旦大学附属肿瘤医院病理科生物样本库类器官平台负责人。以第一作者在Advanced Science、Cell Death & Disease、Biomarker Research等SCI收录期刊上发表论文5篇,申请国家发明专利1项,参编《类器官生物学》。
通信作者简介

许蜜蝶,副主任医师,副研究员,硕士研究生导师,复旦大学附属肿瘤医院病理科生物样本库负责人,上海恶性肿瘤生物样本库专业技术服务平台执行主任。上海市青年东方英才,国家重点研发计划子课题负责人。长期致力于生物样本标准化质量技术体系建设、以及常见消化系统肿瘤的精准病理诊断与分型等应用基础研究。主持国家“工程科学与综合交叉”重点专项子课题等国家级、省部级项目十余项。现任联合国工业发展组织首位特聘生物样本库/ISO 20387技术专家,全国生物样本标准化技术委员会(SAC/TC559)第三届委员,中国医药生物技术协会组织生物样本库分会青年工作组组长,中国研究型医院学会临床数据与样本资源库专业委员会常委,中国抗癌协会类器官与器官芯片专业委员会首届委员,中国细胞生物学学会类器官研究与应用工作委员会首届委员,中国医药生物技术协会类器官技术临床应用分会第一届委员会委员,上海市抗癌协会类器官专业委员会首届常委,Biomarker Research杂志编辑兼特刊“Multi-omics and Biomarkers”组稿编辑等。在Nature Metabolism、Science Advances、Nature Communications、Advanced Science、Journal of the National Cancer Center等SCI收录期刊上发表论著30多篇,申请国家发明专利11项。
作者解读
▲ 许蜜蝶 医师
肿瘤类器官构建通用规范专家共识(2026年版)
上海市抗癌协会类器官专业委员会,中国医师协会临床精准医疗专业委员会,中国医药生物技术协会组织生物样本库分会,中国研究型医院学会临床数据与样本资源库专业委员会,中国抗癌协会类器官与器官芯片专业委员会,中国细胞生物学学会类器官研究与应用工作委员会,中国医药生物技术协会类器官技术临床应用分会
[摘要] 类器官技术通过三维体外培养高度模拟人体组织器官的结构和功能特征,在疾病模型构建、精准医疗和药物研发等领域具有重要价值。类器官技术在2019年被The New England Journal of Medicine评为优秀的临床前疾病模型,随着研究的不断深入,肿瘤类器官已广泛覆盖多种实体瘤。然而,目前中国在肿瘤类器官的样本采集、培养体系、质量控制及合规治理等关键环节尚缺乏统一的技术规范和共识框架,限制了研究成果的可重复性和临床转化应用。为此,本共识由上海市抗癌协会类器官专业委员会、中国医师协会临床精准医疗专业委员会等组织,基于广泛的国内外文献检索、证据分级及专家审议形成,首次系统性地提出肿瘤类器官构建技术的全流程通用规范,涵盖从样本采集、处理,到类器官培养、传代、冻存、复苏及质量控制全流程。希望通过本共识,能够为从事肿瘤类器官研究的科研人员和临床工作者提供科学的技术指导框架,以提高模型的保真度和可靠性,促进数据共享和横向比较,加速类器官技术在肿瘤精准诊疗中的规范化落地。本共识将根据未来开展的基于类器官的各项研究成果和实践经验定期更新。
[关键词] 类器官;肿瘤;通用规范;全流程;共识
[Abstract] Organoid technology, which enables three-dimensional in vitro culture to closely recapitulate key structural and functional features of human tissues and organs, has significant value in disease modeling, precision medicine, and drug discovery and development. With continued advances in organoid research, tumor organoids have been established for a wide range of solid tumors, and the technology was highlighted by The New England Journal of Medicine in 2019 as an excellent preclinical disease model. However, in China, unified technical guidelines and a consensus framework are still lacking for critical aspects of tumor organoid practice, including specimen collection, culture systems, quality control, and compliance governance. This has limited the reproducibility of research findings and their clinical translation. To address these gaps, this consensus was developed by the Organoid Professional Committee of the Shanghai Anticancer Association and Clinical Precision Medicine Professional Committee of Chinese Medical Doctor Association, among others, based on extensive searches of domestic and international literature, evidence grading, and expert review. For the first time, it systematically proposes a full-process general framework for tumor organoid construction, covering specimen collection and processing, organoid culture and passaging, cryopreservation and recovery, and quality control throughout the entire workflow. This consensus is intended to provide a scientific and practical technical guidance framework for researchers and clinicians engaged in tumor organoid studies, improve model fidelity and reliability, facilitate data sharing and cross-study comparability, and accelerate the standardized implementation of organoid technology in precision oncology. The consensus will be updated periodically in accordance with emerging evidence and accumulated practical experience from organoid-based research.
[Key words] Organoids; Tumor; General guidelines; End-to-end workflow; Consensus
《肿瘤类器官构建通用规范专家共识(2026年版)》专家组
总顾问
王红阳|海军军医大学东方肝胆外科医院细胞信号转导研究室/国家肝癌科学中心
季加孚|北京大学肿瘤医院胃肠肿瘤中心
曾木圣|中山大学肿瘤防治中心实验研究部
杜 祥|复旦大学附属肿瘤医院病理科
执笔专家
许蜜蝶|复旦大学附属肿瘤医院病理科
钟 茜|中山大学肿瘤防治中心检验科
陈 磊|海军军医大学东方肝胆外科医院细胞信号转导研究室/国家肝癌科学中心
张连海|北京大学肿瘤医院生物样本库
王 琦|复旦大学附属肿瘤医院病理科
龙子雯|复旦大学附属肿瘤医院胃外科
编写秘书
何爱娜|上海市第六人民医院肿瘤内科
江婧婧|雄安生命科学大数据中心及转化应用示范基地(筹)
共识专家组成员(按姓名汉语拼音排序)
艾晓妮|北京大学药学院
白 龙|上海大学转化医学研究院
卜鹏程|中国科学院生物物理研究所
陈策实|昆明医科大学生物医学工程研究院
陈 飞|复旦大学附属肿瘤医院肿瘤研究所
陈曲波|广东省中医院生物资源中心
陈荪睿|湖北江夏实验室
陈玥尧|上海交通大学医学院附属第九人民医院生物样本库
付彩云|浙江理工大学生命科学与医药学院
高 栋|中国科学院分子细胞科学卓越创新中心
郜恒骏|生物芯片上海国家工程研究中心
郭 卫|北京大学人民医院骨肿瘤科
贺巾帼|生物芯片上海国家工程研究中心
胡 欣|复旦大学附属肿瘤医院精准肿瘤中心
贾卫华|中山大学肿瘤防治中心生物资源库
江一舟|复旦大学附属肿瘤医院乳腺外科
吉顺荣|复旦大学附属肿瘤医院胰腺外科
康晓楠|上海交通大学医学院附属仁济医院生物资源中心
李 飞|中国科学院上海营养与健康研究所
李建明|南昌大学第一附属医院病理科
李 颖|大连医科大学附属第一医院干细胞临床研究机构
刘小珍|浙江省人民医院转化医学中心
刘 妍|中国人民解放军总医院第五医学中心感染病医学部/传染和感染性疾病国家临床医学研究中心
梁 玮|上海临床研究中心生物样本库
马骁驰|大连医科大学药学院
满秋红|同济大学医学院脑功能与人工智能转化研究所
苗一非|中国科学院动物研究所
苗智峰|中国医科大学附属第一医院肿瘤外科
聂勇战|空军军医大学西京医院消化系统肿瘤整合防治全国重点实验室
孔祥谦|中国科学院广州生物医药与健康研究院
彭 飞|大连医科大学肿瘤干细胞研究院
盛伟琪|复旦大学附属肿瘤医院病理科
施 思|复旦大学附属肿瘤医院胰腺外科
时 雨|陆军军医大学西南医院病理科
孙 涛|南开大学药学院
王桂华|华中科技大学同济医学院附属同济医院胃肠外科
王勤英|复旦大学附属肿瘤医院大肠外科
王 昕|中国医学科学院肿瘤医院乳腺外科
汪 源|四川大学华西医院生物治疗研究中心
王跃祥|中国科学院上海营养与健康研究所
王振宁|中国医科大学附属第一医院胃肠肿瘤外科
吴来阳|清华大学第一附属医院临床研究质量促进中心
向冬喜|上海市肿瘤研究所
熊利泽|同济大学医学院脑功能与人工智能转化研究所
杨庆诚|上海市第六人民医院骨科
杨庆凯|大连医科大学肿瘤干细胞研究院
杨亚军|复旦大学生命科学学院
尹 荣|江苏省肿瘤医院胸外科
于颖彦|上海交通大学医学院附属瑞金医院普外科
徐彦辉|复旦大学附属肿瘤医院肿瘤研究所
许 川|四川省人民医院肿瘤中心
叶棋浓|军事科学院军事医学研究院
尹鹏滨|中国人民解放军总医院骨科医学部
应建明|中国医学科学院肿瘤医院病理科
郑小辉|中山大学肿瘤防治中心生物资源库
张小燕|生物芯片上海国家工程研究中心
张志谦|北京大学肿瘤医院肿瘤研究所
张 勇|生物芯片上海国家工程研究中心
周 婕|香港大学李嘉诚医学院微生物学系
周兆才|复旦大学生命科学学院
朱 鹤|上海市肿瘤研究所
癌症是全球性的公共健康问题[1],尽管过去几十年来癌症预防、诊断及治疗取得了重要进展,但由于其高度的异质性、复杂的分子病理学机制及患者个体差异,如何精准高效地开展个体化治疗仍是当前肿瘤防治领域亟待解决的难题之一。有效的癌症临床治疗方案形成,需要高度可靠且能够真实反映患者肿瘤生物学特征的临床前研究模型[2]。然而,长期以来广泛使用的传统癌症研究模型,如细胞系和患者来源的异种肿瘤移植(patient-derived tumor xenograft,PDX)模型,虽然在揭示癌症发病机制和药物开发方面发挥了重要作用,但仍存在诸多难以克服的局限性。传统的二维细胞系缺乏体内生长的三维空间和肿瘤微环境,无法再现原发肿瘤的遗传异质性;PDX模型成瘤率有限、构建耗时且昂贵,肿瘤在小鼠体内可能经历物种特异性的进化,难以真实模拟患者的疾病过程[3]。相比之下,新兴的类器官技术为建立更接近体内病理生理学状态的肿瘤模型提供了新途径[4]。类器官通常由患者组织中的成体干细胞或诱导多能干细胞体外分化形成,能够长期传代并保留原组织的组织学结构、遗传特征和功能表型[5]。2017年,类器官技术被Nature Methods评为年度生命科学技术,也作为关键技术被列入中国“十四五”期间的多项国家重点研发计划,显示出巨大的发展潜力。类器官模型已广泛用于多种实体瘤的研究,在肿瘤发生机制、药物筛选和个体化治疗方面展现出巨大潜力[6]。
目前国内在类器官构建、鉴定及质量控制方面尚无统一规范,各实验室操作差异较大,导致模型质量参差不齐,影响研究结果的可靠性和多中心数据共享。为提高肿瘤类器官模型的可靠性和可重复性,促进基础研究成果向临床转化,制定人源肿瘤类器官构建技术通用规范具有重要意义。本共识重点涵盖“肿瘤类器官构建-鉴定-质量控制”全过程的通用最低要求和关键控制点,强调过程记录和可追溯性,并与聚焦类器官药敏检测临床应用和平台质控的相关国内专家共识,以及国际上正在推进的类器官规范化、标准化工作有所侧重和区别。本共识基于最新研究进展和已有相关标准,凝练多学科专家经验,经过共同讨论和修改,采用循证医学证据分级系统在国内首次形成意见草案。为确保共识制定的科学性、透明度和规范性,本共识项目已在国际实践指南注册与透明化平台(Practice guideline REgistration for transPAREncy,PREPARE)上完成注册,注册号为PREPARE-2026CN150。
1 共识制定方法
本共识严格遵循循证医学方法进行制定,具体制定流程见图1。经多轮专家论证与审议,最终形成19条核心推荐意见。
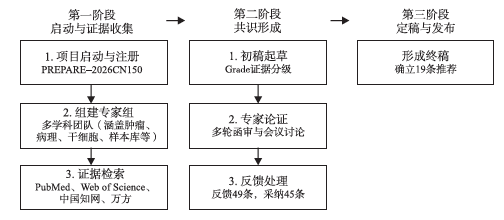
图1 肿瘤类器官构建通用规范专家共识制定流程图
Fig. 1 Flowchart of the development process for the expert consensus on general guidelines for tumor organoid construction
1.1 共识专家组构成
本共识由上海市抗癌协会类器官专业委员会、中国医师协会临床精准医疗专业委员会、中国医药生物技术协会组织生物样本库分会、中国研究型医院学会临床数据与样本资源库专业委员会、中国抗癌协会类器官与器官芯片专业委员会、中国细胞生物学学会类器官研究与应用工作委员会、中国医药生物技术协会类器官技术临床应用分会等多家学术机构联合发起。共计73位专家参与共识编制,其中,总顾问4位,执笔专家6位,编写秘书2位,共识专家组成员61位。专家来自全国15个省级行政区的40余家单位。学科背景涵盖肿瘤学、病理学、细胞生物学、生物样本库及伦理学等多学科领域。
1.2 文献检索方法
共识专家组检索了PubMed、Web of Science、中国知网、万方数据库等国内外数据库。检索关键词包括“Organoid”“Tumor”“Cancer”“Biobank”“Culture”“Quality Control”“类器官”“肿瘤”“生物样本库”等。检索时间截至2025年10月。主要纳入关于肿瘤类器官构建、培养、鉴定及质控的高质量原始研究、综述及相关规范性文献,排除重复发表、与本共识主题无关、仅涉及非肿瘤类器官且无直接参考价值、缺乏关键方法学信息或参考价值有限的文献。经筛选后,最终纳入文献49篇。
1.3 共识形成的方法
本共识采用专家会议法与多轮函审相结合的方式。初稿由执笔专家组基于文献证据起草,随后通过线上/线下专家会议进行研讨,广泛征求意见并进行修改,最终经全体专家组成员投票通过。
1.4 证据分级方法
本共识的证据等级和推荐级别标准参照GRADE分级体系的基本框架,并基于肿瘤类器官构建作为实验室技术的特殊属性进行适用性修订。证据等级分为A级、B级和C级,推荐级别分为1级和2级(表1)。

1.5 共识的使用人群
本共识适用于从事肿瘤类器官研究的科研机构、医疗机构及第三方医学检验实验室的科研人员、临床医师及技术人员。
1.6 共识的传播、实施及更新
本共识发表后,将通过学术会议及专业培训进行推广。专家组将根据国内外类器官领域的最新研究成果和实践经验,计划每1~2年对共识进行更新。
1.7 共识形成结果
共识制定过程共收集到49条反馈意见,经专家组审议讨论后采纳45条,依据这45条反馈意见对草案进行修订。最终形成了涵盖全流程的19条推荐意见,涉及合规性、样本处理、培养及质控等关键环节。
2 推荐意见陈述
2.1 合规性和伦理
开展涉及人体来源组织的类器官技术活动,必须严格遵守国家相关法律法规和伦理指南的要求,确保研究合规合法、受试者权益得到保护。具体要求为:① 遵守人类遗传资源管理相关规定,包括《中华人民共和国生物安全法》《中华人民共和国人类遗传资源管理条例》;② 严格进行伦理学审查,依据《人类生物样本保藏伦理要求》(GB/T 38736-2020)等规定,应建立知情同意制度;③ 注意患者个人信息保护,根据《中华人民共和国个人信息保护法》,实验室对获取的患者临床信息和样本数据,应采取匿名化或去识别化处理,仅保留与研究相关的数据,并安全存储。
推荐意见1:所有涉及人类遗传资源的类器官研究应依法依规履行审批或备案,并在研究开展前取得受试者的知情同意和伦理委员会批准;同时严格保护患者隐私和数据安全(A级证据,1级推荐,《中华人民共和国生物安全法》《中华人民共和国人类遗传资源管理条例》《人类遗传资源管理条例实施细则》《涉及人的生物医学研究伦理审查办法》《中华人民共和国个人信息保护法》)。
2.2 样本采集和接收
患者来源肿瘤类器官(patient-derived tumor organoids,PDTO)构建成功与否,在很大程度上取决于初始样本的质量,而样本质量又受样本采集和运输过程中各类分析前变量的影响。本共识以建立肿瘤类器官构建的通用技术要求和质量控制体系框架为目标,适用于常见实体瘤,并兼顾血液系统肿瘤相关样本的规范化处理。组织来源多样性—从手术切除标本[7]、内镜或穿刺活检组织,到细针穿刺抽吸术(fine-needle aspiration,FNA)样本[8],亦包括来源于胸/腹水及脑脊液等恶性积液的肿瘤细胞[9],以及外周血循环肿瘤细胞(circulating tumor cell,CTC)衍生样本[10]。上述组织样本类型直接决定了可用于培养的细胞数量和质量,从而影响培养的成功率。组织的获取应尽量选择肿瘤实体部位且避免取样坏死或纤维化区域[11]。通常,能够提供充足组织(体积大于5 mm3)的手术切除标本具有最高的培养成功率,而较小的活检样本由于起始材料有限,则具有较大的技术挑战。例如,FNA作为一种微创技术,虽然扩大了可获取样本的患者范围(如转移性病灶),但其细胞获得量低,需要通过优化方案(如合并多次穿刺样本)来提高建系成功率[8]。对于体液来源样本及CTC等低起始量样本,应尽快完成接收和处理,并在进入三维培养前进行细胞富集/去除杂细胞等必要关键步骤,以提高建系成功率和稳定性。
影响细胞活力的一个关键因素是冷缺血时间(cold ischemia time,CIT),即组织从血供中断到开始处理的时间。尽管关于CIT对类器官成功率的直接研究仍在不断积累,但大量来自器官移植领域的证据表明,延长CIT会显著增加原发性无功能和细胞死亡的风险,这一原理同样适用于类器官起始所需的敏感干/祖细胞群[12]。因此,最大程度地缩短CIT至关重要。目前已发表的文献[13-15]都一致推荐,组织一旦离体,应立即置于无菌、预冷的运输保存液中,并在整个运输过程中维持在2~8 ℃(冰上)的环境中。保存液通常为含有抗生素的基础培养基,以防止微生物污染;必要时可短期加入Rho激酶抑制剂Y-27632,以减少失巢凋亡并提高细胞存活率[7]。虽有研究[16]表明,在严格低温条件下,离体组织冷藏72 h后仍可成功培育出类器官。为保证细胞活性,建议手术标本在24 h内、活检标本在更短的时间内(12 h)送达实验室进行处理,超过该范围按高风险样本处理并预先评估细胞活性。
推荐意见2:应建立标准化的类器官样本采集、运输和接收流程,确保样本及时于低温条件下送达并登记入库。所有送达样本进入实验室后应立即录入信息管理系统,赋予唯一可追溯编号,并至少记录样本类型、采集时间、运输条件、CIT(组织样本)或采集至处理时间(体液/CTC样本)等关键信息;超出推荐时限者应标记为高风险样本并记录处置措施(A级证据,1级推荐,GB/T 37864-2019)。
推荐意见3:手术切除组织应选取无明显坏死的区域且体积不小于5 mm3,离体后立即置于含组织保护液的无菌容器中,于2~8 ℃的环境下运输;内镜/穿刺活检及FNA样本宜在无临床风险的前提下多点取材(≥3条、长度≥1 cm的组织条)并低温快速送达实验室。建议手术标本≤24 h、活检/FNA标本≤12 h内完成送达和处理;超过该范围按高风险样本处理,继续构建前需评估细胞活性(B级证据,1级推荐)。
推荐意见4:恶性胸/腹水、脑脊液及外周血CTC等体液/液体活检来源样本应尽快接收处理(全程低温运输为宜),进入培养前可根据需要进行离心/密度梯度分离等细胞富集并去除杂细胞,以提高建系成功率和稳定性(B级证据,2级推荐)。
2.3 样本处理和类器官原代培养
组织样本送达实验室后应立即进行预处理,以获取用于类器官培育的细胞悬液。此过程通常包括机械剪切和酶解消化两个步骤。对于恶性胸/腹水、脑脊液等体液来源样本及外周血CTC样本,一般无需机械剪切或组织酶解,处理重点为尽快接收并进行离心/密度梯度分离等富集步骤,必要时可通过红细胞裂解并去除杂细胞后获得肿瘤细胞沉淀。而对于实体组织样本,送达实验室后应立即进行预处理,以获取用于类器官培育的细胞悬液。通过灭菌眼科剪或手术刀片以机械方式将组织剪切成1 mm3或更小的小块,以增大与消化酶的接触面积。后续的酶解消化是关键环节,其方案因组织来源和肿瘤类型的不同而存在显著差异[7]。常用的酶混合物包含用于分解基质的胶原酶(Ⅰ、Ⅱ或Ⅳ型),并与分散酶(dispase)、温和的胰蛋白酶替代物(如TrypLETM)或用于防止DNA释放导致细胞凝集的DNase Ⅰ联用[15,17]。在部分基质/糖胺聚糖较丰富的组织中,可在胶原酶基础上联用透明质酸酶(hyaluronidase)以提高解离效率[18-19];常见组合方案包括胶原酶+透明质酸酶(±DNase Ⅰ),胶原酶(Ⅱ/Ⅳ)+dispase(±DNase Ⅰ),胶原酶(Ⅱ/Ⅳ)+透明质酸酶+dispase等(表2)。消化过程的温度和时间必须经过验证和优化,在有效解离组织的同时,最大限度地保护细胞表面蛋白和维持细胞整体活力,这是成功启动培养的先决条件。消化结束后通过70~100 µm的细胞滤网筛选以获得细胞簇和单细胞的混悬液,需对细胞活力和细胞数量进行评估。细胞活力可采用锥虫蓝法或荧光染料双染等方法评估,并记录活细胞数。存活率≥70%可直接接种;存活率<70%不建议直接接种,宜先去除死细胞/碎片(如密度梯度分离)并复测后再培养;若存活率<50%或活细胞数过少(如细胞数量<1×104个),则视为高风险样本,一般不建议继续尝试培养(除非可通过补采/合并提高活细胞量)。针对细胞总数极少的样本(如穿刺标本),可通过增加穿刺样本量(对同一病灶进行≥3次的穿刺),合并样本以提高细胞总量;同时可通过提高类器官接种密度、调整培养基及基质胶等方式优化培养,避免样本损失。

目前常用的接种方法主要有两种:一是基质胶滴培养法(也是最常用的方法)[13],即将细胞与三维基质支架(如Matrigel基质胶)混合作为小胶滴进行接种;二是悬浮培养法[20-21],即在培养基中加入低浓度基质使细胞以悬浮球形式培养。采用胶滴法时,按照细胞悬液体积∶基质胶=3∶7的比例混匀后种胶,避免产生气泡。将培养板置于37 ℃的培养箱中静置至胶滴成形并固化至胶滴不再流动(固化时间与基质胶体系及胶滴体积有关,必要时可适当延长,以所用基质胶说明书/预实验为准)。同时应记录基质胶的品牌、货号和批号,同一研究宜固定批号。采用悬浮培养法时,将类器官直接悬于含有低浓度(通常为1%~5%)基质胶的培养基中,并在轨道摇床上以60~80 r/min的速率进行持续、温和的水平振荡培养,这种动态环境能有效地防止类器官沉降、聚集和贴壁,同时改善营养和氧气的交换效率,从而实现高密度的扩增。
肿瘤类器官的培养基建议采用“基础培养基+核心添加组分+癌种特异性可调模块”的框架进行标准化管理。基础培养基可选Advanced DMEM/F12,并常规补充GlutaMAX、HEPES、N2、B27、N-acetylcysteine等以维持细胞稳态和抗氧化环境;核心生长因子通常至少包含表皮生长因子(epidermal growth factor,EGF)、Noggin及R-spondin1,必要时可补充Wnt3a以满足部分组织/肿瘤对Wnt信号的更高需求。小分子调控剂可在核心框架上按需加入(如TGF-β通路抑制剂A83-01、p38抑制剂SB202190、烟酰胺、胃泌素、PGE2等),并可在原代起始或复苏早期短期加入ROCK抑制剂(如Y-27632)以降低失巢凋亡并提高存活率。不同癌种对信号转导通路的需求不同,可根据肿瘤驱动通路对营养因子依赖性的差异进行短期选择性培养初筛。例如,消化道肿瘤通常高度依赖Wnt3a,而部分妇科肿瘤则需补充Neuregulin 1。此外,为抑制正常上皮过度生长,需精准调控转化生长因子β(transforming growth factor-β,TGF-β)抑制剂的使用或在特定阶段撤除Wnt。常见实体瘤的关键特异性因子差异见表2。需要注意的是选择性培养可能带来克隆选择偏倚,应在记录中注明,并通过病理学检查和(或)分子质控最终确认肿瘤属性后再进入应用。
无论采用哪种方法,接种密度都需要根据细胞类型和培养器皿表面积进行优化。一般可参考:在24孔板中每孔细胞约5×104~1×105个;若使用其他规格培养板则可按表面积比例换算。接种后初始培养阶段(原代培养)的环境应保持恒定:温度37 ℃±0.5 ℃,CO2体积分数为5%±0.2%。为降低污染风险,抗生素/抗真菌药建议分阶段规范使用:样本运输接收和清洗阶段可短期加入抗感染成分;对高风险样本(如消化道来源、坏死/感染风险高、体液样本等)可在原代培养早期短期过渡性使用,并在污染风险降低后逐步停用;长期培养阶段不建议常规依赖抗生素/抗真菌药,并应配套开展定期支原体检测。通常在接种后72 h内即可观察到部分细胞聚集并开始自组装形成三维结构,此时应进行首次培养基更换[29]。此后每隔2~3 d更换1次培养基,每次换液的体积宜超过培养孔总容积的一半。定期换液可及时补充营养、清除代谢废物,维持类器官良好的生长环境。
一般来说,不同来源组织的类器官生长速度有所差异[7]。多数情况下,培养7 d左右即可在显微镜下见到类器官结构形成,培养约2~3周后类器官生长进入平台期并可考虑传代扩增[13]。稳定生长的类器官形态多种多样,包括囊状、实心致密状、低黏附性球状等,不同组织、不同患者的类器官形态可能存在个体化差异[14-15,17]。培养过程中,研究人员应密切观察并记录类器官形成的时间和形态变化,为后续优化培养条件和判断模型成熟度提供依据。
推荐意见5:及时且规范地对新鲜组织进行预冷清洗、机械切割和适度酶解,是获取高活性细胞悬液的关键。消化后细胞活力宜达到70%以上方可直接用于类器官培养;如果细胞数量过少(细胞数<1×104个)或活性过低(存活率<50%),应视为高风险样本,可在充分评估后通过调整解离方法、提高类器官接种密度、优化培养基成分及基质胶等方式进行优化尝试,并结合复测结果决定是否继续培养(B级证据,2级推荐)。
推荐意见6:类器官接种密度需根据培养板规格和细胞类型优化(以24孔板计,5×104~1×105个细胞/孔),培养初期72 h内应完成首次换液,以确保类器官的存活和生长(B级证据,2级推荐)。
推荐意见7:培养基宜采用Advanced DMEM/F12为基础的核心培养基框架,并标准化核心添加组分(N2、B27等)、核心生长因子(EGF、Noggin、R-spondin1等)及可选小分子化合物;不同癌种允许在统一框架下进行配方微调(B级证据,1级推荐)。
推荐意见8:抗生素应分阶段规范化使用,组织接收清洗阶段可采用更优的抗污染清洗策略。原代早期可短期保护性使用,后续尽量停用并定期开展支原体污染监测,避免长期使用抗生素掩盖污染或影响细胞状态(B级证据,2级推荐)。
2.4 类器官传代培养
传代操作旨在为类器官提供新的生长空间和充足的营养,以避免因过度拥挤、营养耗尽而导致的中心坏死。传代节点主要依据类器官的密度、大小和生长状况来判断。通常,当培养孔中的类器官数量密集、体积增大(如直径超过300 µm),且部分类器官中心因细胞凋亡而呈现暗色时,即表明需要进行传代。囊性类器官直径达到200~300 μm或实心致密类器官密布整个培养孔时,即视为已达到适宜的传代程度[16]。类器官传代周期通常为1~3周,传代比例则根据不同类器官的增殖速率而异,从生长缓慢的1∶2到快速增殖的1∶5不等。
传代操作需要先将类器官从三维基质支架中取出并消化成小细胞簇后重新种植。收集培养孔中的类器官[可使用冰冷磷酸缓冲盐溶液(phosphate-buffered saline,PBS)缓慢吹洗培养孔使基质胶部分解离后移取悬液],低速离心后弃去上清,加入适量消化液(如TrypLE)于37 ℃水浴中消化数分钟。消化时间需严格控制,一般TrypLE消化不超过15 min,以防止过度消化导致细胞表面受损。当绝大多数大团块已解离为直径<50 µm的小细胞簇时,立即终止消化。终止后再次评估细胞活力,要求消化后细胞存活率应≥80%。低于此标准提示消化过程对细胞造成了较大损伤,应优化消化条件。随后以(200~400)×g低速离心3~5 min收集细胞,经计数后按1∶2~1∶5的比例重新混入基质胶进行下一代培养。
在传代培养过程中,应建立完善的过程记录和监控制度。每次传代操作都必须准确记录日期、传代比例及代次等信息,并将这些数据录入信息管理系统以确保可追溯。此外,形态学监测非常重要:在培养过程的关键节点(如换液后、传代前后),应观察类器官的形态和数量变化,必要时拍照留存。图像记录有助于评估类器官的结构完整性和生长动态,如观察是否出现空泡、坏死、分化改变等。形态学记录也应作为质量控制的重要组成部分,可用于后期的回顾性分析。
推荐意见9:类器官应在适宜时机及时传代扩增,避免因过度生长导致坏死和克隆选择。传代过程应严格控制酶消化时间,确保消化后细胞存活率在80%以上;并建议根据生长情况将传代比例调整为1∶2~1∶5之间,以维持后续培养的良好状态(B级证据,2级推荐)。
推荐意见10:建议建立类器官培养全过程的记录和监测机制,每次传代需记录传代时间、比例和代次,并定期进行显微镜下的形态学观察和影像记录,以确保培养过程可追溯、模型形态稳定(A级证据,1级推荐,GB/T 37864-2019)。
2.5 类器官冻存和复苏
类器官的高效冻存和复苏是建立“活体生物样本库”的基石,这为科学研究和临床应用提供了可再生的宝贵资源[30-31]。推荐方法是将处于良好生长状态的类器官(以小碎片或完整结构形式)重悬于含有低温保护剂的冻存液中。建议优先采用无血清、化学成分明确的商业化冻存液。此类试剂批次间稳定性好,无动物源性成分,能有效地避免外源因子污染及血清成分对后续药敏检测基线的干扰。在缺乏专用试剂的基础研究场景中,可使用传统方案,即90%的血清并添加10%的二甲基亚砜(dimethyl sulfoxide,DMSO)[7],但需注意,高浓度血清存在较大的批次间差异及潜在病原体风险,且血清中的生长因子残留可能影响类器官复苏后的药物敏感性表现。因此,在涉及精准医疗检测或多中心数据共享时,不推荐使用含血清的冻存液,建议逐步向无血清体系过渡。
采用程序性降温法进行冷冻,理想的降温速率为-1 ℃/min,这可通过将商业化的细胞冻存盒置于-80 ℃的冰箱中实现[32],也可使用传统冻存剂配方并配合程序化降温仪实现更稳定的控速降温。在-80 ℃的环境中放置至少24 h后,应将冻存管迅速转移至液氮罐中进行长期稳定储存。
复苏过程与冻存同样关键。为最大化细胞存活率,必须快速复苏冻存管,通常将其置于37 ℃水浴中1~2 min,以防止微小冰晶重结晶为更大的、具有破坏性的冰晶。接近完全融化后,应立即将类器官悬液转移至3~5倍体积的基础培养基中稀释,后续经离心收集类器官沉淀。复苏后的类器官通常需要经历一定的恢复期,继续培养观察7~14 d应能重新形成类器官并进入生长扩增状态。若复苏后培养一段时间未见新的类器官结构出现,则提示冻存失败。为确保冻存方法的可靠性,建议对每一批次冻存的类器官都进行抽样试复苏,以验证实际存活率和建系成功率。
推荐意见11:类器官达到预定传代节点,应及时进行低温冻存备份。采用经验证的冻存液按约-1 ℃/min速率降温至-80 ℃后转入液氮环境中长期保存,可最大程度保障类器官的存活率和遗传稳定性[A级证据,1级推荐,国际生物与环境样本库协会(International Society for Biological and Environmental Repositories,ISBER)发布的第5版《最佳实践指南》]。
推荐意见12:冻存类器官在复苏时应快速解冻并及时去除冻存液。活力评估需与类器官特征匹配,推荐在温和解离后采用3D 腺苷三磷酸(adenosine triphosphate,ATP)发光法或活/死细胞荧光染色对结构体进行评估。冻存时间<6个月,复苏后细胞活性应≥70%,若冻存超过6个月,随着冻存时间延长,复苏后的细胞活力下降到30%~60%不等,但应在1~2周内能够重新建立类器官培养体系。建议每批次冻存样本定期抽样尝试复苏,评估冻存效果(B级证据,1级推荐)。
2.6 类器官质量控制
确保肿瘤类器官模型能够真实地代表来源患者的癌症特征,是质量控制的核心目标。质量控制贯穿于样本采集与接收、样本处理与原代培养、传代扩增、冻存与复苏4个阶段,并在关键节点设置入库判定和异常处置。现有文献[29,33-34]普遍支持采用多层次的质量控制策略来全面评估模型的保真度。考虑到不同组织来源/肿瘤类型及培养体系的差异,质控应遵循用途适配原则:在本共识提出的通用最低要求基础上,各单位可按癌种、来源类型和研究用途增补特异性指标和判定标准。
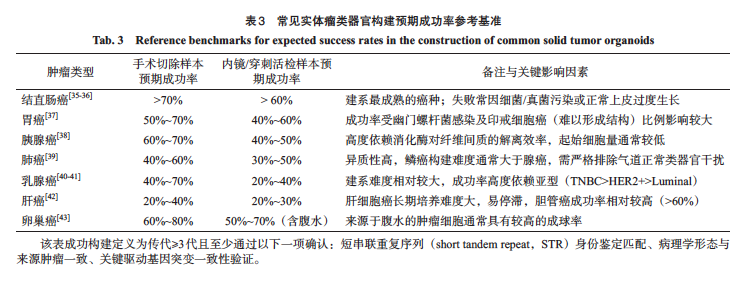
实验室应建立建系成功率的基准监控机制。建系成功率受肿瘤类型、样本来源、既往治疗史及样本质量等多重因素影响。通常,未经放化疗的手术切除样本成功率最高,而经过多线治疗的穿刺样本成功率会显著降低。为便于各实验室评估自身技术体系的稳定性,本共识综合国内外文献及专家经验,汇总了常见实体瘤的预期建系成功率参考范围(表3)。若实验室的长期统计数据显著低于该参考范围下限,建议启动原因分析,从样本运输、酶解效率及培养基组分等方面排查技术缺陷。
一级质控包括对类器官的日常监测,涵盖形态学特征、生长状态及微生物污染。形态学观察不仅应描述类器官的大小(直径)、结构(如囊状、实心或葡萄状),还应关注结构复杂度、囊腔形成、出芽、碎片和坏死样改变等关键特征,并建议在固定时间点、固定倍率和统一标尺下进行规范化拍照留存,用于纵向比较和追溯。同时,建议将信息质控纳入质量控制范畴,对关键字段的完整性、准确性和一致性(含代次/批次、操作记录、质控结果、冻存位置等)进行核查,并保留版本/审计追踪;信息质控的类型和频次应在标准操作规程(standard operating procedure,SOP)中明确,并至少在接收、入库/共享前及定期复核时执行。还应建立严格的微生物污染检测流程,包括对细菌、真菌及支原体的定期筛查,仅凭肉眼/光学显微镜通常难以发现支原体污染,因此需采用专门检测[如聚合酶链反应(polymerase chain reaction,PCR)法、DNA染色等]并进行周期性复核[44]。此外,可基于类器官数量、直径、面积等指标绘制生长曲线以估算扩增效率,并结合传代间隔、比例及恢复时间等参数评价传代稳定性,用以识别异常衰退或生长行为漂移的批次。
二级质控侧重于类器官表型的保真度验证。通常通过组织病理学和免疫组织化学法实现,将类器官的H-E染色切片形态及关键分子标志物的表达模式与原始肿瘤组织进行直接比较。高质量的类器官模型应在组织结构和关键蛋白表达上与来源肿瘤保持高度一致。
三级质控关注点在于模型的身份确认和遗传保真度。为防止和鉴别细胞培养中常见的交叉污染问题,建议对每一个类器官系进行身份确认。STR分型是国际公认的人源细胞身份鉴定方法,可形成遗传指纹用于溯源和交叉污染排查。根据既定标准(如ANSI/ATCCASN-0002-2022),类器官与来源组织(或患者对照样本)的STR图谱匹配度应不低于80%[32, 45]。除身份确认外,评估类器官在长期培养过程中的基因组稳定性同样重要。建议比较类器官与原发肿瘤的关键驱动基因突变谱,并开展单核苷酸变异(single-nucleotide variants,SNV)、拷贝数变异(Copy Number Variations,CNV)等变异的一致性分析。有研究[46]表明,类器官具有高度的遗传稳定性,能够在多次传代后依然保留亲本肿瘤的关键驱动突变和拷贝数变异。然而,培养过程中的选择压力仍可能导致遗传漂变。通常类器官原代培养(P0)至第10代(P10)为早期代次,此阶段类器官刚建立,遗传特征与原肿瘤高度一致,细胞异质性保留较好,适合用于药敏测试或临床相关性研究[16,47-48];类器官培养超过20代后(>P20),为晚期代次,此阶段类器官可能因体外长期培养发生遗传漂变或表型改变,需联合多组学验证遗传保真度,避免用于治疗决策模型。因此建议在早期和晚期传代时进行基因组学分析(如全外显子组测序),以记录类器官的遗传演变,确保其在特定研究中的持续适用性。当类器官用于药敏测试或机制研究时[37,49],建议增加功能层面的验证,包括药敏测试结果的重复性评估(设置阳性/阴性对照、评估实验质量指标如Z′因子等),以及与研究问题相关的信号通路活性检测/读出(如特定通路标志分子表达、报告系统或磷酸化水平等),用于支持可用且可解释的功能一致性。
另外,需制定异常情况的分级处置和预防改进流程。对于经质控检出的异常批次,应根据风险等级采取差异化措施:如发现某批次类器官活力显著下降甚至失活(如存活率<50%),应标记为“失效”并隔离处置,不再用于实验;如遇培养物被污染(如培养基浑浊、镜下见到细菌或真菌),应迅速弃去污染的培养物,彻底消毒相关培养器具;如质控发现混入正常细胞或克隆漂移,应优先回溯至已验证的早期代次。同时,应将质控结果作为技术体系持续改进的依据:如针对污染需追溯源头,强化对相关试剂和操作的无菌监测;针对细胞纯度问题,则视需要采用选择性培养体系或重新取材建系。通过及时整改与长效优化相结合,可全方位保障类器官模型的质量和可比性。
本共识建议将可入库/可共享的肿瘤类器官最低放行标准概括为:培养物无细菌、真菌和支原体污染,形态学和生长状态稳定且可追溯记录完整;与来源肿瘤在组织学形态及关键分子标志物表达上具有一致性;完成身份确认并通过交叉污染排查(如STR与来源样本匹配度一般≥80%);在预定用途所需的代次范围内维持可接受的遗传保真度(关键驱动事件/SNV/CNV一致性满足研究需求),必要时以药物敏感性或通路活性作为用途导向的功能验证。
推荐意见13:应在类器官建立的关键节点进行组织病理学和分子标志物的保真度验证。建议在每个类器官系成功建立、入库前及用于关键研究或共享前,常规进行组织病理学评估。通过H-E染色比较类器官与来源肿瘤的组织学形态,并采用免疫组织化学法检测关键分子标志物(如诊断、分型或治疗靶点相关的蛋白)的表达,标志物组合可根据肿瘤类型、组织来源及预定用途确定。经验证的类器官模型,其组织结构和标志物表达模式应与对应的原始肿瘤组织高度一致(B级证据,1级推荐)。
推荐意见14:建议建立并执行分级分类的质量控制体系,对类器官模型全生命周期进行质量监控,包含异常情况处置预案,并将一级质控(常规监测)贯穿于日常培养,必须包括:显微形态学观察并规范记录其大小、结构复杂度、囊腔形成及出芽等关键形态特征,建议定期拍照留存;细菌、真菌和支原体筛查,并建议至少在接收及疑似污染时进行支原体检测;二级质控(表型鉴定)作为模型保真度的核心验证,应常规开展;三级质控(遗传鉴定)建议在早期和后期代次进行基因组测序比对和STR分析,其中STR与来源组织匹配度一般应≥80%,至少应验证类器官与来源肿瘤在关键驱动突变上的一致性。对晚期代次类器官用于关键研究或潜在临床决策支持时,宜再次进行基因组验证(B级证据,1级推荐)。
推荐意见15:建议将生长动力学评估和功能验证纳入应用相关质控,可通过生长曲线、扩增效率及传代稳定性评价培养状态;当类器官用于药敏测试时,应设置阳性/阴性对照,并报告基本实验质量指标(如Z′/Z因子、变异系数等)以确保结果可靠。建议在实验体系建立并经预实验验证的前提下,将Z′/Z因子≥0.5作为基本可接受标准之一,阴性对照孔变异系数≤15%;必要时结合检测平台和终点指标进一步优化阈值(B级证据,2级推荐)。
2.7 实验室建设和运行管理要求
高质量的类器官培养离不开合格的实验室基础条件和专业技术团队。开展类器官构建的机构应建立并维持覆盖全流程的质量管理体系,确保操作能力、公正性和一致性的各项要求落实到位。
2.7.1 人员资质和培训
承担类器官构建和研究的人员应具备相应的教育背景和培训经历,并通过严格考核。所有关键岗位人员(如样本处理、细胞培养、质量检测等)都应有明确的资格要求,并经过系统的岗前培训。培训内容应包括无菌操作规范、细胞培养原理、仪器设备使用、生物安全及应急预案等。上岗后还需持续在职培训,定期更新专业知识和操作技能。建议建立客观的能力评估机制,如定期组织盲样操作考核或比对实验,确保人员技能达标。有条件的单位宜定期参加或组织多中心质控比对/能力验证,包括盲样类器官的STR分型一致性比对、病理学判读一致性评价及药敏测试中心间一致性评估,结果可作为实验室能力验证、持续改进和多中心数据整合的重要依据。所有培训和考核记录均应存档备查。同时,实验室应推行SOP,使不同人员严格按照统一步骤执行实验,以减少人为差异。良好的人员管理能够显著提高类器官培养的一致性和成功率。
2.7.2 实验室环境和分区
类器官培养对无菌环境和空气洁净度有较高要求,实验室建设和运行应符合细胞和组织培养实验室的规范。应根据功能合理进行区域分隔布局,通常需划分样本接收区、组织处理区、培养区和储存区等相对独立的区域,并通过设计合理的气流方向和人员/物流通道,避免产生交叉污染,气流应遵循从清洁区到潜在污染区的单向流动原则[33]。各分区的空气洁净度等级可参照洁净室的相关标准进行控制:组织解离和细胞接种等核心无菌操作区域应达到ISO 5级洁净度(相当于局部层流工作台内环境);培养温育和试剂储存区域可达到ISO 7级洁净度(相当于洁净室的整体环境)。实验室的温度和湿度也需控制在适宜范围:一般环境温度为18~26℃,相对湿度为40%~70%。其中培养操作间应配备恒温控制系统,将局部温度稳定在37 ℃±0.5 ℃,CO2体积分数稳定在5%±0.2%。这些环境参数需配备监测和报警装置,以便在偏离设定值时及时调整。
2.7.3 仪器和设备配置
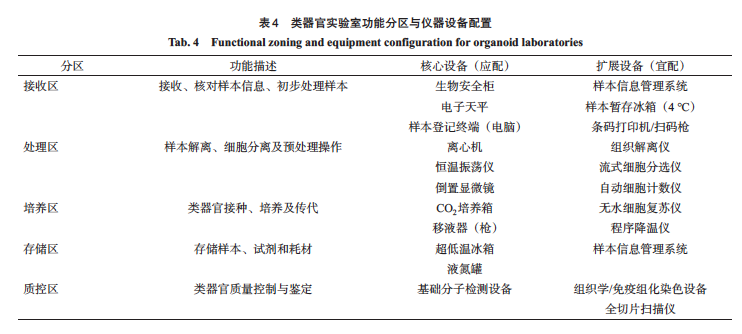
进行类器官构建需要配备一系列必要的实验设备。各功能分区应根据工作需要配置核心设备(表4),并可选配扩展设备以提高效率。
2.7.4 试剂和耗材管理
用于类器官培养的各类培养基、消化酶、生长因子等试剂对实验结果有重大影响,必须加强质量管理。所有试剂应有可靠来源并保证质量可追溯;入库时应查验供应商提供的质量证明文件或检测报告。对于可能影响类器官培养成功率的关键试剂(如基质胶、消化酶混合液等),建议建立供应商审计和批次质检制度。例如,基质胶为动物源混合基质,不同批次在成分和强度上可能存在差异,实验室可对新批次基质胶进行小规模试验以评估其支持类器官生长的效果,或检测其蛋白质浓度等指标;必要时可更换供应商或特定批次。条件允许时,可对去细胞外基质或化学定义的合成水凝胶等替代基质开展等效性评估,以进一步降低批次不确定性。
推荐意见16:类器官实验室应建立覆盖“人-机-料-法-环”全要素的质量管理体系。人员(人)必须经过系统培训且严格遵守SOP;环境(环)的核心操作区洁净度需达到ISO 5级;关键仪器设备(机)必须定期校验并良好运行;关键试剂耗材(料)需建立批次质检制度以保证质量;所有操作方法(法)均应标准化;通过对各环节(环)的严格管控,确保类器官培养全流程的规范性、稳定性和可追溯性(A级证据,1级推荐,ISO 14644-1:2015)。
2.8 数据管理和生物安全
样本和数据权限管理方面,应明确样本和相关数据的管理主体、使用边界及审批机制。样本及其关联数据的共享和使用应遵循知情同意和伦理审查要求,建立成文的共享使用申请程序和分级授权机制;对外提供或共享时应通过正式协议(如材料/数据使用协议)明确供体、样本库(管理方)和使用方的权利义务,以及数据共享、知识产权和利益分配等事项;并制定数据共享政策,规定可访问和可提供的数据类型、范围及安全要求。
类器官培养过程中产生的含人体组织/细胞、培养物及其污染耗材(如移液器吸嘴、离心管、培养板、基质胶残余等)的废物应按医疗废物管理要求进行分类收集、包装标识、内部转运、暂存和集中处置,并建立交接登记和应急处置流程。医疗卫生机构应建立医疗废物管理责任制和岗位职责,制定医疗废物分类收集、内部运送、暂存、对外移交及发生泄漏/扩散等意外事件的应急预案,确保全过程可追溯和人员职业防护落实到位。
推荐意见17:应建立样本与数据访问委员会和授权机制(或等效治理流程),形成标准化申请、审核、授权、留痕和撤销流程;对外共享须签署材料/数据使用协议,明确权责边界、用途限制、再分发限制、知识产权和成果署名/利益分配安排,并与知情同意和伦理批件保持一致(A级证据,1级推荐,GB/T 38736-2020,《中华人民共和国人类遗传资源管理条例》及其《实施细则》)。
推荐意见18:应建立并执行实验室生物废弃物处理SOP,覆盖“分类收集—包装标识—内部转运—暂存—对外移交—处置”全流程,并保存交接和处置记录,配套泄漏/扩散应急预案和职业防护要求(A级证据,1级推荐,《医疗废物管理条例》《医疗机构医疗废物管理办法》《医疗废物分类目录》)。
2.9 信息化管理
建立完善的类器官信息管理系统(organoid information management system,OIMS)对于提高样本管理效率和模型数据可追溯性至关重要。本共识强烈建议有条件的单位开发或采用专门的软件平台,对类器官研究的全流程进行数字化管理。一个完善的信息系统应至少具备以下功能:
⑴ 样本溯源与双向追溯:登记每个类器官来源患者的基本信息(脱敏编码后)、知情同意和伦理信息、样本采集时间和部位、病理学诊断结果等,实现从患者到类器官的来源追溯。为每个类器官赋予唯一编号以支持查询、比对和审计记录,满足样本及其关联数据的可追溯管理要求。在此基础上,从临床实际需求出发,OIMS宜预留标准化接口与医院电子病历系统对接,将类器官全生命周期关键数据(建模、传代、质控、冻存、复苏、药敏/组学结果等)与患者诊疗过程和随访数据进行结构化关联,形成“患者→类器官”和“类器官→患者结局/疗效反馈”的双向追溯能力,为未来临床转化、个体化治疗优化和真实世界证据积累提供可重复使用的数据内容。
⑵ 库存管理:记录类器官培养物当前所在的位置和状态,包括在培情况及冻存管的位置(如所属冰箱和架子位置等)。样本的转移或出入库操作均由系统登记,避免混淆和遗失。
⑶ 培养过程记录:系统应支持录入培养过程中的关键操作记录和数据,如每次传代的时间和代次、更换培养基的配方和时间、添加生长因子浓度、是否发生过污染等。理想情况下,系统还能与实验设备联动,如对接培养箱监测模块获取温度、CO2浓度异常报警等信息,实现全程信息记录。
⑷ 质量控制数据:将每个类器官的重要质控结果录入系统,包括形态学照片、STR鉴定结果、病理学和分子标志物检测结果、支原体检测结果等。这样在需要评估某个类器官时,可直接调取完整档案。对于质控未通过的批次也应予以标识,避免误用。
通过信息化管理,可以极大地减少人工记录的错误,提高工作效率,并为多中心合作和数据共享打下基础。特别是在建立国家或区域性的类器官生物样本库时,统一的信息管理标准将有助于整合不同单位的数据资源,实现大数据分析和挖掘,服务于基础研究和转化应用。
推荐意见19:建议建设覆盖类器官全生命周期的信息管理系统,对样本来源、培养操作、质控结果和存储位置等进行数字化管理,实现样本的可追溯性和数据的规范共享(A级证据,2级推荐,GB/T 37864—2019)。
3 讨论及展望
本共识的制定过程尽可能参考了国内外相关文献和标准,并凝聚了专家组的经验意见,系统提出了肿瘤类器官构建的全流程通用技术框架,覆盖样本采集与接收、组织处理与原代培养、接种与扩增、冻存复苏、分级质量控制、合规与伦理等关键环节,旨在提升不同机构间操作的一致性和结果的可比性。尽管如此,本共识仍存在一些局限性。首先,类器官技术作为新兴领域,仍处于快速发展阶段,许多推荐意见缺乏大规模临床或实验研究的高等级循证医学证据的支持,部分条目主要依据专家共识和实践经验,证据等级相对有限,需要在更广泛的真实世界场景中进一步验证和细化。其次,本共识聚焦于人源肿瘤类器官构建的一般性技术要求,对不同肿瘤类型、不同组织微环境背景及不同应用场景(如药敏测试、器官芯片、再生医学等)所需的专门规范未深入展开,因此在具体实践中,各机构仍需在本共识核心框架下结合本地条件、样本特点和研究目的进行补充和扩展。
面向未来,肿瘤类器官领域的关键挑战和发展方向也日益清晰:一方面,当前广泛使用的动物来源基质胶(如Matrigel)存在成分复杂、批次差异和动物源性等问题,可能影响实验可重复性和临床转化的规范化要求,推动可调控及可规模化替代产品的研发和验证是提升标准化水平和产业化可行性的核心环节之一;另一方面,单纯肿瘤上皮细胞类器官在复杂肿瘤微环境模拟方面仍存在天然不足,肿瘤免疫细胞、基质细胞、血管及神经等组分的缺失,会限制对免疫治疗反应、侵袭转移、耐药演化等真实生物学过程的刻画,因此构建更复杂、更接近体内生态位的模型将成为重要的发展趋势,从而在培养体系标准化、质控指标和结果解释方面产生更高的要求。与此同时,随着多组学测序、空间组学和高通量药敏试验等技术的普及,类器官研究正在从能建立走向可量化、可预测、可验证的阶段,如何在统一元数据和质控标准下实现跨平台数据整合、建立可共享的类器官资源和分析框架,并通过更严格的临床一致性验证和前瞻性研究推动其进入真实世界决策链条,仍是从科研工具迈向临床转化的关键门槛。
鉴于本领域方法学迭代迅速、证据持续累积,本共识旨在为从事肿瘤类器官研究的科研人员和临床工作者提供科学的技术指导框架,以提高模型的保真度和可靠性。未来将结合新的循证医学研究和实践经验定期修订迭代,以不断完善肿瘤类器官构建和质控的通用标准体系,促进不同研究间的数据共享和横向比较,并加速其在肿瘤精准诊疗和转化应用中的规范落地。
第一作者:
王琦,硕士,复旦大学附属肿瘤医院病理科生物样本库类器官平台负责人。
通信作者:
许蜜蝶,博士,副主任医师,复旦大学附属肿瘤医院病理科生物样本库主任。
[参考文献]
[1] BRAY F, LAVERSANNE M, SUNG H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2024, 74(3): 229-263.
[2] BALANI S, NGUYEN L V, EAVES C J. Modeling the process of human tumorigenesis[J]. Nat Commun, 2017, 8: 15422.
[3] BEN-DAVID U, HA G, TSENG Y Y, et al. Patient-derived xenografts undergo mouse-specific tumor evolution[J]. Nat Genet, 2017, 49(11): 1567-1575.
[4] TUVESON D, CLEVERS H. Cancer modeling meets human organoid technology[J]. Science, 2019, 364(6444): 952-955.
[5] XIA X Y, LI F, HE J, et al. Organoid technology in cancer precision medicine[J]. Cancer Lett, 2019, 457: 20-27.
[6] POLAK R, ZHANG E T, KUO C J. Cancer organoids 2.0: modelling the complexity of the tumour immune microenvironment[J]. Nat Rev Cancer, 2024, 24(8): 523-539.
[7] DRIEHUIS E, KRETZSCHMAR K, CLEVERS H. Establishment of patient-derived cancer organoids for drug-screening applications[J]. Nat Protoc, 2020, 15(10): 3380-3409.
[8] PHIFER C J, BERGDORF K N, BECHARD M E, et al. Obtaining patient-derived cancer organoid cultures via fine-needle aspiration[J]. STAR Protoc, 2020, 2(1): 100220.
[9] SEGHERS S, LE COMPTE M, HENDRIKS J M H, et al. A systematic review of patient-derived tumor organoids generation from malignant effusions[J]. Crit Rev Oncol Hematol, 2024, 195: 104285.
[10] PAN C, WANG X P, YANG C, et al. The culture and application of circulating tumor cell-derived organoids[J]. Trends Cell Biol, 2025, 35(5): 364-380.
[11] LIU B, WANG Q, QIN G, et al. A retrospective quality audit of a prostate cancer biobank reveals procurement method as the critical determinant of biospecimen fitness-for-purpose[J]. Biopreserv Biobank, 2026. Online ahead of print.
[12] DROST J, CLEVERS H. Organoids in cancer research[J]. Nat Rev Cancer, 2018, 18(7): 407-418.
[13] SATO T, STANGE D E, FERRANTE M, et al. Long-term expansion of epithelial organoids from human colon, adenoma, adenocarcinoma, and Barrett’s epithelium[J]. Gastroenterology, 2011, 141(5): 1762-1772.
[14] VAN DE WETERING M, FRANCIES H E, FRANCIS J M, et al. Prospective derivation of a living organoid biobank of colorectal cancer patients[J]. Cell, 2015, 161(4): 933-945.
[15] BOJ S F, HWANG C I, BAKER L A, et al. Organoid models of human and mouse ductal pancreatic cancer[J]. Cell, 2015, 160(1/2): 324-338.
[16] DEKKERS J F, VAN VLIET E J, SACHS N, et al. Long-term culture, genetic manipulation and xenotransplantation of human normal and breast cancer organoids[J]. Nat Protoc, 2021, 16(4): 1936-1965.
[17] SACHS N, DE LIGT J, KOPPER O, et al. A living biobank of breast cancer organoids captures disease heterogeneity[J]. Cell, 2018, 172(1/2): 373-386.e10.
[18] WANG R, HARRIS T, NEGRÓN-FIGUEROA D, et al. Protocol for culturing patient-derived organoids of cervical cancer[J]. STAR Protoc, 2024, 5(4): 103353.
[19] TIRIAC H, FRENCH R, LOWY A M. Isolation and characterization of patient-derived pancreatic ductal adenocarcinoma organoid models[J]. J Vis Exp, 2020(155): e60364.
[20] HIROKAWA Y, CLARKE J, PALMIERI M, et al. Low-viscosity matrix suspension culture enables scalable analysis of patient-derived organoids and tumoroids from the large intestine[J]. Commun Biol, 2021, 4(1): 1067.
[21] PRICE S, BHOSLE S, GONÇALVES E, et al. A suspension technique for efficient large-scale cancer organoid culturing and perturbation screens[J]. Sci Rep, 2022, 12: 5571.
[22] FUJII M, SHIMOKAWA M, DATE S, et al. A colorectal tumor organoid library demonstrates progressive loss of niche factor requirements during tumorigenesis[J]. Cell Stem Cell, 2016, 18(6): 827-838.
[23] YAN H H N, SIU H C, LAW S, et al. A comprehensive human gastric cancer organoid biobank captures tumor subtype heterogeneity and enables therapeutic screening[J]. Cell Stem Cell, 2018, 23(6): 882-897.e11.
[24] NANKI K, TOSHIMITSU K, TAKANO A, et al. Divergent routes toward Wnt and R-spondin niche independency during human gastric carcinogenesis[J]. Cell, 2018, 174(4): 856-869.e17.
[25] SEINO T, KAWASAKI S, SHIMOKAWA M, et al. Human pancreatic tumor organoids reveal loss of stem cell niche factor dependence during disease progression[J]. Cell Stem Cell, 2018, 22(3): 454-467.e6.
[26] BROUTIER L, MASTROGIOVANNI G, VERSTEGEN M M, et al. Human primary liver cancer-derived organoid cultures for disease modeling and drug screening[J]. Nat Med, 2017, 23(12): 1424-1435.
[27] KIM M, MUN H, SUNG C O, et al. Patient-derived lung cancer organoids as in vitro cancer models for therapeutic screening[J]. Nat Commun, 2019, 10(1): 3991.
[28] EBISUDANI T, HAMAMOTO J, TOGASAKI K, et al. Genotype-phenotype mapping of a patient-derived lung cancer organoid biobank identifies NKX2-1-defined Wnt dependency in lung adenocarcinoma[J]. Cell Rep, 2023, 42(3): 112212.
[29] NEMATI N, BOECK N, LAMBERTI G, et al. Protocol for functional profiling of patient-derived organoids for precision oncology[J]. STAR Protoc, 2024, 5(1): 102887.
[30] WEEBER F, OOFT S N, DIJKSTRA K K, et al. Tumor organoids as a pre-clinical cancer model for drug discovery[J]. Cell Chem Biol, 2017, 24(9): 1092-1100.
[31] YANG R X, QI Y, ZHANG X Y, et al. Living biobank: Standardization of organoid construction and challenges[J]. Chin Med J, 2024, 137(24): 3050-3060.
[32] GAMERO-ESTEVEZ E, HENSEL I V, STEINHAUER M, et al. Protocol for immune cell isolation, organoid generation, and co-culture establishment from cryopreserved whole human intestine[J]. Bio Protoc, 2025, 15(1): e5157.
[33] ZHOU C C, WU Y B, WANG Z Y, et al. Standardization of organoid culture in cancer research[J]. Cancer Med, 2023, 12(13): 14375-14386.
[34] VLACHOGIANNIS G, HEDAYAT S, VATSIOU A, et al. Patient-derived organoids model treatment response of metastatic gastrointestinal cancers[J]. Science, 2018, 359(6378): 920-926.
[35] TAN T, MOURADOV D, GIBBS P, et al. Protocol for generation of and high-throughput drug testing with patient-derived colorectal cancer organoids[J]. STAR Protoc, 2024, 5(2): 103090.
[36] OOFT S N, WEEBER F, SCHIPPER L, et al. Prospective experimental treatment of colorectal cancer patients based on organoid drug responses[J]. ESMO Open, 2021, 6(3): 100103.
[37] JIANG K L, WANG X X, LIU X J, et al. Success rate of current human-derived gastric cancer organoids establishment and influencing factors: a systematic review and meta-analysis[J]. World J Gastrointest Oncol, 2024, 16(4): 1626-1646.
[38] GRÜTZMEIER S E, SODAL H M M, KOVACEVIC B, et al. EUS-guided biopsies versus surgical specimens for establishing patient-derived pancreatic cancer organoids: a systematic review and meta-analysis[J]. Gastrointest Endosc, 2024, 100(4): 750-755.
[39] HU Y W, SUI X Z, SONG F, et al. Lung cancer organoids analyzed on microwell arrays predict drug responses of patients within a week[J]. Nat Commun, 2021, 12(1): 2581.
[40] SCHWERD-KLEINE P, WÜRTH R, CHEYTAN T, et al. Biopsy-derived organoids in personalised early breast cancer care: Challenges of tumour purity and normal cell overgrowth cap their practical utility[J]. Int J Cancer, 2025, 156(11): 2200-2209.
[41] PRZANOWSKA R K, LABBAN N, PRZANOWSKI P, et al. Patient-derived response estimates from zero-passage organoids of luminal breast cancer[J]. Breast Cancer Res, 2024, 26(1): 192.
[42] WANG H C, CALVISI D F, CHEN X. Organoids for the study of liver cancer[J]. Semin Liver Dis, 2021, 41(1): 19-27.
[43] KOPPER O, DE WITTE C J, LÕHMUSSAAR K, et al. An organoid platform for ovarian cancer captures intra- and interpatient heterogeneity[J]. Nat Med, 2019, 25(5): 838-849.
[44] GERAGHTY R J, CAPES-DAVIS A, DAVIS J M, et al. Guidelines for the use of cell lines in biomedical research[J]. Br J Cancer, 2014, 111(6): 1021-1046.
[45] VISCONTI P, PARODI F, PARODI B, et al. Short tandem repeat profiling for the authentication of cancer stem-like cells[J]. Int J Cancer, 2021, 148(6): 1489-1498.
[46] ROSSI G, MANFRIN A, LUTOLF M P. Progress and potential in organoid research[J]. Nat Rev Genet, 2018, 19(11): 671-687.
[47] SHI X H, LI Y G, YUAN Q Y, et al. Integrated profiling of human pancreatic cancer organoids reveals chromatin accessibility features associated with drug sensitivity[J]. Nat Commun, 2022, 13(1): 2169.
[48] TAN R H, ZHANG Z, DING P R, et al. A growth factor-reduced culture system for colorectal cancer organoids[J]. Cancer Lett, 2024, 588: 216737.
[49] FRANCIES H E, BARTHORPE A, MCLAREN-DOUGLAS A, et al. Drug sensitivity assays of human cancer organoid cultures[J]. Methods Mol Biol, 2019, 1576: 339-351.
来源:中国癌症杂志