引用本文: 马佳, 柏预立, 韩光. 硼中子俘获治疗现状及发展方向[J]. 肿瘤防治研究, 2026, 53(4): 243-250.
基金项目: 湖北省肿瘤医院启航人才项目 (2025HBCHQHRC011)
作者单位:430079 武汉,华中科技大学同济医学院附属湖北肿瘤医院放射治疗中心
通信作者:韩光,男,博士,主任医师,主要从事各种常见恶性肿瘤的放疗为基础的临床及机制研究,E-mail:hg7913@163.com,ORCID: 0000-0001-5500-3338
作者简介:马佳,女,博士,主治医师,主要从事肺癌、食管癌等常见恶性肿瘤的诊疗,ORCID: 0000-0002-2383-7706;柏预立*,女,硕士,主要从事恶性肿瘤放射治疗的临床研究,ORCID: 0009-0006-0500-2023(*:并列第一作者)
专家简介 韩光 教授 主任医师,肿瘤学博士,硕士生导师,湖北省肿瘤医院放疗中心主任。美国内布那斯加州大学医学院(UNMC)放疗中心访问学者;中国临床肿瘤学会(CSCO)放疗专委会委员;中华医学会肿瘤放射治疗分会肺癌组、硼中子俘获治疗(BNCT)组委员;湖北省免疫学会放射免疫专业委员会主任委员;湖北省医学会肿瘤放射治疗分会副主任委员;湖北省医师协会肿瘤放射治疗医师分会副主任委员。从事肿瘤放射治疗工作近20年,擅长肺癌、食管癌、鼻咽癌、脑胶质瘤、头颈鳞癌和乳腺癌等各种常见恶性肿瘤放疗为基础的临床及机制研究。研究方向主要包括BNCT综合治疗、免疫联合放疗、肺癌脑转移生物标志物及信号转导、肿瘤放化疗、肿瘤抗血管生成治疗、正常组织的放射耐受及不良反应等。曾获得军事科学技术二等奖、湖北省科技进步二等奖。主持国家及省市级科研课题10项;以第一或者通讯作者发表论文70余篇,其中SCI论文48篇,包括Cell Research,Eur Respir J,Int J Radiat Oncol Biol Phys,Radiother Oncol,J Infect,Clin Microbiol Infect等期刊,参编医学论著5本 。
摘要: 硼中子俘获治疗(BNCT)作为一种精准肿瘤治疗技术,国际上以日本为代表已进入成熟临床阶段。中国起步虽晚,但凭借自主研发,在加速器中子源设备、硼药国产化及临床疗效验证等方面实现快速发展,部分指标达到国际先进水平。未来需聚焦第三代硼药研发、治疗规范、治疗成本的降低与可及性的提升,以构建具有竞争力的BNCT临床应用与技术创新体系。 关键词: 硼中子俘获治疗;临床现状;研究进展
0 引言
硼中子俘获治疗(Boron Neutron Capture Therapy, BNCT)是基于二元靶向原理的新一代肿瘤放疗技术,核心机制为:先向患者注射含硼药物,使其选择性富集于肿瘤组织;再通过PET/CT显像剂(如18F-FBPA)检测肿瘤与正常组织的硼浓度比值(T/N),筛选T/N值达标的患者;最后用中子束照射,中子与肿瘤细胞内的硼-10发生核反应,产生射程仅4~9 μm的α粒子(4He)与反冲7Li核,精准破坏肿瘤细胞DNA,同时最大程度保护正常组织[1-2]。用于BNCT的中子束主要通过核反应堆中子源、加速器中子源、自发裂变中子源(以人工锎Cf为主)产生[3],其中加速器中子源是当前主流发展方向。 根据2025年第63届粒子治疗合作组织(PTCOG)BNCT小组委员会会议纪要,中国内地现有13个BNCT中心,其中11个处于建设阶段[4]。2024年5月,厦门弘爱医院完成国内首例BNCT注册临床试验患者治疗,2025年8月,该院完成Investigational New Drug(IND)Ⅰ期临床试验的全部患者入组,成为国内首个完成BNCT注册Ⅰ期临床试验的机构;同期东莞市人民医院首次使用国产BNCT系统全流程治疗复发鼻咽癌患者;2025年10月,海南博鳌成功举办第十二届BNCT世界青年研究者大会(YBNCT 2025),掀起国内BNCT中心建设热潮。中国BNCT项目汇总于表1。基于上述背景,本文系统梳理国内外BNCT技术发展现状,通过深度对比与数据支撑,剖析核心问题并展望未来方向。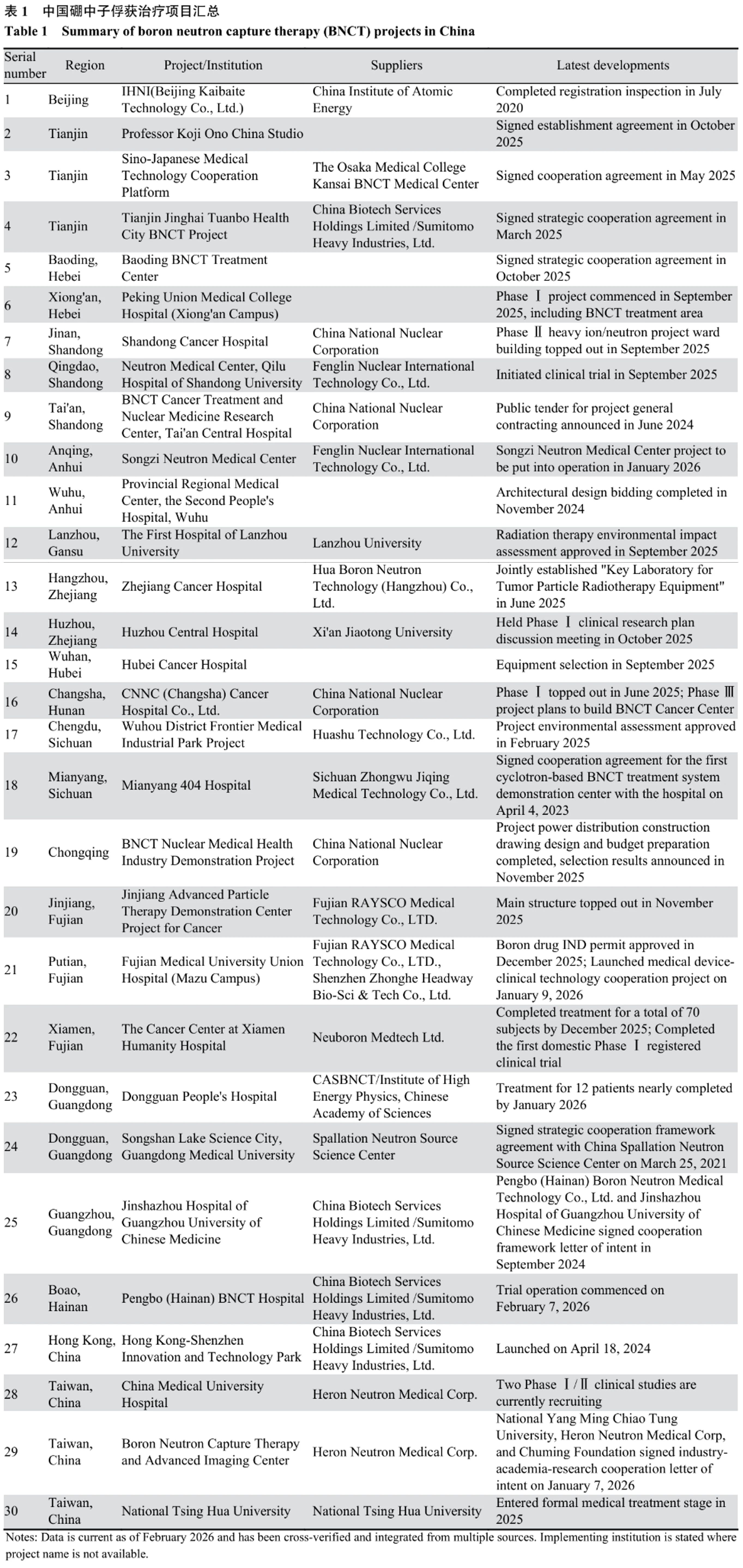
1 国外硼中子俘获治疗的发展现状
自1936年Gordon Locher首次提出BNCT概念以来,该技术历经近90年发展,核心突破集中于硼药与中子源两大领域[5]。 1.1 硼药迭代 早期第一代硼药(以硼酸为代表)受合成技术限制,存在肿瘤富集时间短、T/N比值低的缺陷,导致疗效不佳,技术发展停滞[6-7]。直至1989年,以硼苯丙氨酸(BPA)和硼卡钠(BSH)为代表的第二代硼药进入人体临床试验,BPA的T/N比值可达3.0~3.5,BSH在中枢神经系统肿瘤中实现特异性富集,才推动BNCT进入发展新阶段[3,8-10]。目前全球仅BSH和BPA获批临床应用[11],但其局限性阻碍了临床推广:BPA的肿瘤靶向性不足,根据一项18FBPA-PET研究显示,约17%的患者T/N比值未达到2.5的治疗阈值[12-13];BSH主要适用于中枢神经系统肿瘤[14]。 1.2 中子源技术升级 国际上已形成“从核反应堆向加速器转型”的明确路径。根据国际中子俘获治疗学会(ISNCT)数据,截至2025年底,全球正在运营、交付或建设的加速器型BNCT设施共29个,其中除中国的9个项目外,其余20个分布在日本、欧洲及美洲等国家和地区[15]。多国研发出射频四极场加速器+漂移管直线加速器(RFQ+DTL),直线、回旋、静电等适配BNCT的加速器;国际上针对基于加速器的BNCT中子源(AB-BNCT)中子转换靶散热问题,提出了液态锂靶、旋转锂靶等解决方案;美国、日本、意大利等国研发了NCTPlan、NeuCure® Dose Engine、BDTPS等专属治疗计划系统,日本NeuCure™ System成为首个获批临床的AB-BNCT系统,实现了加速器中子源技术的临床落地[16]。 1.3 临床研究现状 国际上BNCT临床试验以Ⅰ期、Ⅱ期为主,聚焦局部复发或晚期头颈癌、恶性脑肿瘤、软组织肿瘤、黑色素瘤等浅层肿瘤,但统一治疗标准尚未形成,给药剂量、辐照时间及联合策略均呈现高度异质性。BPA的给药剂量跨度为40~900 mg/kg[17-18],其中250 mg/kg和500 mg/kg方案较为常见[19];BSH的常用剂量为100 mg/kg[20-24]或固定剂量5 g[25-26]。给药时机依据试验目的存在显著差异,包括辐照前数小时滴注、辐照期间持续滴注以及术中给药。联合治疗策略同样差异显著,筑波大学、大阪医科大学在治疗新诊断胶质母细胞瘤时,将BNCT与常规分割外照射放疗联用[25,27];大阪医科大学还探索了BNCT联合贝伐珠单抗治疗[28];日本京都大学和筑波大学、芬兰及中国台湾在治疗中采用了二次BNCT,但二次治疗的给药方案及间隔时长尚未形成统一标准[19,29-32]。此外,当前临床研究重点正从已证实有效的癌种,向复发性高级别脑膜瘤、血管肉瘤及新发胶质瘤等更多类型的实体瘤拓展[27,33-34],旨在持续拓宽该疗法的应用边界。
2 国内硼中子俘获治疗的发展现状
2.1 国产设备研发 中硼医疗“极锋刀”系统作为国内首个启动正式注册临床试验的AB-BNCT设备,最大可治疗深度达11 cm[35];配套的“蝠魟NeuMANTA”专用治疗计划系统,计算效率为著名MCNP6代码的2~3倍,且两者剂量计算结果的最大偏差仅为3%,剂量分布基本一致[16];利用其完成的对1例常规治疗不敏感的间叶性软骨肉瘤,肿瘤最大径缩小了45.8%[36]。中国国科中子公司也提出了旋转锂靶设计方案,该方案有望通过扩大辐照面积降低平均热功率密度,从而提升中子产额。西安交通大学BNCT团队设计的RFQ加速器已实现20 mA峰值束流稳定输出,通过多层复合结构设计与工艺优化,成功制备微米级氢扩散层,实现中子转换靶连续运行150小时无氢鼓泡,同时,创新边缘冷却结构解决了高功率散热难题;其与华硼中子科技联合开发的HealingBeam_TPS已实现自主研发,其蒙特卡罗引擎计算效率比传统算法高3倍左右,且偏差小于3%[16]。 2.2 硼药研发 国内已形成“第二代硼药规模化生产+第三代硼药临床前研发”的协同推进的发展态势。我国有4家公司已经具备大规模生产BPA的能力[37]。我国学者研发的相变溶菌酶修饰的氮化硼纳米粒子也展示了良好的抑瘤效应[38]。多种纳米制剂(如硼化卟啉纳米复合物BPN、外泌体包裹的10B碳点BCD-Exos等)在动物模型中展现出优异的肿瘤富集能力;小分子氟硼酪氨酸则表现出代谢稳定、正常脑组织摄取低的优势[37]。 2.3 临床规范探索 截至2025年10月,国内已在国家药监局药品审评中心(CDE)及国际临床试验注册平台(ICTRP)注册了13项BNCT相关临床试验,分布于厦门、东莞、中国台湾。 洪俊强等开展的国内首个AB-BNCT前瞻性研究(纳入14例复发难治性肿瘤患者)显示,治疗后90天所有患者客观缓解率(ORR)达64%,疾病控制率(DCR)71%,完全缓解率(CRR)为14%;最佳缓解疗效ORR为71%。安全性方面,最常见的不良反应为血清淀粉酶升高(发生率100%)、脱发(发生率71.4%)及高泌乳素血症(发生率64%),多数为1~2级,所有不良反应经观察或治疗后均恢复。生存数据显示,头颈部肿瘤1年生存率为71.4%,较以光子调强放疗为代表的传统挽救性再放疗提升近1倍,2年生存率为42.8%,复发脑肿瘤1年生存率为42.8%,与国际上AB-BNCT治疗同类肿瘤的先进水平相近[39-40]。
3 国内外BNCT技术发展横向对比
日本在BNCT领域已进入成熟的临床推广阶段,产业化路径相对清晰。2020年,日本率先将BNCT纳入国家健康保险,覆盖复发及不可手术的头颈癌,使其成为全球BNCT治疗患者最多的国家[41],截至2025年,日本小野公二教授团队累计完成治疗591例。欧美目前仍以科研和早期临床试验为主。2026年2月鹏博(海南)硼中子医院试运营,使我国成为全球第二个拥有正式获批BNCT临床治疗机构的国家,缩小了与日本临床推广应用的差距。中国在BNCT设备研发上与国际保持同步,在靶材散热等特定工程问题上展现出创新性,但设备普及度和商业化验证尚在进行中。国内已实现第二代药物大规模自主生产,打破进口依赖,但在第三代药物的原始创新和临床转化上仍需加速,目前与国外处于相同发展阶段。
4 关键问题评述
4.1 BNCT在肿瘤治疗中的定位 BNCT的核心价值在于“细胞级精准杀伤”,是传统治疗手段的重要补充,而非替代,其优势与局限需清晰界定。BNCT核心优势在于细胞选择性高、疗程短、性价比高。BNCT仅需1~2次照射,相较于传统放疗30次的疗程[42],可大幅降低患者时间成本;设备建设成本方面,BNCT为3.9亿元,约为质子治疗10~15亿元建设成本的1/3(以上费用数据由中硼医疗测算得出)。BNCT对传统放化疗抵抗的肿瘤有效,一项研究显示,针对复发性胶质母细胞瘤,BNCT仍能实现较好的局部控制:接受BNCT治疗的复发性高级别胶质瘤患者术后中位生存期达29.6个月,36例随访超过 3个月的患者中35例出现肿瘤缩小,局部复发率仅为22.2%[33]。 BNCT的局限性在于患者筛选严格,仅T/N比值≥2.5的患者适合治疗[13],且其超热中子束的有效治疗深度为皮下8~10 cm[43],即使是我国首套加速器BNCT装备系统“极锋刀”(NeuPex),最大治疗深度也仅达到11 cm[35],这一深度限制使得BNCT在当前技术条件下难以覆盖肝脏、胰腺等深部肿瘤。BNCT的治疗机制决定了它是一种局部的高精度治疗手段,仅对局部进展或局部复发且未发生广泛转移的患者有效。在多项BNCT临床试验中,纳入标准通常限定为局部进展或复发肿瘤,而广泛转移则被列为排除标准。 BNCT应作为传统放疗、化疗、靶向治疗失败后的“挽救性治疗手段”,优先用于复发头颈癌、脑胶质细胞瘤等难治性肿瘤[44-46]。未来可向“新辅助治疗”拓展,如探索术前BNCT能否缩小肿瘤体积,提高手术切除率。 4.2 BNCT在肿瘤治疗中的定位 4.2.1 技术瓶颈 目前国内第二代硼药的大规模产业化供应能力仍显不足[47],第三代硼药仍需数年才能进入临床。射频直线加速器存在成本高、系统复杂等固有难题;在加速器中子源靶系统中,氢鼓泡与散热问题被列为关键瓶颈,其中高功率锂靶的冷却技术直接制约了中子通量的提升;工程化应用需在提升中子品质与保证靶体稳定运行间取得平衡;尽管旋转靶理论产额更高,但其设计复杂,目前全球仅有两家机构提出设计方案[16]。 4.2.2 人才瓶颈 BNCT需放疗科医师、医学物理师、放射技师、核医学科医师、药师等多学科协同开展,但国内经系统培训的专业人才不足,其中医学物理师缺口最大,其原因在于培养体系的缺失:目前国内尚无高校开设BNCT相关专业方向,且缺乏统一的培训标准、规范的教材与考核体系。未来可通过在已有BNCT临床经验的医院建立人才培训基地,并设置理论与实践相结合的教学模式破解这一困境。 4.2.3 经济瓶颈 据台湾清华大学网站公开信息,BNCT治疗费用12万台币起步;中硼医疗测算治疗费用约为15万人民币,且因患者个体差异浮动。且短期内BNCT难纳入医保,治疗前的18F-FBPA PET/CT筛选检查多为需自费。同时,中硼医疗测算显示,单个BNCT中心建设成本约3.9亿元,投资回收期约8年,BNCT中心投资回报周期漫长,这可能导致医疗机构投资意愿不足。未来有望通过推动商业保险纳入、技术降本、建立“政府-企业-公益组织”三方补贴机制等措施加以解决。
5 未来技术路线展望
5.1 硼药研发升级 未来硼药研发将聚焦“高靶向、高富集、智能可控”三大方向,突破当前T/N比值与肿瘤穿透性瓶颈。 5.1.1 纳米载体硼药 采用聚乳酸-共聚乙醇酸(PLGA)、树枝状聚合物等生物相容性材料,构建负载硼化合物的纳米颗粒,如粒径在100~200 nm之间的PLGA纳米颗粒。该粒径范围内的纳米颗粒可通过高通透性和滞留(EPR)效应联合修饰肿瘤特异性配体(如RGD肽、叶酸)的主动靶向作用,实现肿瘤部位的高效富集[48-53]。 5.1.2 抗体偶联硼药 可考虑将硼化合物通过可裂解连接子与肿瘤特异性抗体(如抗EGFR、抗HER2、抗PD-L1抗体)偶联[54],实现“肿瘤细胞级”精准递送。 5.1.3 智能响应型硼药 设计对pH或酶敏感的硼药载体,使其在肿瘤微环境(如低pH、高基质金属蛋白酶MMP表达)中选择性触发硼化合物释放,从而提高T/N比值[55-58]。 5.2 中子源技术发展 5.2.1 紧凑型加速器 紧凑型加速器是降低部署难度、推动临床普及的关键。目前射频直线加速器(如RFQ)已实现长度5.8米,未来应实现更短长度、更高集成度,才能满足医院环境对设备占地和运行便捷性的要求[16]。 5.2.2 超热中子束优化 攻克高功率束流下靶冷却难题,优化加速器中子源靶体稳定性,以此实现超热中子通量的有效提升[16]。 5.2.3 加速器中子源装置低成本化 未来可考虑模块化设计、标准化生产以及关键部件国产化,以降低设备制造成本和维护费用,加快BNCT技术部署速度[16]。 5.2.4 智能化控制 与人工智能及多模态影像融合,未来可望实现从患者影像输入到剂量执行的全流程智能化闭环,包括加速器运行参数的自动调节、靶系统状态的实时监控,以及治疗计划系统的自适应计算等[16]。 5.3 联合治疗策略 5.3.1 BNCT+免疫治疗 BNCT与免疫治疗联用能产生协同抗肿瘤效应,显著诱导局部、区域抗肿瘤效果并触发远隔效应。有研究报道,对于免疫治疗和放疗无效的黑色素瘤小鼠模型,BNCT联合免疫治疗在BNCT治疗灶和远隔部位都可产生肿瘤抑制效果[59-60];机制上,BNCT对免疫细胞存活能力的影响极小,且能触发肿瘤细胞免疫原性死亡,并显著增强树突状细胞、T细胞和NK细胞活性,重塑肿瘤微环境[61]。 5.3.2 BNCT+靶向治疗 对于驱动基因阳性的肿瘤(如EGFR突变型肺癌),靶向药物可增强肿瘤细胞对硼药的摄取[62]。Kaniowski等研究了经硼簇修饰的抗EGFR mRNA反义寡核苷酸在不同细胞系中的作用,EGFR蛋白不仅参与癌症的发生与扩散,还会导致肿瘤对化疗和放疗产生耐药性,该研究设计的这种复合物本身即具有抗肿瘤效果——既能抑制EGFR基因的表达,又可作为硼载体应用于硼中子俘获治疗[63-64]。 5.3.3 BNCT+外照射治疗 该联合治疗的理论基础是采用外照射治疗照射深部肿瘤病灶,BNCT补充照射残留微小病灶,形成“互补治疗”模式[65]。BNCT与常规放疗的联合,是当前肿瘤放射治疗领域一个重要的研究方向,旨在结合两种技术的优势,实现更精准、更强大的肿瘤杀灭效果。虽然目前仍处于临床探索的早期阶段,面临诸多技术和规范化的挑战,但其背后的科学逻辑非常坚实,是未来放射肿瘤学一个极具潜力的发展方向。
6 结论
BNCT作为新一代精准肿瘤治疗技术,在难治性肿瘤治疗中展现出不可替代的优势。国际上以日本为代表已进入成熟推广阶段,在技术成熟度、临床规范等方面领先;中国虽起步晚,但在加速器中子源设备研发、注册临床试验推进及第二代硼药国产化生产方面快速发展,多项指标已达国际先进水平。未来,我国需聚焦新型硼药开发、中子源技术优化、联合治疗策略探索以及设备成本降低,以推动BNCT技术的广泛临床应用,为肿瘤患者提供更优质、更经济的治疗选择,同时构建具有国际竞争力的BNCT产业生态。
参考文献 [1] Coderre JA, Morris GM. The Radiation Biology of boron neutron capture Therapy[J]. Radiat Res, 1999, 151(1): 1-18. [2] Chadwick J, Goldhaber M. The nuclear photoelectric effect[J]. Proc R Soc Lond Math Phys Sci, 1935, 151(873): 479-493. [3] 张晓敏, 张文仲, 骆亿生. 硼中子俘获治疗技术的研究现状. 国外医学(放射医学核医学分册), 2004, 28(4): 188-191. [Zhang XM, Zhang WZ, Luo YS. The research status of BNCT technique. Guo Wai Yi Xue (Fang She Yi Xue He Yi Xue Fen Ce), 2004, 28(4): 188-191.] [4] Nakai K, Koivunoro H, Giap H, et al. Minutes of the Meeting of the PTCOG BNCT Subcommittee[C]. PTCOG, 2025, 63. [5] Barth RF, Soloway AH, Brugger RM. Boron Neutron capture therapy of brain tumors: past history, current status, and future potential[J]. Cancer Invest, 1996, 14(6): 534-550. doi: 10.3109/07357909609076899 [6] Mishima Y, Ichihashi M, Hatta S, et al. First human clinical trial of melanoma neutron capture. Diagnosis and therapy[J]. Strahlenther Onkol, 1989, 165(2-3): 251-254. [7] Barth RF, Soloway AH, Fairchild RG. Boron neutron capture therapy for cancer[J]. Sci Am, 1990, 263(4): 100-103,106-107. doi: 10.32388/6qx174 [8] Yokoyama K, Miyatake SI, Kajimoto Y, et al. Pharmacokinetic study of BSH and BPA in simultaneous use for BNCT[J]. J Neurooncol, 2006, 78(3): 227-232. doi: 10.1007/s11060-005-9099-4 [9] Lamba M, Goswami A, Bandyopadhyay A. A periodic development of BPA and BSH based derivatives in boron neutron capture therapy (BNCT)[J]. Chem Commun (Camb), 2020, 57(7): 827-839. doi: 10.1039/d0cc06557a [10] Ono K, Masunaga S, Kinashi Y, et al. The Dose Planning of BNCT for Brain Tumors[C]//Mishima Y. Cancer Neutron Capture Therapy. New York: Plenum Press, 1996: 563-569. [11] Farhood B, Samadian H, Ghorbani M, et al. Physical, dosimetric and clinical aspects and delivery systems in neutron capture therapy[J]. Rep Pract Oncol Radiother, 2018, 23(5): 462-473. doi: 10.1016/j.rpor.2018.07.002 [12] Aihara T, Hiratsuka J, Morita N, et al. BNCT for Head and Neck Cancer—History at our institution—[J]. Pract Otorhinolaryngol Suppl, 2017, 149: 227-240. [13] Fukumitsu N, Matsumoto Y. Development of an imaging technique for Boron Neutron Capture Therapy[J]. Cells, 2021, 10(8): 2135. doi: 10.3390/cells10082135 [14] Skwierawska D, López-Valverde JA, Balcerzyk M, et al. Clinical Viability of Boron Neutron Capture Therapy for Personalized Radiation Treatment[J]. Cancers (Basel), 2022, 14(12): 2865. doi: 10.3390/cancers14122865 [15] ISNCT. Accelerator-based BNCT projects[EB/OL]. [2026-02-22]. https://isnct.net/bnct-boron-neutron-capture-therapy/accelerator-based-bnct-projects-2021/. [16] 王盛, 李志峰, 李海鹏, 等. 硼中子俘获癌症治疗技术研究与应用进展[J]. 西安交通大学学报, 2026: 1-11. [Wang S, Li ZF, Li HP, et al. Advances in Research and Application of Boron Neutron Capture Therapy for Cancer Treatment[J]. Xi'an Jiao Tong Da Xue Xue Bao, 2026: 1-11.] [17] Capala J, Stenstam BH, Sköld K, et al. Boron neutron capture therapy for glioblastoma multiforme: clinical studies in Sweden[J]. J Neurooncol, 2003, 62(1-2): 135-144. doi: 10.1007/BF02699940 [18] Hiratsuka J, Kamitani N, Tanaka R, et al. Boron neutron capture therapy for vulvar melanoma and genital extramammary Paget’s disease with curative responses[J]. Cancer Commun (Lond), 2018, 38(1): 38. doi: 10.1186/s40880-018-0297-9 [19] 程祥. 硼中子俘获治疗: 硼化拉帕替尼的合成与体外评估[J]. 合肥: 安徽医科大学, 2024. [Cheng X. Boron neutron capture therapy: Synthesis and in vitro Evaluation of Boronated-Lapatinib[D]. Hefei: Anhui Medical University, 2024.] [20] Kageji T, Nagahiro S, Matsuzaki K, et al. Boron neutron capture therapy using mixed epithermal and thermal neutron beams in patients with malignant glioma—correlation between radiation dose and radiation injury and clinical outcome[J]. Int J Radiat Oncol Biol Phys, 2006, 65(5): 1446-1455. doi: 10.1016/j.ijrobp.2006.03.016 [21] Kageji T, Mizobuchi Y, Nagahiro S, et al. Clinical results of boron neutron capture therapy (BNCT) for glioblastoma[J]. Appl Radiat Isot, 2011, 69(12): 1823-1825. doi: 10.1016/j.apradiso.2011.05.029 [22] Yamamoto T, Matsumura A, Nakai K, et al. Current clinical results of the Tsukuba BNCT trial[J]. Appl Radiat Isot, 2004, 61(5): 1089-1093. doi: 10.1016/j.apradiso.2004.05.010 [23] Kageji T, Mizobuchi Y, Nagahiro S, et al. Long-survivors of glioblatoma treated with boron neutron capture therapy (BNCT)[J]. Appl Radiat Isot, 2011, 69(12): 1800-1802. doi: 10.1016/j.apradiso.2011.03.021 [24] Burian J, Marek M, Rataj J, et al. Report on the first patient group of the phase Ⅰ BNCT trial at the LVR-15 reactor[J]. Int Congr Ser, 2004, 1259: 27-32. doi: 10.1016/S0531-5131(03)01515-2 [25] Yamamoto T, Nakai K, Kageji T, et al. Boron neutron capture therapy for newly diagnosed glioblastoma[J]. Radiother Oncol, 2009, 91(1): 80-84. doi: 10.1016/j.radonc.2009.02.009 [26] Kato I, Fujita Y, Maruhashi A, et al. Effectiveness of boron neutron capture therapy for recurrent head and neck malignancies [J]. Appl Radiat Isot, 2009, 67(7-8 Suppl): S37-S42. [27] Kawabata S, Miyatake SI, Kuroiwa T, et al. Boron neutron capture therapy for newly diagnosed glioblastoma[J]. J Radiat Res, 2009, 50(1): 51-60. doi: 10.1269/jrr.08043 [28] Shiba H, Takeuchi K, Hiramatsu R, et al. Boron Neutron Capture Therapy Combined with Early Successive Bevacizumab Treatments for Recurrent Malignant Gliomas-A Pilot Study[J]. Neurol Med Chir (Tokyo), 2018, 58(12): 487-494. doi: 10.2176/nmc.oa.2018-0111 [29] Haginomori SI, Miyatake SI, Inui T, et al. Planned fractionated boron neutron capture therapy using epithermal neutrons for a patient with recurrent squamous cell carcinoma in the temporal bone: a case report[J]. Head Neck, 2009, 31(3): 412-418. doi: 10.1002/hed.20895 [30] Koivunoro H, Kankaanranta L, Seppälä T, et al. Boron neutron capture therapy for locally recurrent head and neck squamous cell carcinoma: An analysis of dose response and survival[J]. Radiother Oncol, 2019, 137: 153-158. doi: 10.1016/j.radonc.2019.04.033 [31] Haapaniemi A, Kankaanranta L, Saat R, et al. Boron Neutron Capture Therapy in the Treatment of Recurrent Laryngeal Cancer[J]. Int J Radiat Oncol Biol Phys, 2016, 95(1): 404-410. doi: 10.1016/j.ijrobp.2015.11.010 [32] Wang L, Liu YH, Chou F, et al. Clinical trials for treating recurrent head and neck cancer with boron neutron capture therapy using the Tsing‐Hua Open Pool Reactor[J]. Cancer Commun (Lond), 2018, 38(1): 37. doi: 10.1186/s40880-018-0295-y [33] Takai S, Wanibuchi M, Kawabata S, et al. Reactor-based boron neutron capture therapy for 44 cases of recurrent and refractory high-grade meningiomas with long-term follow-up[J]. Neuro Oncol, 2022, 24(1): 90-98. doi: 10.1093/neuonc/noab108 [34] Igaki H, Murakami N, Nakamura S, et al. Scalp angiosarcoma treated with linear accelerator-based boron neutron capture therapy: A report of two patients[J]. Clin Transl Radiat Oncol, 2022, 33: 128-133. [35] 罗庆有, 朱皓, 吴巧敏. 厦门先行示范: 全球硼中子俘获疗法蓬勃发展[J]. 厦门科技, 2024, 30(5): 14-17. [Luo QY, Zhu H, Wu QM. Xiamen Pilot Demonstration: Booming Development of Global Boron Neutron Capture Therapy[J]. Xiamen Ke Ji, 2024, 30(5): 14-17.] Luo QY, Zhu H, Wu QM. Xiamen Pilot Demonstration: Booming Development of Global Boron Neutron Capture Therapy[J]. Xiamen Ke Ji, 2024, 30(5): 14-17. [36] Hong J, Liu YH, Zhu X, et al. Boron Neutron Capture Therapy as a Novel Approach for Chondrosarcoma: Case Study of Tumor Reduction and Long-term Control[J]. Adv Radiat Oncol, 2025, 10(11): 101897. doi: 10.1016/j.adro.2025.101897 [37] Zhang Z, Chong Y, Liu Y, et al. A review of planned, ongoing clinical studies and recent development of BNCT in mainland of China[J]. Cancers (Basel), 2023, 15(16): 4060. doi: 10.3390/cancers15164060 [38] Li L, Li J, Shi Y, et al. On-Demand Biodegradable Boron Nitride Nanoparticles for Treating Triple Negative Breast Cancer with Boron Neutron Capture Therapy[J]. ACS Nano, 2019, 13(12): 13843-13852. doi: 10.1021/acsnano.9b04303 [39] Gao J, Hu J, Guan X, et al. Salvage Carbon-Ion radiation therapy for locoregionally recurrent head and neck malignancies[J]. Sci Rep, 2019, 9(1): 4259. doi: 10.1038/s41598-019-39241-y [40] 洪俊强, 林小艺, 赖友群, 等. 硼中子俘获疗法治疗复发恶性肿瘤的安全性和有效性研究[J]. 中华放射肿瘤学杂志, 2025, 34(10): 985-992. [Hong JQ, Lin XY, Lai YQ, et al. The safety and efficacy of boron neutron capture therapy(BNCT)in the treatment of recurrent malignant tumors[J]. Zhonghua Fang She Zhong Liu Xue Za Zhi, 2025, 34(10): 985-992.] doi: 10.3760/cma.j.cn113030-20250517-00194 [41] Matsumura A, Asano T, Hirose K, et al. Initiatives Toward Clinical Boron Neutron Capture Therapy in Japan[J]. Cancer Biother Radiopharm, 2023, 38(3): 201-207. [42] 何静, 汤晓斌, 刘渊豪, 等. 硼中子俘获治疗头颈部肿瘤临床试验进展[J]. 中华放射医学与防护杂志, 2020, 40(8): 642-647. [He J, Tang XB, Liu YH, et al. Progress in clinical trials of boron neutron capture therapy of head and neck cancers[J]. Zhonghua Fang She Yi Xue Yu Fang Hu Za Zhi, 2020, 40(8): 642-647.] [43] 刘志凯, 程炜诗, 吴王锁, 等. 硼中子俘获疗法的原理及临床应用[J]. 协和医学杂志, 2023, 14(4): 698-705. [Liu ZQ, Cheng WS, Wu WS, et al. Principles and Clinical Applications of Boron Neutron Capture Therapy[J]. Xie He Yi Xue Za Zhi, 2023, 14(4): 698-705.] doi: 10.12290/xhyxzz.2023-0120 [44] Kim W, Park JS, Song JH, et al. Boron Neutron Capture Therapy in Recurrent High-Grade Gliomas: Safety, Efficacy, and Pharmacokinetics From a Multicenter, Dose-Escalation Phase 1 Trial[J]. Adv Radiat Oncol, 2026, 11(1): 101947. doi: 10.1016/j.adro.2025.101947 [45] Hirose K, Sato M. Clinical Results and Prognostic Factors in Boron Neutron Capture Therapy for Recurrent Squamous Cell Carcinoma of the Head and Neck Under the Japan National Health Insurance System: A Retrospective Study of the Initial 47 Patients[J]. Int J Radiat Oncol Biol Phys, 2024, 120(3): 796-804. doi: 10.1016/j.ijrobp.2024.03.041 [46] Porra L, Wendland L, Seppälä T, et al. From Nuclear Reactor-Based to Proton Accelerator-Based Therapy: The Finnish Boron Neutron Capture Therapy Experience[J]. Cancer Biother Radiopharm, 2023, 38(3): 184-191. doi: 10.1089/cbr.2022.0059 [47] 周贝霖, 胡石林. 硼同位素分离研究进展[J]. 化学工程与技术, 2023, 13(3): 161-173. [Zhou BL, Hu SL. Research Progress in Boron Isotope Separation[J]. Hua Xue Gong Cheng Yu Ji Shu, 2023, 13(3): 161-173.] [48] Li X, He P, Wei Y, et al. Application and perspectives of nanomaterials in boron neutron capture therapy of tumors[J]. Cancer Nanotechnol, 2025, 16(1): 25. doi: 10.1186/s12645-025-00324-3 [49] Wu CY, Hsieh HH, Chang TY, et al. Development of MRI-Detectable Boron-Containing Gold Nanoparticle-Encapsulated Biodegradable Polymeric Matrix for Boron Neutron Capture Therapy (BNCT)[J]. Int J Mol Sci, 2021, 22(15): 8050. doi: 10.3390/ijms22158050 [50] Chen J, Yang Q, Liu M, et al. Remarkable Boron Delivery of iRGD-Modified Polymeric Nanoparticles for Boron Neutron Capture Therapy[J]. Int J Nanomedicine, 2019, 14: 8161-8177. doi: 10.2147/IJN.S214224 [51] Shukla S, Wu G, Chatterjee M, et al. Synthesis and biological evaluation of folate receptor-targeted boronated PAMAM dendrimers as potential agents for neutron capture therapy[J]. Bioconjug Chem, 2003, 14(1): 158-167. doi: 10.1021/bc025586o [52] Wu J. The Enhanced Permeability and Retention (EPR) Effect: The Significance of the Concept and Methods to Enhance Its Application[J]. J Pers Med, 2021, 11(8): 771. doi: 10.3390/jpm11080771 [53] Shi Y, Li J, Zhang Z, et al. Tracing Boron with Fluorescence and Positron Emission Tomography Imaging of Boronated Porphyrin Nanocomplex for Imaging-Guided Boron Neutron Capture Therapy[J]. ACS Appl Mater Interfaces, 2018, 10(50): 43387-43395. doi: 10.1021/acsami.8b14682 [54] Barth RF, Mi P, Yang W. Boron delivery agents for neutron capture therapy of cancer[J]. Cancer Commun (Lond), 2018, 38(1): 35. doi: 10.1186/s40880-018-0299-7 [55] 山西医科大学. 基于硼中子俘获治疗的富硼纳米制剂及其制备方法: CN202211140524.1[P]. 2023-01-17. [Shanxi Medical University. Boron-Rich Nanoformulations Based on Boron Neutron Capture Therapy and Their Preparation Methods: CN202211140524.1[P]. 2023-01-17.] [56] Das BC, Chokkalingam P, Masilamani P, et al. Stimuli-Responsive Boron-Based Materials in Drug Delivery[J]. Int J Mol Sci, 2023, 24(3): 2757. doi: 10.3390/ijms24032757 [57] Sauerwein WAG, Sancey L, Hey-Hawkins E, et al. Theranostics in Boron Neutron Capture Therapy[J]. Life (Basel), 2021, 11(4): 330. doi: 10.3390/life11040330 [58] Flieger S, Takagaki M, Kondo N, et al. Carborane-Containing Hydroxamate MMP Ligands for the Treatment of Tumors Using Boron Neutron Capture Therapy (BNCT): Efficacy without Tumor Cell Entry[J]. Int J Mol Sci, 2023, 24(8): 6973. doi: 10.3390/ijms24086973 [59] Trivillin VA, Langle YV, Palmieri MA, et al. Evaluation of local, regional and abscopal effects of Boron Neutron Capture Therapy (BNCT) combined with immunotherapy in an ectopic colon cancer model[J]. Br J Radiol, 2021, 94(1128): 20210593. doi: 10.1259/bjr.20210593 [60] Fujimoto T, Yamasaki O, Kanehira N, et al. Overcoming immunotherapy resistance and inducing abscopal effects with boron neutron immunotherapy (B-NIT)[J]. Cancer Sci, 2024, 115(10): 3231-3247. doi: 10.1111/cas.16298 [61] Sun Q, Zhao Y, Qiao S, et al. Boron neutron capture therapy preserves immune cells and induces robust anti-tumour immunity in preclinical mouse model[J]. Nat Commun, 2026, 17(1): 1229. doi: 10.1038/s41467-025-67984-y [62] Ma W, Wang Y, Xue Y, et al. Molecular engineering of AIE-active boron clustoluminogens for enhanced boron neutron capture therapy[J]. Chem Sci, 2024, 15(11): 4019-4030. doi: 10.1039/D3SC06222H [63] Monti Hughes A, Hu N. Optimizing Boron Neutron Capture Therapy (BNCT) to Treat Cancer: An Updated Review on the Latest Developments on Boron Compounds and Strategies[J]. Cancers (Basel), 2023, 15(16): 4091. doi: 10.3390/cancers15164091 [64] Kaniowski D, Suwara J, Ebenryter-Olbińska K, et al. EGFR-Targeted Cellular Delivery of Therapeutic Nucleic Acids Mediated by Boron Clusters[J]. Int J Mol Sci, 2022, 23(23): 14793. doi: 10.3390/ijms232314793 [65] Cheng X, Li F, Liang L. Boron Neutron Capture Therapy: Clinical Application and Research Progress[J]. Curr Oncol, 2022, 29(10): 7868-7886. doi: 10.3390/curroncol29100622
来源:《肿瘤防治研究》官网