预防性人乳头瘤病毒疫苗中国临床应用指南(2025 版)
中华医学会妇科肿瘤学分会 中国优生科学协会阴道镜和宫颈病理学分会 中华预防医学会肿瘤预防与控制专委会 中国妇幼健康研究会子宫颈癌防控研究专委会 中国癌症基金会全国子宫颈癌防治协作组 中国抗癌协会子宫颈癌专委会 中国医疗保健国际交流促进会妇产健康医学分会
基金项目:国家重点研发计划(2021YFC2701202,2021YFC2701203)
通信作者:
孔北华 Email: kongbeihua@yahoo.com.cn;
马 丁 Email: dma@tjh.tjmu.edu.cn;
魏丽惠 Email: weilhpku@163.com
【摘要】预防性人乳头瘤病毒(human papilloma virus, HPV)疫苗接种是预防 HPV 感染的有效方法,可降低 HPV 感染相关疾病的发生。目前国内外临床试验及真实世界研究均表明,预防性 HPV 疫苗是安全的,具有很好的免疫原性、保护效力和保护效果。优先推荐 9 ~ 26 岁女性接种 HPV 疫苗,重点是 9 ~ 14 岁女孩;同时推荐 27 ~ 45 岁女性和 9 ~ 26 岁男性接种,倡导男女共防。对于 HPV 感染或细胞学异常人群、HPV 相关病变治疗史人群、遗传易感人群、子宫颈癌发病高风险生活方式人群,以及免疫功能低下人群均推荐预防性 HPV 疫苗接种。接种 HPV 疫苗后仍应定期进行子宫颈癌筛查。
【关键词】人乳头瘤病毒;疫苗;临床应用;高风险;特殊人群
预防性人乳头瘤病毒(human papilloma virus, HPV)疫苗接种是通过预防 HPV 感染,进而预防 HPV 相关病变及肿瘤的一级预防措施。随着 HPV 疫苗接种全球数据的更新,中华医学会妇科肿瘤学分会、中国优生科学协会阴道镜和宫颈病理学分会等七个学会在上一版《人乳头瘤病毒疫苗临床应用中国专家共识》[1] 的基础上,依据循证医学证据及我国国情和临床实际,制定了此《预防性人乳头瘤病毒疫苗中国临床应用指南(2025 版)》。本指南推荐类别见表 1。

1. HPV 基因型别和分类
HPV 是一种嗜上皮组织的无包膜双链环状 DNA 病毒,由病毒蛋白衣壳和核心单拷贝的病毒基因组 DNA 构成,病毒衣壳由主要衣壳蛋白 L1 和次要衣壳蛋白 L2 组成 [2]。HPV 主要通过性行为或皮肤黏膜接触传播。在有异性伴侣的人群中,女性一生中感染 HPV 的概率为 84.6%,男性为 91.3% [3]。HPV 型别根据致癌潜力分为高危型(high-risk, HR)HPV 和低危型(low-risk, LR)HPV。HR-HPV主要包括14种HPV 16/18/31/33/35/39/45/51/52/56/58/59/66/68,其中HPV 16 风险最高,可引起子宫颈、阴道、外阴、肛门、阴茎、头颈等部位的 HPV 相关癌前病变及肿瘤的发生。LR-HPV 以 HPV 6/11 为主,可引起肛门生殖器疣(anogenital warts, AGW) 和 复 发 性 呼 吸 道 乳 头 状 瘤(recurrent respiratory papillomatosis, RRP)等 [2, 4]。
2. HPV 感染率和基因型别分布
(1)女性 HPV 感染情况:全球范围内 HPV 感染型别在不同地区、不同年龄、不同人群中分布不同 [5]。一项纳入全球 194 项研究共 1 016 719 名女性的荟萃分析显示,子宫颈细胞学正常人群中 HPV 感染率为 11.7% [6]。我国大陆女性人群 HPV 总感染率在 15.5% ~ 24.3%,不同地区、不同人群 HPV 感染率存在差异 [7-10]。我国 9 个省市17 项以人群为基础的 30 207 名女性子宫颈癌筛查数据显示,HPV 感染率呈现两个年龄高峰,分别在 17 ~ 24 岁和40 ~ 45 岁 [11]。我国子宫颈细胞学正常女性中最常见的 5 种HPV 型别是 HPV 52(2.8%)、HPV 16(2.7%)、HPV 58(1.7%)、HPV 18(1.1%)和 HPV 33(1.1%)[12]。
HPV 阳性率和子宫颈上皮内病变级别相关。在子宫颈细胞学结果为无明确意义的非典型鳞状上皮细胞(atypical squamous cells of undetermined significance, ASC-US)的女性中 HPV 感染率为 52%,在低级别鳞状上皮内病变(lowgrade squamous intraepithelial lesion, LSIL)中为 76%, 在高级别鳞状上皮内病变(high-grade squamous intraepitheliallesion, HSIL)中高达 85 % [13]。HPV 16、33、58、52 的感染率,鳞癌(56.8%、4.3%、3.9%、3.7%)高于腺癌(36.1 %、1.8 %、1.1 %、1.3 %);而 HPV 18、45 的感染率,腺癌(34.9%、5.7%)高于鳞癌(11.6%、4.8%)[5]。我国子宫颈上皮内病变患者 HPV 总感染率为 84.4%,其中 子 宫 颈 上 皮 内 瘤 变(CIN)1 和 CIN2/3 分别为 79.6%和 87 % [14]。我国 LSIL 患 者 HPV 感染常见型别依次是HPV 52/16/58/18/33;HSIL 患 者 HPV 感染常见型别依次 是 HPV 16/52/58/33/18;而子宫颈癌患者中则依次是HPV 16/18/58/52/33[12]。
(2)男性 HPV 感染情况:一项纳入全球 65 项研究,涵盖 35 个国家共 44 769 名 15 岁及以上男性的荟萃分析显示,全球男性任意型别 HPV 的总体感染率为 31%,HR-HPV 的感染率为 21%。HPV-16 是最常见的 HPV 基因型(5%, 95% CI: 4%~7%),其次是 HPV 6(4%, 95% CI: 3%~5%)[15]。我国男性普通人群 HPV 总体感染率为 8.0% ~16.9%,其中HR-HPV 感染率为 5.5% ~9.4% [16]。
(3)特殊人群 HPV 感染情况:一项全球荟萃分析发现,子宫颈细胞学正常的人类免疫缺陷病毒(human immunodeficiency virus, HIV)感染人群中 HR-HPV 感 染率为 51%,各地区差异较大。最常见的高危型别为 HPV 16/18/52[17]。我国 HIV 感染女性的子宫颈 HR-HPV 感染率为30.6%(最常见为 HPV 52/16/58),肛门 HR-HPV 为 30.3%,(最常见为 HPV 52/53/39)[18]。HIV 阳性(HIV+)女性子宫颈癌风险是 HIV 阴性(HIV-)女性的 6 倍(RR=6.07)。全球 2018 年新发子宫颈癌病例中, 有 5.8% 为 HIV+ 女性,4.9%的病例可归因于 HIV 感染 [19]。关于男 - 男性行为者(men who have sex with men, MSM),在一项纳入 64 项研究共 29 900 名男性中,HIV 阳性 MSM 人群中 HPV 感染率(74.3%)高于 HIV 阴性 MSM 人群(41.2%)[20]。MSM 人群不同部位 HPV 感染率由高至低依次为肛门、阴茎、尿道。肛门最常见高危型依次为 HPV 16、51、18、52 和 58 型 [21]。
3. HPV 相关疾病负担
(1)子 宫 颈 癌:2022 年全球子宫颈癌新发病例66.10 万,死亡病例 34.82 万,分别位居所有肿瘤的第 8 位和第 9 位 [22]。2022 年中国子宫颈癌新发病例 15.07 万,死亡病例 5.57 万,位居我国女性恶性肿瘤新发和死亡的第 5位和第 6 位 [23]。在我国 15~49 岁女性中,子宫颈癌新发和死亡分别处于第 3 位和第 2 位 [22],与 1990 年相比,2019 年我国女性 40~44 岁年龄组发病率增幅最大,高达 73.1% [24]。
(2)其他 HPV 相关肿瘤:据估计,HPV 感染与全球约4.5%的癌症新发病例有关 [25]。在中国,女性可归因于 HPV感染的肿瘤标化发病率排序依次为子宫颈癌、肛门癌、阴道癌、外阴癌、口咽癌、口腔癌、喉癌。男性发病率依次为阴茎癌、肛门癌、口咽癌、喉癌、口腔癌,并呈上升趋势 [26]。
(3)低危型 HPV 感染相关疾病:全球 AGW 的年发病率估计为 194.5/10 万 [27]。我国一项前瞻性研究显示一般人群中 AGW 发病率约为 126/10 万,12 个月自我报告发病率约为 235/10 万 [28]。RRP 主要由 LR-HPV 6/11 感染上呼吸道致病,分为幼年型 RRP 和成人型 RRP,据估计 RRP 患病率为0.75~4/10 万 [29]。目前我国尚缺乏 RRP 流行病学调查数据。
1. 预防性 HPV 疫苗的免疫机制
(1) HPV 感染与免疫逃逸:机体感染 HPV 后,产生针对 HPV 的特异性免疫反应,包括细胞免疫和抗体介导的体液免疫 [2]。由于 HPV 感染仅存在于黏膜上皮层,不会引起全身强烈的免疫反应。感染 HPV 后,70% ~ 80%的女性会发生血清中和抗体阳转,但是产生的抗体增长缓慢,效价和亲和力不高。从 HPV 感染至血清中和抗体阳转的中位数时间为 8 ~ 12 个月 [4]。由于女性自身无法引起有效的细胞免疫来清除病毒,导致持续 HR-HPV 感染的患者更有可能进展为子宫颈癌前病变 [4]。
(2) 预防性 HPV 疫苗的作用机制:预防性 HPV 疫苗是利用基因重组的方法将 HPV L1 基因装配在不同的表达系统(如酿酒酵母、杆状病毒 - 昆虫细胞、大肠杆菌或毕赤酵母等)中,使其表达 HPV L1 结构蛋白,并组装为HPV 病毒样颗粒(virus-like particles, VLP),辅以佐剂得到可诱导机体产生特异性抗体的 HPV 疫苗。VLP 抗原活性几乎与天然的病毒完全一致。由于 HPV 疫苗不含病毒DNA,所以不具有感染性和致癌性。HPV 疫苗主要通过诱导机体产生能与病毒颗粒结合的中和抗体来发挥作用,从而预防 HPV 感染 [4, 30]。
2. HPV 疫苗的有效性评价
疫苗的有效性评价包括免疫原性(immunogenicity)、保护效力(efficacy)和保护效果(effectiveness)。① 免疫原性:是指疫苗抗原诱导机体产生适应性免疫反应的能力,主要包括体液免疫和细胞免疫,其中体液免疫通常采用疫苗接种后免疫应答率(包括抗体阳转率等)和抗体几何平均滴度(geometric mean titer, GMT)/ 几何平均浓度(geometric mean concentration, GMC)及其增长倍数作为评价指标。② 保护效力:指在接种人群中由接种疫苗诱导的保护作用,是评价HPV 疫苗有效性的直接证据和金标准。CIN2/CIN3 和原位腺癌(AIS)分别是子宫颈鳞癌和腺癌的癌前病变,是 HPV 疫苗Ⅲ期临床试验的终点指标,而 HPV 持续感染是为缩短迭代疫苗获批时间设置的指标 [31]。③ 保护效果:是指对 HPV疫苗接种所产生保护作用的估计,既包括直接保护,也包括间接保护(即疫苗对未接种人群的保护),一般是通过在特定人群常规接种疫苗后监测疫苗所预防疾病来衡量。HPV疫苗在真实人群中的保护效果一般是通过上市后监测,可通过试验研究或收集地区及国家数据进行评估。
2.1 HPV 疫苗的免疫原性
(1)双价 HPV 疫苗:我国临床研究表明,三种双价HPV 疫苗接种 3 剂次后 1 个月,HPV 16/18 型血清中和抗体阳转率均在 97.5% ~100.0% ;9~17 岁女性 HPV 16/18 型血清中和抗体 GMT 在数值上均高于 18~25 岁女性;9~14 岁女性 2 剂次接种后 HPV 16/18 抗体阳转率均达 100%,抗体水平非劣于 18~26 岁女性接种 3 剂次者 [32-34]。另外两项双价吸附 HPV 疫苗在接种后 5 年和 12 年的随访研究显示,HPV 16 和 HPV18 抗体水平显著,且保持稳定 [35-36]。
(2)四价 HPV 疫苗:9~45 岁女性和男性接种 3 剂次四价 HPV 疫苗后 1 个月,疫苗所含 HPV 型别的血清阳转率 达 96.7%~99.3%,9~15 岁女孩和男孩抗体 GMT 可 达16~26 岁女性的 1.4~2.8 倍 [37]。9~13 岁女性接种 2 剂 次的 GMT 非劣效于 16~26 岁女性接种三剂次(疫苗说明书)。16~26 岁男性接种首剂 HPV 疫苗后 7 个月时血清阳转率为97.4%~99.2%,至 36 个月时血清阳转率为 57.0%~97.9%[38];27~45 岁男性接种四价 HPV 疫苗后均发生了中和抗体阳转,与 16~26 岁年轻男性的免疫应答相似 [39]。
(3)九价 HPV 疫苗:9 ~ 45 岁女性完成 3 剂次九价HPV 疫苗接种后 1 个月,疫苗所含 HPV 型别的血清阳转率均 >99%;其中 9 ~ 19 岁组的抗体 GMT 非劣效于20 ~ 26 岁组;27 ~ 45 岁组疫苗所含 HPV 型别的血清阳转率非劣效于 20 ~ 26 岁组 [40]。9 ~ 14 岁女孩接种 2 剂次血清阳转率和抗体 GMT 非劣效于接种 3 剂的 16 ~ 26 岁年轻女性 [41]。9 ~ 15 岁男孩接种 3 剂次疫苗后中和抗体 GMT 显著高于接种 3 剂次的成年女性 [42],接种 2 剂次疫苗的男孩诱导免疫原性非劣效于接种 3 剂次的成年女性 [41]。
2.2 HPV 疫苗的保护效力
(1)国产双价 HPV 疫苗(大肠杆菌):对 18~45 岁女性 6 个月和 12 个月的持续感染的保护效力分别为 97.7%、95.3%(疫苗说明书)。经 66 个月随访,对 18~45 岁女性HPV16/18 感染相关的高级别病变的保护效力为 100.0%[43-44]。
(2)国产双价 HPV 疫苗(毕赤酵母):18~30 岁中国女性随访 48 个月的结果显示,对 HPV 16/18 相关的 CIN 2+的保护效力为 78.6%(疫苗说明书)。
(3)双价 HPV 吸 附 疫 苗:在 15~25 岁女性未感染过 HPV 人 群, 对 HPV 引起的 CIN3 或 AIS 的保护效力为93.2%,对符合方案集人群的 HPV16/18 相关的 CIN2 级及以上(CIN2+)的保护效力为 94.9%;对 6 个月和 12 个月持续性感染的保护效果分别为 92.9%、94.3%(疫苗说明书)[45]。中国Ⅲ期临床试验随访 72 个月结果显示,在基线 HPV 阴性人群,双价 HPV 吸附疫苗对 HPV 16/18 相关 CIN2+ 的保护效力为 100%,对 6 个月和 12 个月持续性感染的保护效力分别为 96.3% 和 96.7%[46]。
(4)四价 HPV 疫 苗:在 16~24 岁符合方案集女性中对 HPV6/11/16/18 型相关任意级别外生殖器和阴道病变终点的保护效力均为 100%[47]。中国Ⅲ期临床试验随访 78个 月 结 果 显 示, 对 HPV 16/18 相 关 CIN2+、CIN1+ 的保护效力均高达 100% [48]。一项全球多中心、随机、双盲、安慰剂对照的Ⅲ期临床试验 16 ~ 26 岁男性随访 36 个月对 HPV6/11/16/18 相关外生殖器病变终点的保护效力为90.4%,对外生殖器部位 HPV 6/11/16/18 持续感染(6 个月及以上)的保护效力为 85.6% [49]。
(5) 九 价 HPV 疫 苗:对 16~26 岁女性的 HPV 6/11/16/18 相关的持续感染、子宫颈癌前病变及癌的保护效力与四价 HPV 相 当, 对 HPV 31/33/45/52/58 型别相关的 6 个月持续感染保护效力为 96.0%,12 个月持续感染保护效力为 96.7%,对 CIN1+ 的保护效力为 98.2% [50]。在16 ~ 26 岁东亚女性观察到相似的结果,九价 HPV 疫苗对HPV 31/33/45/52/58 型别相关 6 个月和 12 个月持续感染、CIN1+ 的保护效力分别为 95.8%、93.9%和 100% [51]。
2.3 HPV 疫苗的保护效果
2.3.1 临床试验长期随访研究的保护效果
(1)双价 HPV 疫苗:双价 HPV 吸附疫苗 15~25 岁女性接种 3 剂次长达 9.4 年的随访研究结果显示,对 HPV16/18 相关的偶发感染、6 个月持续感染、12 个月持续感染和 CIN2+的保护效果分别为 95.6%、100%、100%和 100% [52]。对18~25 岁女性随访 11 年的哥斯达黎加疫苗试验发现,双价HPV 吸附疫苗对 HPV 16/18 相关 CIN2+ 和CIN3+ 的保护效果分别为 97.4%和 94.9% [53]。
(2)四价 HPV 疫苗:北欧四国 16 ~ 23 岁女性接种四价 HPV 疫苗后长达 14 年的随访研究显示,疫苗的保护效果为 100%[54]。中国 20 ~ 45 岁女性接种 3 剂四价 HPV 疫苗后随访 11 年结果显示,对 HPV 16/18 相关 CIN2+ 的保护效果达 100% [55]。对 16 ~ 26 岁男性早期接种组在首剂接种后中位随访 9.5 年,补种疫苗组中位随访 4.7 年,均未观察到 HPV 6/11 相关的外生殖器尖锐湿疣或与 HPV 6/11/16/18相关的外生殖器病变 [56]。
(3)九价 HPV 疫苗:9~15 岁女孩接种 3 剂后随访 11年,未发生与九价型别相关 CIN2+ 的病例 [57]。在 16~26 岁女性接种 3 剂后长达 12 年的随访未发生 HPV 16/18/31/33/45/52/58 型相关 CIN2+ 的病例,保护效果达 100% [58]。
2.3.2 上市后在真实世界研究中的保护效果
在疫苗上市后,对全球接种双价 HPV 吸附疫苗或四价 HPV 疫苗真实世界研究进行的系统性综述和荟萃分析,以及多国的真实世界研究显示良好的保护效果。
(1)预 防 HPV 感 染:一 项 对 全 球 HPV 疫 苗(双 价HPV 吸附疫苗或四价 HPV 疫苗)真实世界研究,接种疫苗 5~8 年后,13 ~ 19 岁女性 HPV 16/18 型感染率显著降低83%,HPV 31/33/45 型感染率显著降低 54% ;20 ~ 24 岁女性 HPV 16/18 型感染率显著降低 66% [59]。英国、美国等真实世界研究结果也显示,接种 HPV 疫苗后,疫苗相关型别HPV 感染率下降,在年轻女性尤为显著 [60-61]。
(2)预防子宫颈上皮内病变:15 ~ 19 岁女性接种 HPV疫苗 5~9 年后,CIN2+ 发病率下降 51%,20 ~ 24 岁女性CIN2+ 发病率下降 31% [59]。苏格兰真实世界研究结果发现,疫苗接种后 CIN2+ 发病率下降了 88%,CIN3+ 发病率下降 89% [62]。英格兰 [63] 等真实世界研究均显示,接种HPV 疫苗后 CIN2+ 发病率明显降低。
(3)预防子宫颈癌:苏格兰真实世界研究发现,对于12 ~ 13 岁女性进行双价 HPV 吸附疫苗接种后 11 年,预防子宫颈癌的保护效果为 100% [64]。瑞典 167 万 10 ~ 30 岁女性的真实世界研究显示,至少接种 1 剂四价 HPV 疫苗,显著降低子宫颈浸润癌发生率达 63%,其中 17 岁前接种疫苗的女性子宫颈癌发生率下降 88%,17 ~ 30 岁接种的女性下降 53% [65]。英格兰、苏格兰、美国等国的真实世界研究显示,接种疫苗后,子宫颈癌发病率显著降低,在年轻女性尤为显著 [63-66]。
(4)预防肛门生殖器疣:全球多国真实世界研究显示,无论女性或男性接种四价或九价 HPV 疫苗后均有效预防 AGW[59, 67-69]。
1. 我国现有的 HPV 疫苗
截止 2025 年 1 月,我国国家药品监督管理局已批准上市 5 种 HPV 疫苗:国产双价 HPV 疫苗(大肠杆菌)、国产双价 HPV 疫苗(毕赤酵母)、双价 HPV 吸附疫苗(杆状病毒)、四价和九价 HPV 疫苗(酿酒酵母),见表 2。
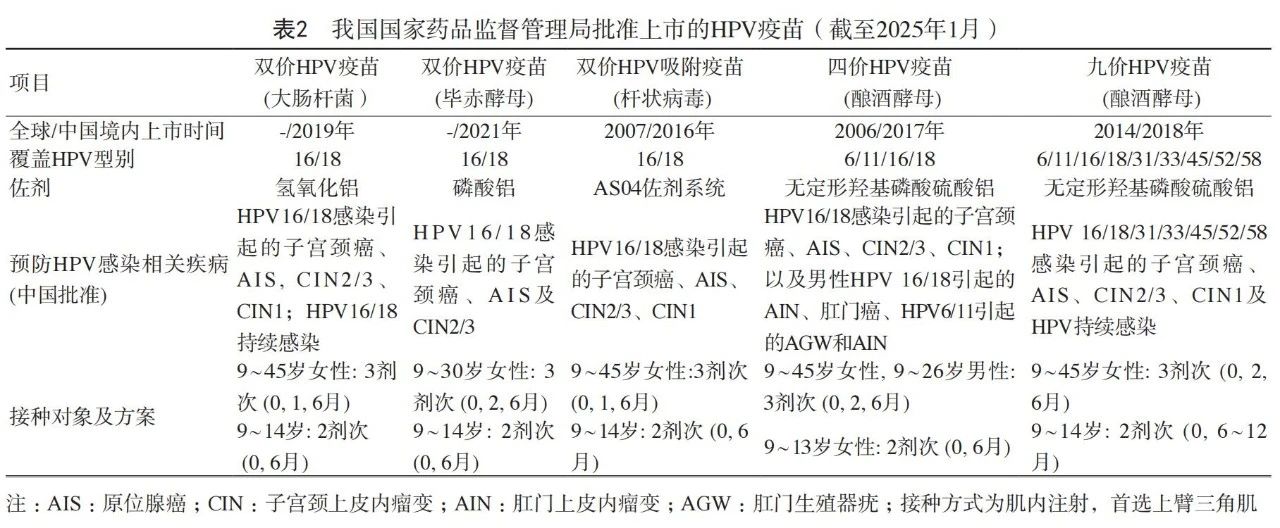
目前,HPV 疫苗在我国属于非免疫规划疫苗(第二类疫苗),接种机构应遵照《中华人民共和国疫苗管理法》、《非免疫规划疫苗使用指导原则》和《预防接种工作规范》的要求,按照疫苗说明书和“知情同意、自愿自费”原则,科学告知受种者或其家长后,为受种者及时提供疫苗接种。
2. 一般人群 HPV 疫苗接种
2.1 国外指南关于 HPV 疫苗接种的推荐
WHO 在 2022 年 12 月更新的立场文件中建议应将HPV 疫苗纳入国家免疫规划,9~14 岁未发生性生活的女孩作为主要目标人群,≥15 岁的女性、男孩、大年龄男性和 MSM 为次要目标人群 [4]。美国疫苗免疫实践咨询委员会(Advisory Committee on Immunization Practices, ACIP)建议女孩和男孩在 11 岁或 12 岁开始接种 HPV 疫苗,最早也可从 9 岁开始接种 [70]。欧洲癌症组织(European Cancer Organisation, ECO)建议,将男孩和女孩纳入常规免疫接种计划,并在此基础上扩大到更大年龄组;至少在 26 岁之前,接种 HPV 疫苗可以预防新发感染或再感染,并阻断 HPV向新的性伴侣传播 [71]。根据 WHO 公布的 2023 年 HPV 疫苗接种率的数据,全球 15 岁女性接种首剂和全部剂次的比例为 20%和 15%,15 岁男性接种首剂和全部剂次的比例为7%和 5%。高收入国家女性首剂接种率为 56%,完成全部免疫剂次的比例为 47% ;中低收入国家女性首剂接种率为16%,完成全部免疫剂次的比例为 13% [72]。
2.2 我国关于一般人群 HPV 疫苗接种的推荐
在中国年轻女性群体中,呈现性行为年龄提前和有高危性行为的趋势。据调查 15~19 岁年龄组中,女性初次性行为中位年龄为 17 岁,20~24 岁年龄组中为 19 岁;城市和农村 15~19 岁女性中已有性生活的比例为 4.5%和 10.8%,在20~24 岁女性中增加至 62.2%和 44% [73]。临床试验研究显示9~15 岁的女性接种 HPV 疫苗后的抗体滴度明显高于 16~26岁女性 [33-34, 37, 40-41]。真实世界研究也显示,17 岁之前接种HPV 疫苗,浸润性子宫颈癌发病率降低 88% [65]。因此,女性在首次性行为前接种 HPV 疫苗获益显著。考虑我国国情、成本效益、受众接受度、组织管理可操作性及可行性,在我国有条件提供免费接种的地区,建议将 13~14 岁女孩作为HPV 疫苗接种的优先推荐人群 [30]。
我国 25 ~ 45 岁女性 HR-HPV 感染率高达 19.9% [8]。随着年龄增长,激素水平和免疫力下降,HPV 感染不易转阴,出现反复感染或持续感染的概率增加,也更容易进展为子宫颈癌前病变和癌 [10]。研究显示,27 ~ 45 岁女性,接种双价、四价和九价 HPV 疫苗诱导的血清抗体阳转率和抗体滴度非劣于 16 ~ 26 岁女性 [34, 37, 40, 74]。因此,27 ~ 45 岁女性接种 HPV 疫苗仍可获益。结合我国女性 HR-HPV 感染流行病学特点、我国 HPV 接种率不足和子宫颈癌筛查覆盖率低的现状,个体化接种策略是必要的。2025 年 1 月 2 日我国国家药监局正式批准四价 HPV 疫苗可用于 9 ~ 26 岁男性。
推荐意见:优先推荐 9 ~ 26 岁女性接种 HPV 疫苗,重点是 9 ~ 14 岁女孩(推荐类别:1 类);推荐 27 ~ 45 岁有条件的女性接种 HPV 疫苗(推荐类别:2A 类)。推荐 9-26 岁男性接种 HPV 疫苗(推荐类别:2A 类)。
1. HPV 感染或细胞学异常人群
HPV 疫苗对既往感染过 HPV(一过性或持续性 HPV感染)的女性具有显著保护效果。研究显示,在 18~25 岁感染非疫苗型 HR-HPV 的中国女性中,双价 HPV 吸附疫苗对 HPV 16/18 相关 6 个月和 12 个月持续感染的保护效力均为100% [75];在 HPV 16/18 血清学阳性的 15~25 岁女性中,该疫苗对 HPV16/18 相关 CIN1+ 的保护效力 67.2%[76]。四价 HPV疫苗在 16~26 岁既往感染疫苗型别 HPV(血清 HPV 抗体阳性而子宫颈 HPV DNA 阴性)的女性中,对疫苗型别 HPV 再感染或其他未感染疫苗型别 HPV 所致 CIN1+ 的保护效力达100%[77]。对 24~45 岁既往感染疫苗型别 HPV 的女性,四价HPV 疫苗对 HPV 16/18 相关 CIN1+ 的保护效力为 66.9% [78]。九 价 HPV 疫苗对 16~26 岁正在感染 HPV 疫苗相关型别的女性,对疫苗型别中未感染的其它型别所致的 CIN 2+的保护效力在 91.1% ~95.8%之间 [79]。另外,HPV 疫苗对细胞学异常女性同样具有较高保护效力。一项纳入约 1.4 万例 16~26 岁年轻女性的多中心 RCT 显示,在初始细胞学异常女性中,九价 HPV 疫苗对 HPV 31/33/45/52/58 相关 6 个月持续感染的保护效力为 94.6% [50]。
推荐意见:无论是否存在 HPV 感染或细胞学异常,推荐适龄女性接种 HPV 疫苗。(推荐类别:2A 类)。
2. HPV 相关病变治疗史人群
2.1 子宫颈癌前病变 / 癌治疗史人群
既往下生殖道 HSIL 的女性,治疗后可能再次发生HPV 感染,或感染持续存在,或疾病复发 [80]。一项纳入 18项研究的荟萃分析显示,接种 HPV 疫苗使 CIN2+ 复发风险降低 57%,尤其 HPV 16/18 相关 CIN2+ 复发风险降低74%[81]。PATRICIA 研究的事后分析表明,对 15~45 岁女性,无论 HPV DNA、HPV 16/18 血清学或子宫颈细胞学检测结果如何,术前接种双价 HPV 疫苗后再接受切除性治疗,随访 4 年中可见术后 CIN2+ 复发风险降低 88.2% [82]。意大利一项前瞻性随机对照试验显示,23~44 岁既往有子宫颈鳞状上皮内病变治疗史的女性,与未接种者相比,接种四价 HPV 疫苗可显著降低 HPV 相关病变复发风险(3.4%vs 13.5% , P =0.0279)[83]。一项中国前瞻性队列研究显示,20~45 岁 CIN2/3 女性接受子宫颈环形电切术(LEEP)术后随访 30 个月,与未接种者相比,接种四价 HPV 疫苗可显著降低术后 2 年 HPV 感染率(8.11% vs. 15.75%, P =0.026)和 CIN2+ 的复发率(1.35% vs. 10.62% , P =0.001);而治疗后未接种 HPV 疫苗 CIN2+ 复发风险显著增高 [84]。
最佳接种时机尚不明确。现有大部分研究中 HPV 疫苗是在子宫颈锥切术前或术后不久(LEEP 术后 1 个月内)进行接种的,因而建议在手术前或术后尽快接种疫苗,推迟接种疫苗可能无法防止有感染风险的女性再次感染 [85]。
推荐意见:推荐子宫颈癌前病变的适龄女性,在治疗前或治疗后尽早接种 HPV 疫苗(推荐类别:2A)。
2.2 其他 HPV 相关部位癌前病变 / 癌治疗史人群
目前针对女性外阴上皮内病变(vulvar intraepithelial neoplasia, VIN)、 阴 道 上 皮 内 病 变(vaginal intraepithelial neoplasia, VaIN)/ 癌、AGW 以及 AIN/ 癌治疗史人群接种HPV 疫苗的临床研究有限。研究表明,在患有 HPV 相关AGW、VIN 或 VaIN 的年轻女性中,接种四价 HPV 疫苗可显著降低任意后续疾病(CIN1+, AGW, VIN1+, VaIN1+)的风险达 64.4% [86]。对接受手术的高级别 VIN 女性进行前瞻性病例对照研究显示,与单纯手术相比,术后不久接种四价 HPV 疫苗可降低高级别 VIN 发病率(19% vs. 32% , P =0.19)和复发率(4.8% vs. 22.3% , P =0.01)[87]。与未接种疫苗的男性相比,四价 HPV 疫苗可显著降低 MSM 者AIN 2+ 的复发 [88]。对 27 岁以上既往 AIN 2+ 的 HIV 阳性的 MSM 患者接种四价 HPV 疫苗可使肛门癌的终身风险降低 60.8% [89]。另有研究显示,RRP 儿童患者接种四价 HPV疫苗后病情得以稳定或持续缓解 [90-91]。成人 RRP 患者经手术和四价 HPV 疫苗接种的联合治疗后可获益 [92]。
推荐意见:推荐既往外阴、阴道癌前病变 / 癌治疗史、肛 门 癌 高 风 险 人 群(包 括 HIV 阳性和 MSM)、AGW 和RRP 人群,尽早接种 HPV 疫苗(推荐类别:2B 类)。
3. 高风险人群
3.1 遗传易感人群
遗传易感因素可能影响 HPV 感染的敏感性、持续性以及子宫颈癌的发展速度 [1]。共有基因遗传度占子宫颈癌易感性总变异的 27% [93]。子宫颈癌的全基因组遗传变异关联性研究(genome-wide association study, GWAS)分析已识别的多个遗传易感变异位点,发现其多与免疫反应基因有关。中国人群 GWAS 先后发现 6p21.32 位 点 突 变,EXOC1 和GSDMB 基因(4q12 和 17q12)区段的遗传易感变异位点,其编码的蛋白分别与固有免疫和肿瘤细胞增殖有关 [94]。德国人群病例对照研究显示,6p21.32 位点突变(rs9357152),14q24.3 位点突变(rs4243652)分别与 HPV16 和 HPV18 阳性浸润性宫颈癌相关;rs9357152 可能在 HPV 存在的情况下通过调节 HLA-DRB1 的诱导来发挥作用 [95]。
推荐意见:推荐遗传易感位点变异的适龄女性(HLADPB2、EXOC1 和GSDMB 基因突变等)接种 HPV 疫苗。建议遗传易感人群在首次性行为之前接种,即使性暴露后亦应尽早接种。(推荐类别:2B 类)。
3.2 子宫颈癌发病高风险生活方式人群
性生活过早、多性伴、多孕、多产、吸烟、长期口服避孕药、性传播疾病者等是子宫颈癌等 HPV 相关疾病的高危因素 [2, 30]。50%以上的年轻女性在开始性行为后的 3 年内就会发生 HPV 感染。青春期女孩下生殖道发育尚未成熟,过早性生活会使子宫颈上皮多次重复暴露于某些细菌或病毒,产生潜在细胞变异。
推荐意见:优先推荐子宫颈癌发病高风险生活方式的适龄女性尽早接种 HPV 疫苗(推荐类别:2A 类)。
4.免疫功能低下人群
免疫功能低下人群包括 HIV 感染者;自身免疫性疾病患者;肥胖、糖尿病、肾衰竭血液透析者;器官 / 骨髓移植后长期服用免疫抑制剂患者。
4.1 HIV 感染者
研究表明,13~45 岁 HIV 感染女性接种四价 HPV 疫苗的抗体应答率为 75% ~100% [96]。HIV 感染人群首剂接种HPV 疫苗(双价、四价和九价 HPV 疫苗)后 28 周对 HPV 16 和 18 血清阳转率 94% ~100%, 并 会 持 续 2~4 年 [97]。≥9 岁的 HIV 感染女性接种四价 HPV 疫苗后中位随访 2 年未发现 CIN2+ 病例 [98]。2022 年 WHO 立场文件明确指出:建议将 HIV 感染在内的免疫功能低下人群的 HPV 疫苗接种作为公众健康计划的优先事项之一 [4]。
推荐意见:优先推荐 HIV 感染的适龄女性人群接种HPV 疫苗,最好在性行为之前接种(推荐类别:2A 类)。
4.2 自身免疫性疾病患者
自身免疫性疾病患者如系统性红斑狼疮、自身免疫 性 炎 症 性 风 湿 病(autoimmune inflammatory rheumatic diseases, AIIRD)、风湿性关节炎、干燥综合征、桥本甲状腺炎等。AIIRD 患者 HPV 感染率是普通人群的 1.6 倍 [99]。对自身免疫性疾病患者接种 HPV 疫苗研究显示,接种四价 HPV 疫苗后在第 12 个月,患者抗 HPV 血清型 6、11、16 和 18 的阳转率分别为 76% ~ 98%,在使用免疫抑制剂患者中抗体滴度较低 [100];血清阳转患者随访 5 年后,抗体仍持续存在,疫苗相关型别血清阳转率为 84% ~ 96% [101];真实世界多中心研究也证实了 HPV 疫苗用于这一人群的安全性和免疫原性 [102]。国内外均建议对自身免疫性疾病患者接种 HPV 疫苗 [103-104]。
推荐意见:推荐患有自身免疫性疾病的适龄人群接种HPV 疫苗(推荐类别:2A 类)。
4.3 糖尿病患者、慢性肾脏病或肾衰竭血液透析者
目前全球范围内关于糖尿病患者接种 HPV 疫苗的相关研究十分有限。对中国 HR-HPV 感染且细胞学诊断为HSIL 患者的研究显示,糖尿病和糖尿病前期与子宫颈癌呈正相关,1 型糖尿病患者生殖器疣的发病率明显增加 [105]。
慢性肾脏病(chronic kidney disease, CKD)或肾衰竭血液透析患者 HPV 感染及相关癌症的风险增高。肾衰竭患者在移植前,30%患者感染 HPV,其中子宫颈样本中感染率最高(60%)[106]。肾衰竭血液透析患者中 HPV 相关癌症的发病率逐年增加,与普通人群相比,发病率最高增加了 16倍 [107]。对于 CKD 和肾衰竭血液透析患者,接种 HPV 四价疫苗后对 HPV 6/11/16/18 抗体应答率均为 100% [108]。
美国 ACIP 发布的儿童和成人免疫接种计划中,推荐糖尿病患者和肾衰竭血液透析患者常规接种 HPV 疫苗 [109-110]。
推荐意见:对于糖尿病、肾衰竭接受血液透析的适龄人群,建议临床医生与患者共同探讨,在病情允许时接种HPV 疫苗。对全身脏器功能差、预期寿命有限者不推荐接种(推荐类别:2B 类)。
4.4 器官 / 骨髓移植后长期服用免疫抑制剂患者和恶性肿瘤患者
器官移植患者中,长期服用免疫抑制剂人群 HPV 感染及相关癌前病变 / 癌的风险升高 [111]。该类人群接种 HPV 疫苗的抗体应答率低于正常人群。肾移植患者血清阳转率 50% ~75%,肝移植患者和健康女性血清阳转率为 100% [112]。一项研究者发起的 18~55 岁实体器官移植患者的Ⅲ期研究表明,九价 HPV 疫苗首剂接种后第 7 个月时疫苗相关型别抗体血清阳转率为 46% ~72%,耐受性良好,无疫苗相关严重不良事件 [113]。对骨髓移植患者接种 HPV 疫苗的前瞻性研究显示,接受免疫抑制剂治疗患者对所有疫苗覆盖型别的抗体应答为 78.3%,未接受免疫抑制剂治疗患者应答率为 95.2%[114]。
2019 年美国移植学会指南建议:所有 9 ~ 26 岁移植患者(最好在移植前)强烈推荐接种 3 剂次九价 HPV 疫苗;45 岁以下人群和患有生殖器疣的 15 ~ 26 岁移植受者,也可接种 HPV 疫苗(弱推荐)[115]。2024 年美国临床肿瘤学会(American Society of Clinical Oncology, ASCO)指南建议:19 ~ 26 岁恶性肿瘤患者推荐接种 HPV 疫苗,27 ~ 45 岁恶性肿瘤患者建议医生与患者共同决策;理想情况下疫苗接种应比肿瘤治疗计划早 2~4 周,以便在肿瘤治疗影响患者的免疫系统之前达到最佳的保护效果;可以在造血干细胞移植后 9 ~ 12 个月接种 HPV 疫苗 [116]。
推荐意见:对于器官或骨髓移植后长期服用免疫抑制剂或恶性肿瘤患者,建议临床医生与患者共同探讨,根据疾病轻重差别给予个体化建议,对于预期寿命长的适龄女性,推荐移植 1 年后接种 HPV 疫苗;对于预期寿命有限者,不推荐接种(推荐类别:2B 类)。
5.妊娠期和哺乳期女性
妊娠期女性接种 HPV 疫苗的研究数据有限。一项关于妊娠女性接种 HPV 疫苗的系统性综述和荟萃分析显示,妊娠期接种 HPV 疫苗不增加不良妊娠结局的风险 [117],安全性结果与全球临床试验及安全性监测研究的结果一致 [118]。接种九价 HPV 疫苗女性妊娠后不良妊娠结局和胎儿先天发育异常率与四价 HPV 疫苗相似,未发现与九价HPV 疫苗相关的不良妊娠结局 [119]。
2019 年美国 ACIP[70]、2022 年 WHO 发表的 HPV 疫苗立场文件 [4] 和 2023 年中国子宫颈癌综合防控指南(第二版)[30]指出:基于妊娠期 HPV 疫苗接种数据有限,不推荐妊娠期女性预防性接种 HPV 疫苗,应将疫苗接种推迟至妊娠结束后。若疫苗接种后发现已妊娠,应将未完成接种剂次推迟至分娩后再行接种,接种 HPV 疫苗前无需常规妊娠检测。
从现有证据来看,哺乳期女性接种 HPV 疫苗后,母亲和婴儿发生疫苗相关不良事件的风险并未升高。2022 年WHO 立场文件认为哺乳期女性接种 HPV 疫苗不影响母亲或婴儿母乳喂养的安全性 [4]。虽然目前临床试验尚未观察到血清 HPV 抗体经母乳分泌,但鉴于多种药物可经母乳分泌,且缺乏更多哺乳期女性接种 HPV 疫苗的安全性研究数据,哺乳期女性接种 HPV 疫苗应慎重。
推荐意见:不推荐妊娠期女性接种预防性 HPV 疫苗。若接种后发现妊娠,应将未完成接种剂次推迟至分娩后再行接种;已完成接种者,无需干预。慎重推荐哺乳期女性接种HPV 疫苗。
以上关于普通人群和特殊人群 HPV 疫苗接种的推荐级别,见表 3。

HPV 疫苗的安全性评价数据主要来自上市前的临床试验和上市后的真实世界研究及不良反应监测。我国主要由疾病预防控制中心和药品不良反应监测中心进行监测。
1. 安全性评价
疫苗不良反应(adverse reaction, AR)是指合格的疫苗在正常用法用量下发生的与疫苗接种有明确因果关系的有害反应,一般可预见,与剂量相关。疫苗不良事件(adverse event, AE)指疫苗接种过程中或之后出现的不良事件,但该事件未必与疫苗接种有因果关系。严重不良事件(serious adverse events, SAE)是指受种者接种疫苗后出现死亡、危及生命、永久或严重的残疾或功能丧失、需要住院治疗或者延长住院时间等。疫苗上市后应用过程中出现的免疫接种后不良事件(adverse events following immunization, AEFI)是指在预防接种后发生的对健康有影响的医学事件或反应,可疑与预防接种有关,但不一定与接种疫苗存在因果关联。
2. 全球 HPV 疫苗安全性评价
目前全球使用 HPV 疫苗的所有来源的数据均显示其具有良好安全性 [4]。全球疫苗安全咨询委员会(GACVS)先后 5 次对 HPV 疫苗的安全性进行定期审查,认为 HPV 疫苗是非常安全的 [120]。WHO 在 2022 年更新的立场文件中指出:自 2006 年获得许可以来,已经使用超过 5 亿剂次 HPV 疫苗,HPV 疫苗安全且耐受性良好,接种后的 AE 通常是轻微且短暂的;迄今为止,除罕见的过敏反应报告外,上市后监测未发现严重的安全问题 [4]。美国疾病预防控制中心(CDC)、国际妇产科联盟(FIGO)和中华预防医学会妇女保健分会等多个权威组织与专家同样认可 HPV 疫苗的安全性 [1-2, 30, 121]。
3. HPV 疫苗临床试验的安全性
双价疫苗在我国的临床试验中,所有受试者发生的局部和全身 AR 均为轻度或中度(≤3 级),接种部位最常见的是疼痛,其次为硬结;发热、头痛和疲劳是三种最常见的全身症状(疫苗说明书);未见疫苗相关 SAE[4]。
四价 HPV 疫苗在中国进行的Ⅲ期临床试验结果表明,在中国 9~45 岁女性中安全性和耐受性良好,与全球临床试验结果相似。最常见为注射部位疼痛和红肿;常见全身性症状为发热、疲乏、头痛等,未见疫苗相关 SAE[37]。9~45 岁中国健康女性接受 3 剂九价 HPV 疫苗的Ⅲ期临床试验显示,大多数为轻度或中度(<3 级),局部注射部位 3 级 AE 发生率为 3.1% ~3.5%,最常见也是疼痛和红肿 [40]。
关于 HPV 疫苗与妊娠相关性,在四价疫苗临床研究中,疫苗组与安慰剂组两组间发生的妊娠结局、胎儿 / 婴儿 SAE和新发医疗状况的频率总体相近,并且在正常范围内 [118];双价吸附疫苗对中国上市前临床试验人群继续跟踪随访观察,结果显示受种者在 10 年的随访期间内均未见与疫苗接种相关的 SAE、免疫介导性疾病或不良妊娠结局 [122]。
4. HPV 疫苗上市后监测的安全性
2006 年上市以来,上市后监测数据显示,局部和全身AR 与临床试验结果基本一致 [4]。中国疾病预防控制信息系统监测 HPV 疫苗的安全性研究显示,2017 ~ 2020 年全国共报告接种 2 274.4 万剂次 HPV 疫苗,AEFI 报告发生率为30.38/10 万剂,表明 HPV 疫苗接种后在 9 ~ 45 岁中国女性耐受性良好,没有发现安全问题 [123]。真实世界研究也得到相同结论,疫苗上市后监测研究也未发生与 HPV 疫苗暴露相关的不良妊娠结局 [119]。
1. 不宜接种 HPV 疫苗的情况
对疫苗的活性成分或任何辅料成分有超敏反应者禁止接种 HPV 疫苗,注射后有超敏反应症状者,不应再次接种。对于以下人群,需慎用 HPV 疫苗:① 有血小板减少症或其他可成为肌内注射禁忌证的凝血功能障碍者不宜接种;② 急性疾病常伴有发热等全身症状,接种疫苗可能会加重症状,建议在痊愈后接种;③ 因部分女性有不同程度的经期不适,建议非经期接种。
2. 接种 HPV 疫苗后仍应进行子宫颈癌筛查
接种 HPV 疫苗后仍需继续进行子宫颈癌筛查。① HPV 疫苗对于存在 HPV 感染或相关疾病危险因素(如多性伴、既往感染过疫苗相关 HPV 型别、免疫缺陷等)的人群有效性降低;② HPV 疫苗是预防性疫苗,不能清除已存在的 HPV 感染和治疗 HPV 相关疾病,也不能防止病变的进展;③ HPV 疫苗所含型别有限,不能预防所有 HPV型别感染,即使接种了 HPV 疫苗,机体仍处于对非疫苗型别 HPV 的感染风险中;④ 少数子宫颈癌可能与 HPV 感染无关,特别是非 HPV 相关性肿瘤;⑤ 全球上市最早的四价HPV 疫苗长期随访研究证实其具有 14 年的保护作用,但HPV 疫苗有终身保护作用还需研究证实。因此,接种 HPV疫苗后仍需继续进行子宫颈癌筛查。
3. 接种 HPV 疫苗后无需进行抗体检测
首先,HPV 接种后的保护效力一般是通过在临床试验中比较安慰剂和疫苗组人群的发病率来计算,不能等同于抗原能刺激机体免疫系统产生抗体和致敏淋巴细胞的特性,即免疫原性(抗体水平)。HPV 疫苗的免疫原性与保护效力之间的相关性目前尚无明确数据(与预防 CIN2/3 或抗持续感染所对应的 HPV 抗体水平的最低阈值尚未明确)。其次,HPV 疫苗抗体检测尚未实现标准化、统一化,并无金标准来设定阳性抗体结果的阈值;抗体血清学检测也未用于临床,仅在研究中使用,而且不同 HPV 疫苗采用的抗体检测方法不同,不同方法的检测结果不具备可比性。此外,由于免疫记忆机制的作用,即使在接种疫苗数年后接种者的抗体水平出现下降,也已证实疫苗型别特异性的保护效果仍然持续存在。美国 ACIP 指出:没有任何通过临床抗体检测可以确定 HPV 疫苗接种者是否已经获得免疫保护或仍对任何特定的 HPV 型别易感 [70]。因此,对于接种者而言,疫苗接种后没有必要进行 HPV 抗体检测。
预防性 HPV 疫苗接种是预防 HPV 感染、HPV 相关下生殖道及其他部位疾病的有效、安全方法。性暴露前接种免疫效果最佳。优先推荐 9 ~ 26 岁女性接种 HPV 疫苗,重点是 9 ~ 14 岁女孩;同时推荐 27 ~ 45 岁女性和 9 ~ 26 岁男性接种,倡导男女共防。HPV 疫苗不仅适用于一般人群,同样推荐用于子宫颈癌发病高风险生活方式人群,以及具有遗传易感、HIV 感染等特殊人群。无论是否存在 HPV 感染、细胞学是否异常的适龄女性均可接种 HPV 疫苗。有HPV 相关病变治疗史的适龄女性患者,接种 HPV 疫苗可能降低复发率。近期有妊娠计划和妊娠期、哺乳期女性不宜接种 HPV 疫苗。接种 HPV 疫苗后仍应进行子宫颈癌筛查,但不必进行 HPV 抗体检测。
执笔专家:李明珠(北京大学人民医院)、赵方辉(中国医学科学院肿瘤医院)、尹如铁(四川大学华西第二医院 /华西妇产儿童医院)、王新宇(浙江大学医学院附属第一医院)、丛青(复旦大学附属妇产科医院)、李双(华中科技大学医学院附属同济医院)、殷爱军(山东大学齐鲁医院)、宋坤(山东大学齐鲁医院)、隋龙(复旦大学附属妇产科医院)、孔北华(山东大学齐鲁医院)、马丁(华中科技大学同济医学院附属同济医院)、魏丽惠(北京大学人民医院)
专家委员会成员(按姓氏笔画排序):王建六(北京大学人民医院)、王临虹(中国疾病预防控制中心)、王晓黎(海南省妇幼保健院)、 尤志学(南京医科大学第一附医院 / 江苏省人民医院)、 毕蕙(北京大学第一医院)、曲芃芃(天津市中心妇产科医院)、乔友林(中国医学科学院肿瘤医院)、向阳(中国医学科学院北京协和医院)、刘继红(中山大学肿瘤防治中心)、李静然(北京大学人民医院)、李亚里(解放军总医院第一医学中心)、李克敏(四川大学华西第二医院)、李隆玉(江西省妇幼保健院)、林仲秋(中山大学孙逸仙纪念医院)、杨帆(中山大学肿瘤防治中心)、吴小华(复旦大学附属肿瘤医院)、吴鹏(华中科技大学同济医学院附属协和医院)、沈丹华(北京大学人民医院)、张国楠(四川省肿瘤医院 / 四川省第二人民医院)、张淑兰(中国医科大学附属盛京医院)、狄文(上海交通大学医学院附属仁济医院)、胡尚英(中国医学科学院肿瘤医院)、郄明蓉(四川大学华西第二医院)、余楠(华中科技大学医学院附属同济医院)、周琦(重庆大学附属肿瘤医院 / 重庆市肿瘤医院)、姜桦(复旦大学附属妇产科医院)、赵超(北京大学人民医院)、赵昀(北京大学人民医院)、郝敏(山西医科大学第二医院)、高雨农(北京大学肿瘤医院)、郭瑞霞(郑州大学第一附属医院)、崔恒(北京大学人民医院)、梁志清(重庆医科大学附属妇女儿童医院)、程文俊(南京医科大学第一附属医院 / 江苏省人民医院)、薛凤霞(天津医科大学总医院)
致谢:感谢各学(协)会专家给予的大力支持。
利益冲突:所有作者均声明不存在利益冲突。
参考文献略