跟随肿瘤界,听点肿瘤学。有趣、有料、有用,肿瘤界100秒是一档利用碎片时间了解肿瘤学的科普音频,每期2~3个知识点,轻松了解肿瘤学知识,挖掘知识背后的奇闻逸事,让知识鲜活。
跟随肿瘤界,听点肿瘤学。大家好,这里是肿瘤界100s,我是主播李静。
一年一度的肿瘤春晚——ASCO年会落幕了。
这届会议给很多研究收尾,比如奥希替尼的ADAURA研究,终于在死亡终点上扬眉吐气。我们今天谈的PHERGain研究也完成了3年的随访,证实了部分早期HER2+乳腺癌,在无化疗和PET检查的辅助下,对曲妥珠单抗+帕妥珠单抗的双HER2+靶向治疗敏感的患者,3年无浸润疾病生存率(iDFS)可以达到惊人的95.4%。
虽然HER2+只占乳腺癌的20%~30%,但围绕着HER2几乎占据了所有乳腺癌靶向治疗的热度。从去年DS8201掀起的低HER2表达热潮,到今年双HER2靶向的PHERGain研究,似乎完善了乳腺癌的HER2宇宙,HER2阴阳之外,还能细分出HER2低表达和超高表达的人群,以对接细分出的双HER2靶向治疗。
老规矩,在进入研究物语之前,我们先来明确一些基础概念。
HER2(Human Epidermal Growth Factor Receptor 2)是一种人类表皮生长因子受体2(HER2)蛋白。
HER2不同于别的mTOR这些缩写,从名字上就可以看出和肿瘤相关,因为癌症就是上皮细胞的癌变,上皮就是表皮,这个人类表皮生长因子受体2,作用是调控上皮生长的。
HER2还不同于肺癌的EGFR突变,20%左右的乳腺癌患者HER2是过度表达的,也就是HER2基因本身没有变化,只是拷贝数明显增加,而正常人的DNA链上只有1段HER2基因,这些患者的HER2基因会接连有4段以上的重复,相当于自身扩增了4次,甚至有的超过了50次。导致了在细胞表面上安插了过多的HER2蛋白,有数据指出,HER2+乳腺癌患者的导管细胞表面的HER2蛋白是正常细胞的100倍以上,导致乳腺导管上皮生长过度,而且HER2蛋白过表达还可促进肿瘤细胞生长和分裂,这是为什么HER2阳性癌症通常具有较高的侵袭性和恶性程度。

记得我去年采访医科院肿瘤医院齐立强教授的时候,他说在没有HER2靶向药物的时代,HER2+的乳腺癌是乳腺癌中的“最差生”,还不如三阴性乳腺癌,常规治疗很难奏效,有了曲妥珠单抗以后,“吊车尾”瞬间成为了“尖子生”。
再说点题外话,在有的教科书和论文中,HER2有时也写作HER2/Neu,这是因为1979年时,有人从小鼠的神经肿瘤中发现了一段原癌基因,然后就根据neurologic tumor的简写命名为Neu。早在1987年,又在人类中发现了与neu相同的表皮生长因子,被命名为HER2。之所以是HER2,是因为HER1已经被EGFR,即表皮生长因子受体占用了。直到目前,HER共发现了四个成员,也都是酪氨酸激酶受体家族的成员。
其实啊,并不是阻断了两次HER2,而是阻断了HER2的两种不同状态。
HER2是一种跨膜蛋白,需要两个HER2或者HER2加上另一个HER家族的蛋白成员,形成二聚体才能向细胞内传递信号,我们之前提过的PI3K-AKT-mTOR就是HER2的下游路径之一。
帕妥珠单抗与曲妥珠单抗的作用位点不同[1]:曲妥珠单抗靠近跨膜结构域结合,抑制HER2形成二聚体,而帕妥珠单抗可以结合曲妥珠单抗的漏网之鱼,也就是可以抑制HER2二聚体的特定结构域,起到全面阻断HER2通路的作用。感兴趣的朋友可以点开文稿看看示意图。
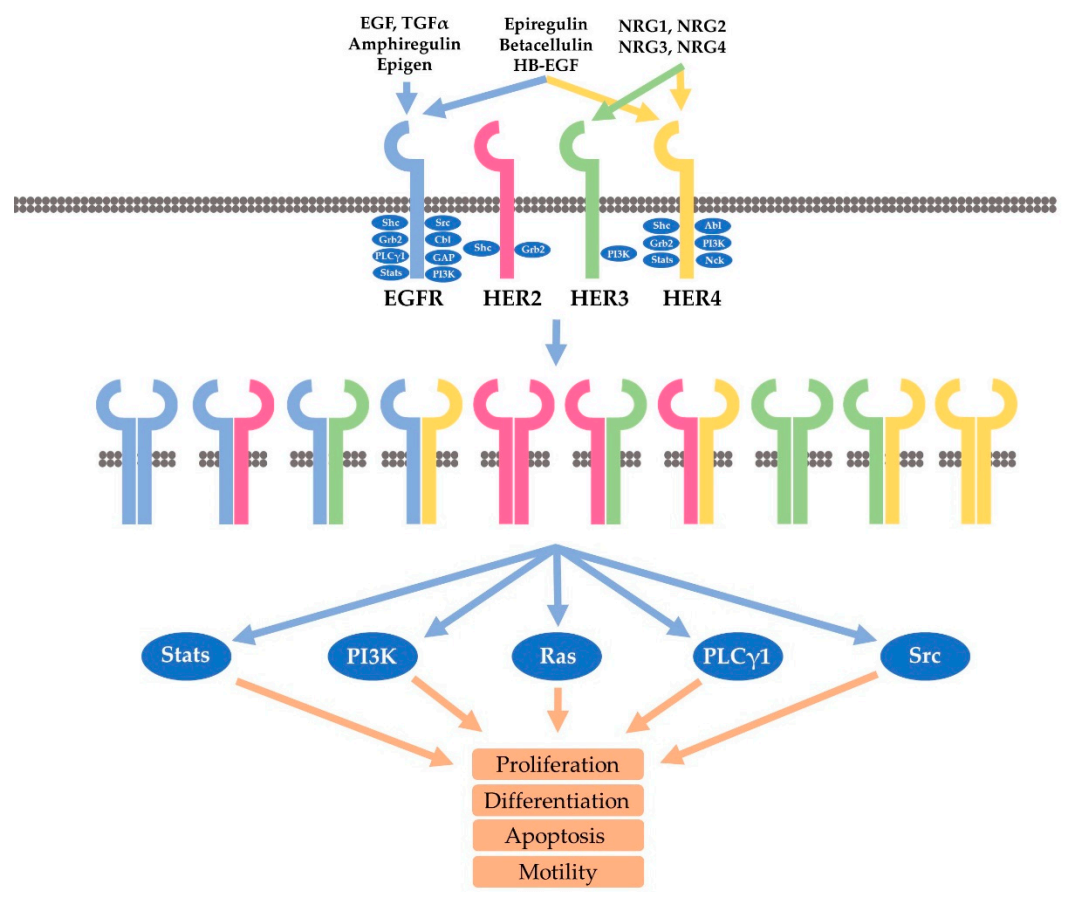
HER家族的二聚化
有了药理机制上的优势,双HER2阻断治疗在PHERGain研究之前也被证实是有效的。早在2017年APHINITY研究就率先使用了帕妥珠单抗+曲妥珠单抗的策略,尝试治疗HER2+、淋巴结阳性或高风险淋巴结阴性、可手术的乳腺癌患者,结果显示,双HER2治疗能够进一步降低乳腺癌的复发风险,3年的无浸润性疾病生存率提升至94.1%。[2]
此次在ASCO年会上的PHERGain研究,早在2021年就在Lancet Oncology[3]上发表了初期结果,此次是随访3年后的次要终点数据。
首先来看受试者,PHERGain研究纳入了HER2+、I~IIIA期、浸润性可手术的乳腺癌患者(肿瘤≥1.5厘米),而且至少做过一次PET,PS评分为0或1。可以看得出受试者的限制条件还是蛮多的。
PHERGain研究不同于常见的随机对照研究的固定分组治疗,而是一直在根据PET的结果在动态改换治疗策略。研究分组较为复杂,您可以点开文稿对照着研究设计图来看。
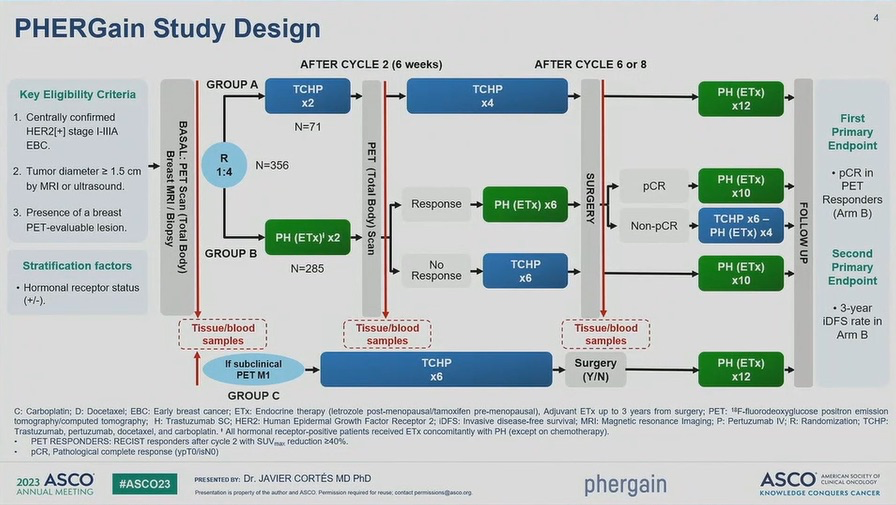
PHERGain的研究分组
首先,研究者将这些受试者分成了A、B两组,A组使用紫杉醇+卡铂化疗,再加上曲妥珠单抗皮下600mg固定剂量给药和帕妥珠单抗840mg负荷剂量和420mg的维持剂量,B组只给与皮下曲妥珠单抗和静脉帕妥珠单抗,两组都是新辅助治疗。
A组完成6个治疗周期即可,但B组需要在双HER2靶向治疗两个周期后进行PET检查,并根据PET结果对治疗方案进行调整,如果PET显示治疗有反应就继续再接受6个周期的双HER2靶向治疗,如果没反应就上A组的化疗+双HER2靶向方案,也是治疗6个周期,两组完成上述治疗后,接受手术,术后对于原B组一直接受双HER2靶向治疗的亚组患者如果PET结果没有到达病理完全缓解(pCR),那么就加入6个周期的化疗方案和4个周期的双HER2靶向治疗,其他人群继续使用双HER2靶向治疗的维持方案。
B组近80%(79.6%)的患者是对双HER2靶向治疗有反应的,PET检测的pCR率达到了37.9%。这一结果其实已经在2021年Lancet杂志公布了。
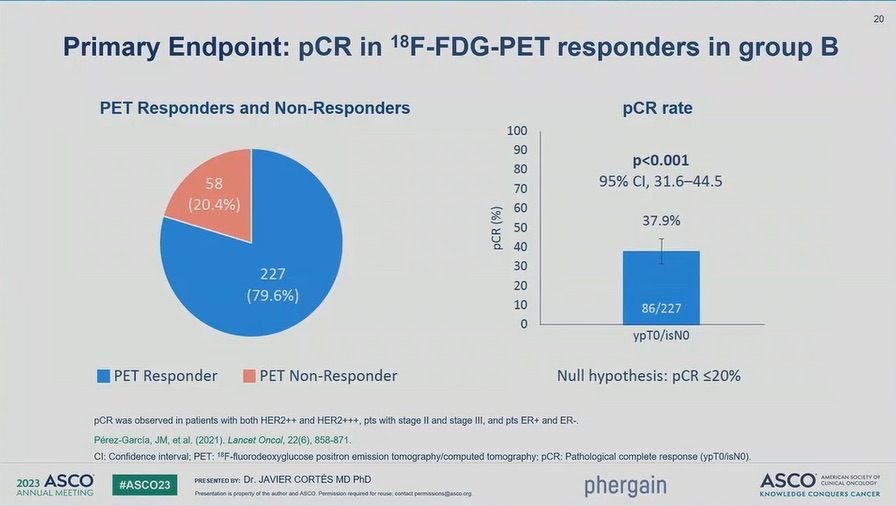
主要终点
而本次会议重点关注的3年无浸润疾病生存(iDFS)终点,对于ITT意向分组人群,iDFS为95.4%,复发低于15例的预期,具有统计学的显著性。
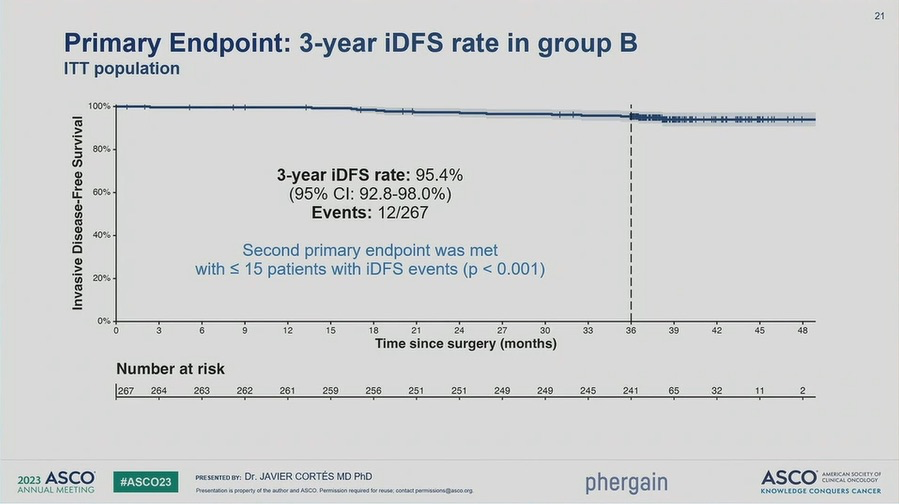 双HER2
双HER2
靶向治疗组(B组)的3年iDFS结果
对于86例从未接受过化疗,且PET显示pCR的患者,3年中只有1例出现复发,iDFS率高达98.8%。
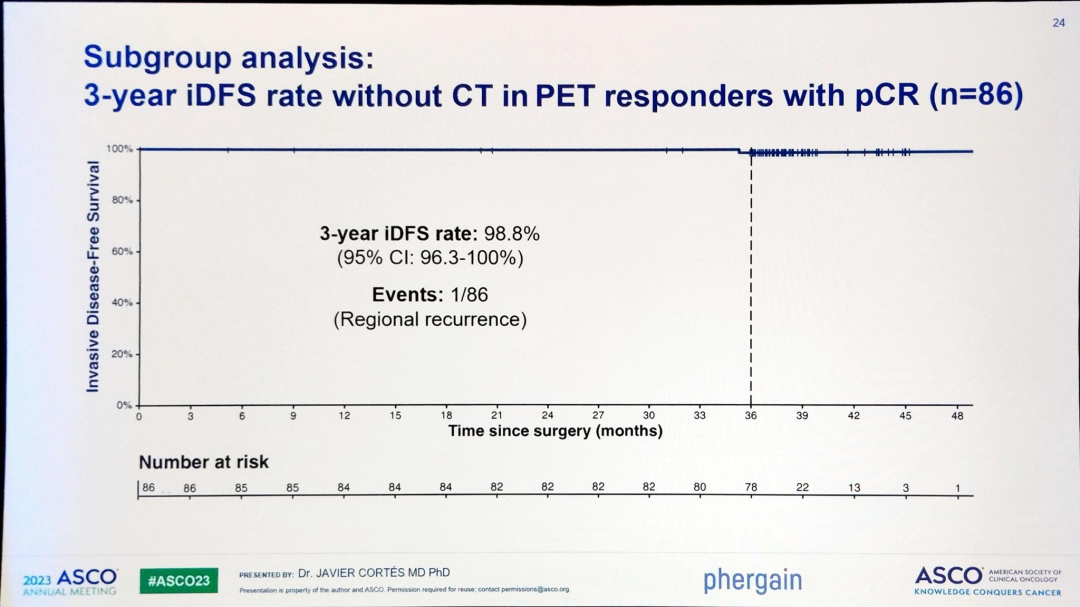
PHERGain研究的直接结果预示着,有的乳腺癌确实可以不化疗了,难怪PHERGain研究的主要研究者在接受媒体采访时表示:
三分之一的(早期HER2+乳腺癌)受试者可以在不接受化疗的情况下治愈,并过上正常的生活,这是令人惊奇的。

单凭一个靶点让整个乳腺癌治疗简化并降级,这的确让人惊讶,毕竟在双HER2靶向之前,只有紫杉醇+曲妥珠单抗这样做出了减少化疗药物的降级方案尝试[4],但鲜有不用化疗的尝试。如果研究真的被广泛认证有效,那么双HER2靶向的唯一问题就是使用时长的问题,会不会在长期使用中发生耐药,以及耐药后如何处理。另外,研究中双HER2靶向治疗组中,最后还是有2/3接受了化疗,所以筛选合适的HER2阳性患者是无化疗的前提,正如我开篇所述,HER2阴阳之外,也许还能细分出HER2超高表达的人群,以对接细分出的双HER2靶向治疗。
希望乳腺癌无化疗时代早些到来。
本期100sASCO特别篇就到这里了,我是李静,感谢您的收听,我们下期见。

编辑:Joy
审核:叶文洁
出品:肿瘤界