
为了响应《“健康中国2030”规划纲要》,实现我国全民消化肿瘤早诊早治,《肿瘤界》设立“齐力荟聚-消化肿瘤频道”,聚焦消化肿瘤患者的诊断治疗。旨在报道国内前瞻性、创新性和高学术水平的关于消化道肿瘤防治的临床应用和基础研究,把握学术发展动向,促进学术交流,整体提高国内消化肿瘤防治的临床与研究水平,结合国内研究特色,以及国内临床规范制度,推动消化肿瘤防治的进步,普及推广临床规范化诊疗。
专家访谈
专家简介

问题一:结直肠癌(统称为大肠癌)是威胁我国居民生命健康的主要癌症之一,造成了严重的社会负担。大肠癌的筛查是降低相关人群死亡率的有效措施。请您谈谈我国居民如何自我发现大肠癌?
良好的生活和饮食习惯,尤其是增加膳食纤维素摄入,可以预防大肠癌的发生。预防是最有效的防癌手段。早期大肠癌几乎没有任何症状,只有发展到中晚期才会有明显症状。目前认为,绝大部分结肠癌来源于没有引起足够重视的肠道息肉。肠道息肉的恶变过程可能长达10-20年。所以,粪便的肠道脱落细胞甲基化检测和肠镜筛查是发现早期大肠癌的重要手段。假如我们没有进行上述的主动肠癌筛查,下面的这些症状出现就要引起我们高度重视。
一、粪便带血
便血是大肠癌的典型症状,因为出血的部位不一样,出血量和出血速度不同,所以便血的颜色也有一定的差异。无论粪便中的血液呈现鲜红色、暗红色还是黑色都要引起重视,及早去医院做相关检查。大便带血的排查要有底线思维,首先要积极检查排查恶性肿瘤,其次是考虑良性疾病。
二、排便习惯改变
大多数大肠癌患者大便习惯可随之发生改变,排便次数明显增加,有时会出现腹泻,即使服用止泻药物也没有任何效果。因为生长在直肠的肿块、恶性肿瘤溃疡可产生太多分泌物,从而造成肠道刺激症,导致排便次数增加和排便不尽感以及里急后重,常常会排出黏液或脓血物质。
三、大便性状改变
大部分结直肠癌患者大便外形发生改变,如大便变细、大便呈现扁平状,有时大便较稀且不成形,同时大便中带有黏液或血液。
四、腹部是否有不适感
大肠癌患者腹部会出现难以解释的阵发性胀痛或隐痛,有时会出现便秘,便秘腹泻交替进行,有时可在腹部摸到包块。
问题二:晚期大肠癌(或称转移性结直肠癌,mCRC)患者总生存期(OS)随着治疗线数增多而延长,您能否谈一谈对于mCRC患者,如何优化前线治疗和有序启动更多后线治疗,实现尽可能长的OS?
对于mCRC患者,主诊医生要基于PS评分、病理学类型、分子生物学特征、身体耐受性、经济可负担性和治疗意愿等综合因素,优化方案选择、合理布局和进行全程管理。尤其是后线治疗患者,随着新药越来越多,需要对患者进一步细分,动态的基因检测评估,再根据患者上述综合评估,重新选择合适匹配的药物。
一线治疗mCRC通常会根据患者的发病部位和RAS基因型选择不同靶向药物联合化疗。mCRC的MSI-H的患者能够从免疫治疗中获益,选择免疫检查点抑制剂为基础的治疗方案有望进一步提高疗效。在未来,或许通过联合治疗将MSS型结直肠癌转化为“热肿瘤”,也有望为更多患者带来新希望。
mCRC后线治疗的原则是在保证患者生存质量的基础上改善生存,因此对于前线治疗存在严重不良反应的患者,则要考虑其他的治疗方案。部分患者在接受化疗时,可能会产生较重的骨髓抑制和消化道反应等,那么,Chemo-Break方案能够让患者从前期的治疗不良反应中得以恢复,为后线治疗提供更多机会。以瑞戈非尼为代表的TKI类药物已成为mCRC后线治疗的标准方案。而对于能够耐受化疗,或者无法耐受TKI不良反应的患者,曲氟尿苷替匹嘧啶片(TAS-102)也是可供选择的后线化疗方案。此外,随着病程进展,肿瘤可能存在分子表型的改变,后线治疗需根据基因检测结果灵活调整治疗方案。
总而言之,mCRC治疗已经迈向精准化和个体化治疗,在选择治疗方案时要充分考虑药物疗效和患者耐受情况,为患者创造更好的OS和生存质量。
问题三:基于多年来的研究探索,TAS-102联合贝伐珠单抗治疗mCRC患者在PFS、安全性、耐受性方面得到了更优的研究结果。请您结合相关研究谈谈该方案在2022年发布的CACA-RC指南中有着怎样的推荐地位?
2015年,TAS-102获美国FDA批准,用于难治的mCRC多线治疗。获批的主要依据是国际多中心大型临床Ⅲ期随机试验RECOURSE研究。此外,2018年国际多中心III期临床试验TERRA研究也同样验证了TAS-102的疗效。两项研究结果非常一致,TAS-102治疗的DCR为44%,mOS在7~8个月。RECOURSE和TERRA研究的亚组分析显示,KRAS野生型患者经TAS-102治疗的生存获益显著,死亡风险较对照安慰剂降低23%~42%。
C-TASK-FORCE研究和DANISH研究均显示,对于PS为0~1分的mCRC患者,TAS-102+贝伐珠单抗三线治疗实现了超过4.5个月的mPFS时间,超越了既往单药三线治疗的总体水平,且未显著增加AEs。TAS-102+贝伐珠单抗4周方案治疗mCRC显示了良好抗肿瘤活性。BiTS研究确证了双周方案可在不影响疗效的前提下,明显降低中性粒细胞减少症发生。KSCC 1602研究也成功探索了FTD/TPI +贝伐珠单抗用于mCRC一线治疗的疗效和安全性。
2021年ASCO-GI大会报告了一项TASCO1研究进展,2016年4月至2017年3月,随机对153例患者进行随访,直到2020年9月1日研究结束。有21例患者(TT-B组,n=11;C-B组,n=10)仍存活并接受了检查分析。纳入的是经研究者判断不能耐受强烈治疗的患者和老年患者,既往未接受过化疗,肿瘤负荷较低,证实TAS-102+贝伐珠单抗较卡培他滨+贝伐珠单抗显著延长mPFS(9.23个月对比7.82个月)和OS(22.31个月对比17.67个月)。
TAS-102+贝伐珠单抗该治疗方案毒副反应相对较低,疗效确切,被CACA-RC指南推荐为姑息一线治疗方案,为国内不适合强烈治疗的mCRC患者和老年患者带来持续的、更优的生活获益。
问题四:目前靶免联合治疗在mCRC肝转移领域进行了诸多探索,也取得了一些成绩。请您谈谈目前靶免联合治疗在mCRC肝转移群体中的应用情况如何,未来又有哪些探索的方向呢?
超过一半的晚期大肠癌患者都会出现肝转移。大肠癌肝转移患者经过综合治疗达到NED状态的患者5年生存率可达到40%,但无法达到NED状态的患者5年生存率不足10%。因此,实现结直肠癌肝转移的无瘤状态值得我们继续努力的方向。根据我们的临床实践经验,目前评价结肠癌的瘤负荷状态优选手段包括:FDG的PET-CT、肝脏和直肠的高分辨MRI平扫及增强扫描等多参数评估、ctDNA或者cfDNA的高深度NGS检测评估。mCRC合并肝转移患者治疗前后的评估,尤其是准备积极手术切除的或者其他局部干预的患者,强烈建议肝脏的高分辨MRI评估和全身的PET-CT评估,避免前功尽弃。
MDT模式对于结直肠癌肝转移有着重要意义,多学科专家根据患者具体情况给予合适的治疗策略。对于可手术患者,在综合评判后积极进行手术治疗,以期达到NED状态;对于不可手术的患者,则要综合应用介入治疗、化疗、靶向治疗等手段,争取最佳的临床获益。免疫治疗的兴起,为结直肠癌肝转移的治疗提供了新的希望,靶免联合也已取得一定进展。免疫治疗在MSI-H型结直肠癌中的疗效已经得到认可,而对于MSS型免疫治疗单药获益甚微,联合抗血管生成治疗有望发挥协同效应,提高抗肿瘤疗效。REGONIVO研究显示,瑞戈非尼联合纳武利尤单抗治疗可给MSS型mCRC患者带来获益,引燃MSS型mCRC免疫治疗的研究热潮。在此之后,国内外学者开展一系列研究,探索靶免联合治疗在mCRC肝转移中的应用价值。
但就目前而言,靶免联合的疗效仍有进一步提升的空间。在机制方面,尽管现已发现瑞戈非尼等抗血管生成药物能够改善肿瘤微环境,通过抑制CSF-1R耗竭肿瘤相关巨噬细胞(TAM)、下调免疫抑制因子表达,进而增强抗肿瘤免疫作用。但未来还需进一步探索联合机制,优化联合治疗策略。在治疗方面,未来在靶免联合的基础上,进一步联合射频消融(RFA)、肝动脉化疗栓塞术(TACE)、立体定向放射治疗(SBRT)或放射性粒子植入等局部手段,有望进一步提高结直肠癌肝转移患者的生存获益。
我们期望在不停地摸索中,能够发现更多的规律,寻找更好的治疗策略,积累更加充足的循证医学证据,从而为患者争取最佳预后。
病例分享
专家简介

1 病历资料
刘XX,54岁,男性。
2018-1 因“大便带血20天”外院就诊。
个人史:吸烟指数500(初吸年龄20余岁,25年*20支/天),饮酒5年、200g/d,已戒烟酒。
既往史:体健。
家族史:无特殊。
专科检查:ECOG PS 1分,心肺、腹部未见异常。
2 外院病史资料
2018-1-18 电子肠镜:距肛门9-14cm处见黏膜不规则结节隆起,累及3/4肠壁,镜下诊断直肠癌。
病理活检:直肠中分化腺癌。
2018-1-22 PET/CT:直肠上段肠壁增厚、管腔狭窄,右侧髂内血管走行区、直肠周围间隙多个淋巴结,考虑直肠癌并淋巴结转移瘤,双肺多个小结节,未见明显代谢增高,不除外转移瘤。
2018-1-22 PET/CT
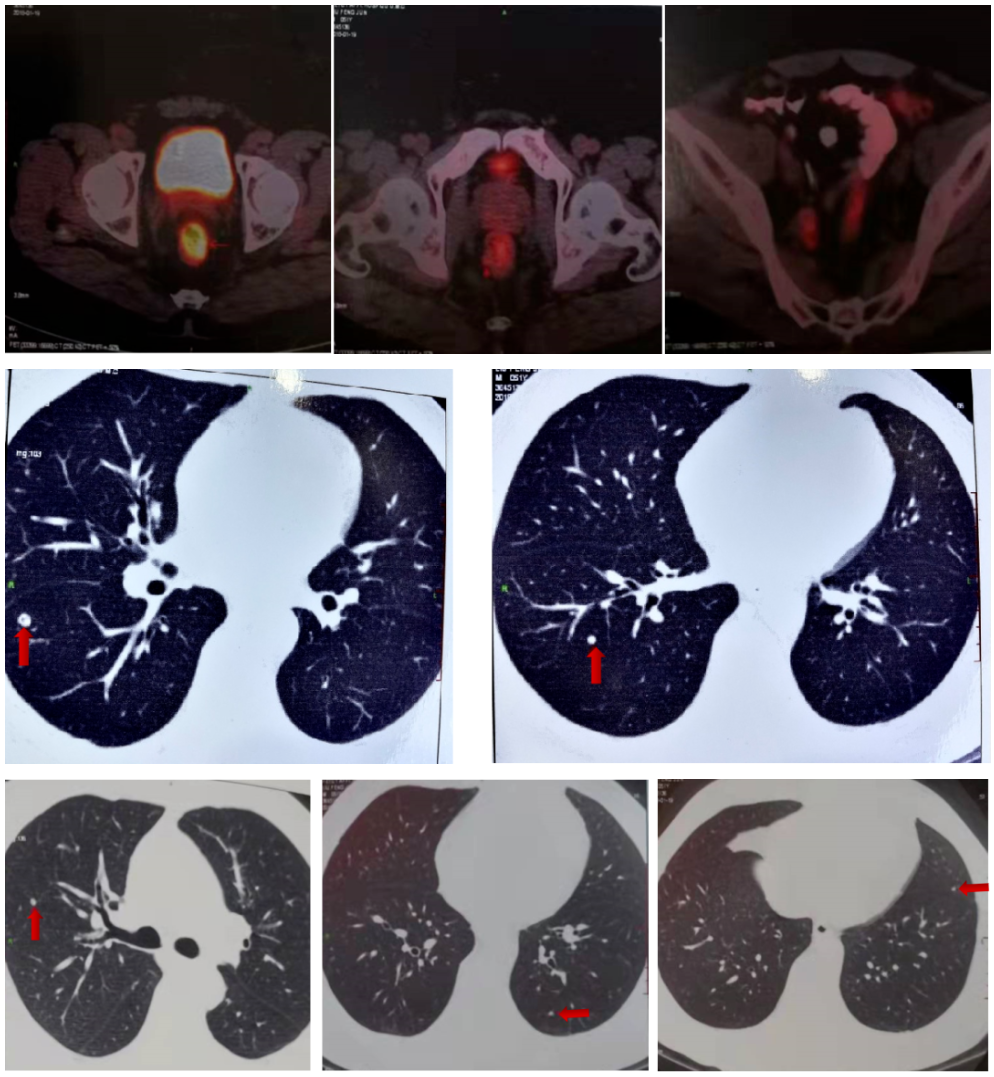
2018-1-27至2018-3-20 行3周期XELOX方案化疗。
2周期化疗后疗效评价SD。
基因检测:RAS、BRAF基因野生型。
2018-4-11至2018-6-30 行5周期西妥昔单抗+FOLFOX方案治疗,疗效评价SD。
2018-8-29 全身麻醉下行达芬奇机器人直肠癌根治术+回肠末端造口术,术后病理:直肠中分化腺癌(溃疡型,直径1.5cm),侵达外膜,符合化疗后反应(Mandard肿瘤消退分级:TRG3级),脉管癌栓(+),肠周淋巴结内癌转移(2/14)。ypT3N1bMx。
一线治疗
2018-10-11 胸部CT:双肺转移瘤较前进展。
2018-10-22至2019-1-19 行5周期贝伐珠单抗+FOLFIRI方案治疗。
2、4周期化疗后疗效评价PR。
2019-3-13 行回肠造口还纳术。
局部治疗(一):射频消融治疗
2019-4至2019-6 外院行肺内转移瘤(6处)射频消融治疗。
2019-5-31 基因检测。

3 我院治疗
2020-1-7强化CT(我院)
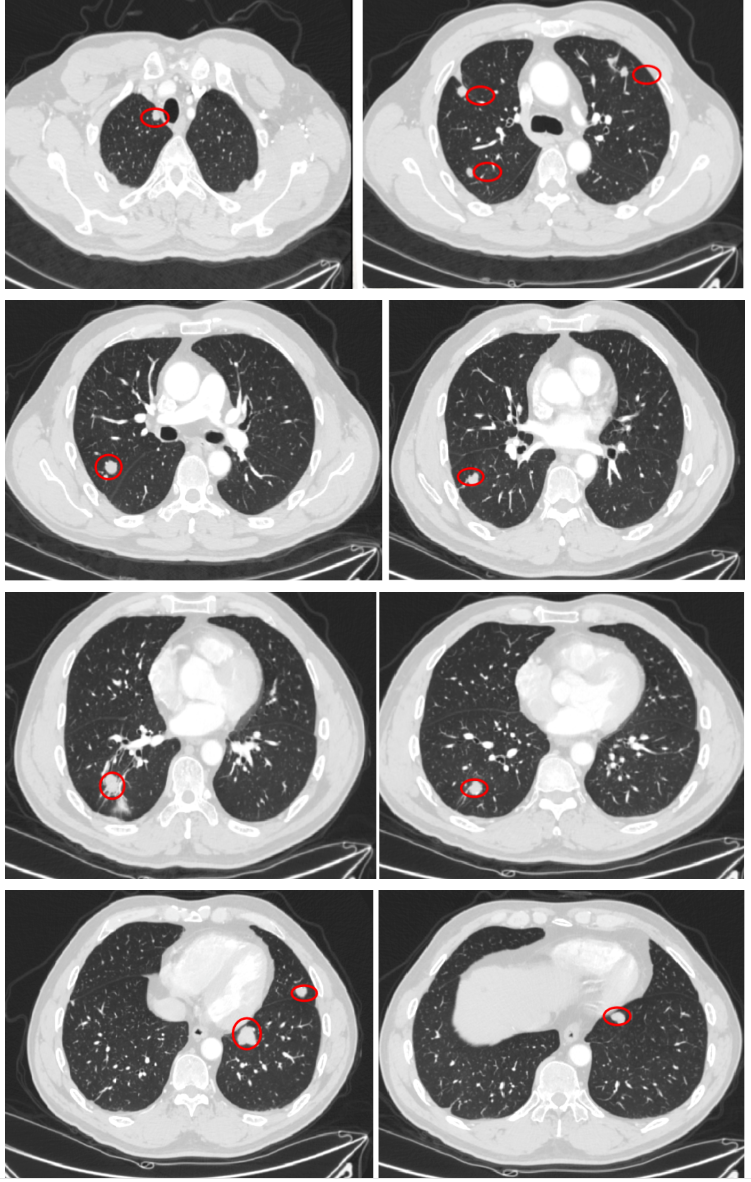
入院诊断:直肠(上段)中分化腺癌;cT0N0M1,IV期;双肺转移;MSS型,RAS/BRAF基因野生型;ERBB2基因扩增型。
二线治疗
2020-1-8至2020-3-4 行4周期西妥昔单抗+FOLFIRI方案治疗,第2周期起联合曲妥珠单抗治疗。
2020-3-23至2020-7-28 予5周期贝伐珠单抗+曲妥珠单抗+伊立替康+卡培他滨(因菌血症输液港取出换用卡培他滨,因皮疹反应不耐受换用贝伐珠单抗)。
二线治疗疗效评价:部分缩小,SD。
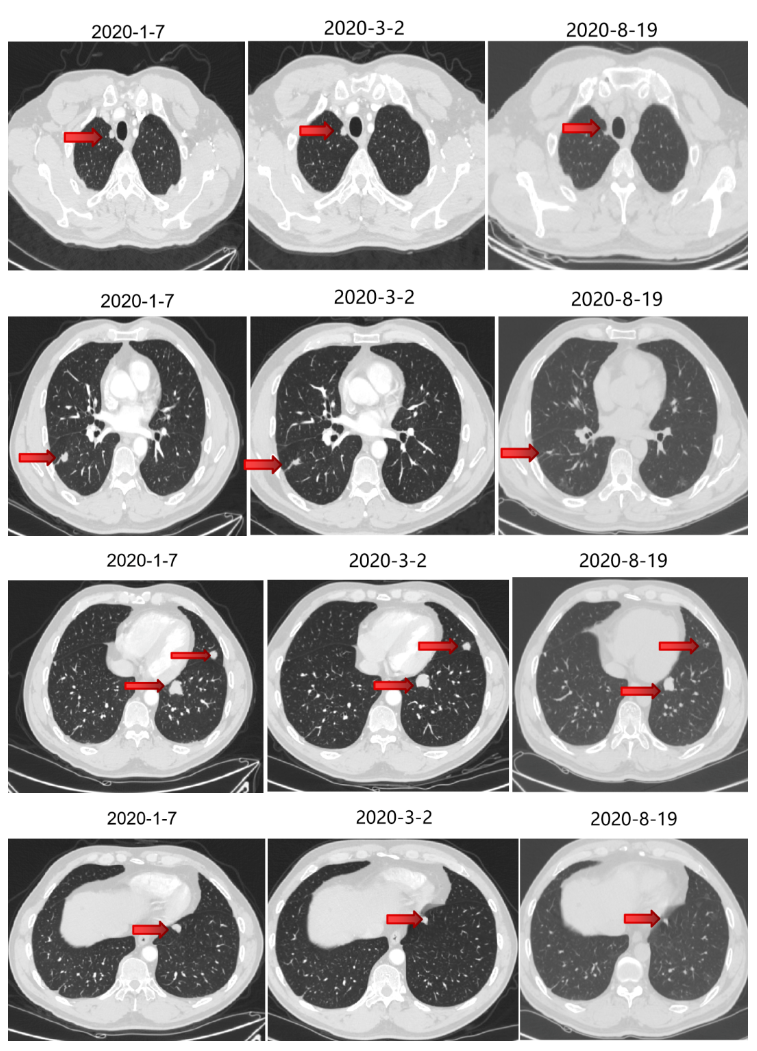
维持治疗
2020-8-19至2020-10-22 予4周期维持治疗:贝伐珠单抗+曲妥珠单抗+卡培他滨。
维持治疗疗效评价:部分略大,SD。
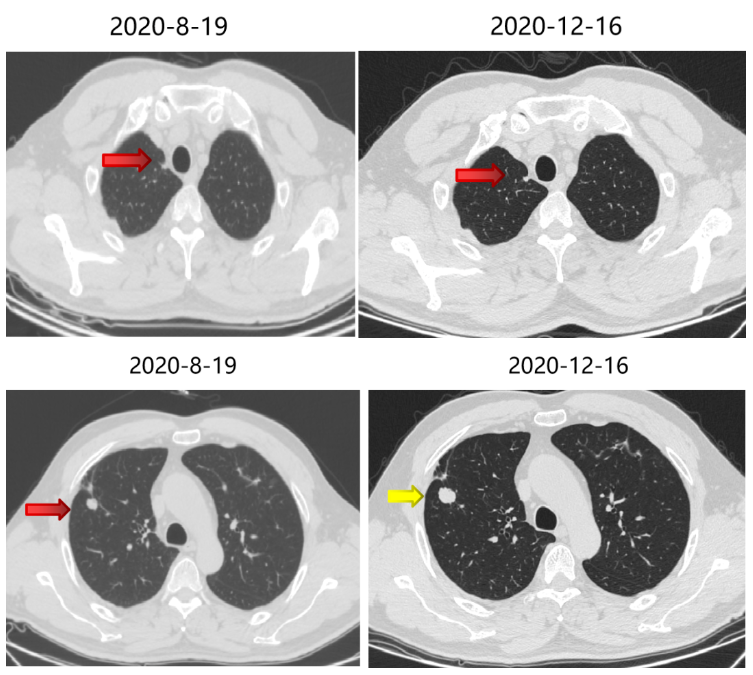
局部治疗(二):SBRT治疗
2020-11-6至2020-11-25 左肺下叶及右肺下叶转移灶放疗:95% PTV1-2 74.7Gy/4.98Gy/15F。
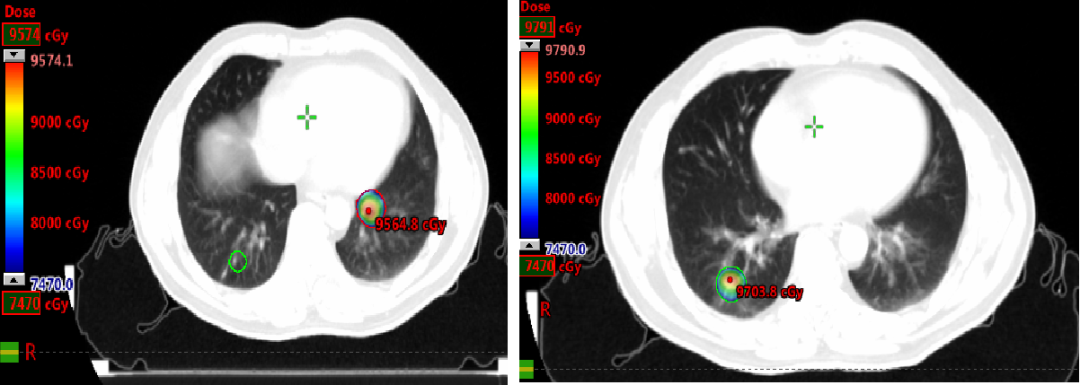
2020-12-31至2021-1-19右肺上叶转移灶放疗:95% PTV 74.7Gy/4.98Gy/15F。
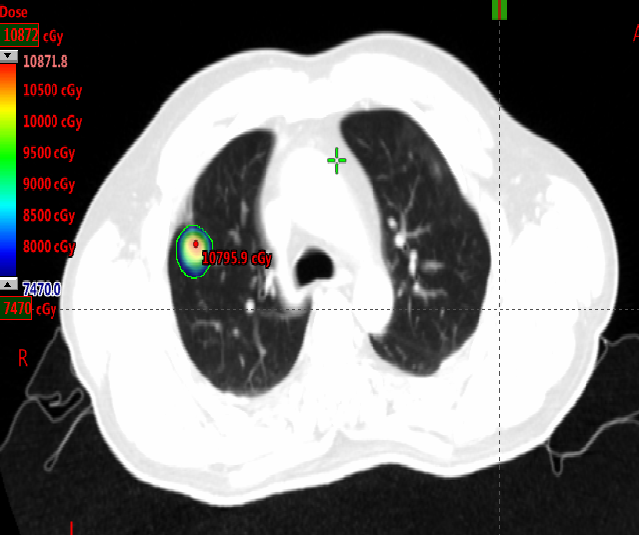
SBRT疗效评价:部分缩小。
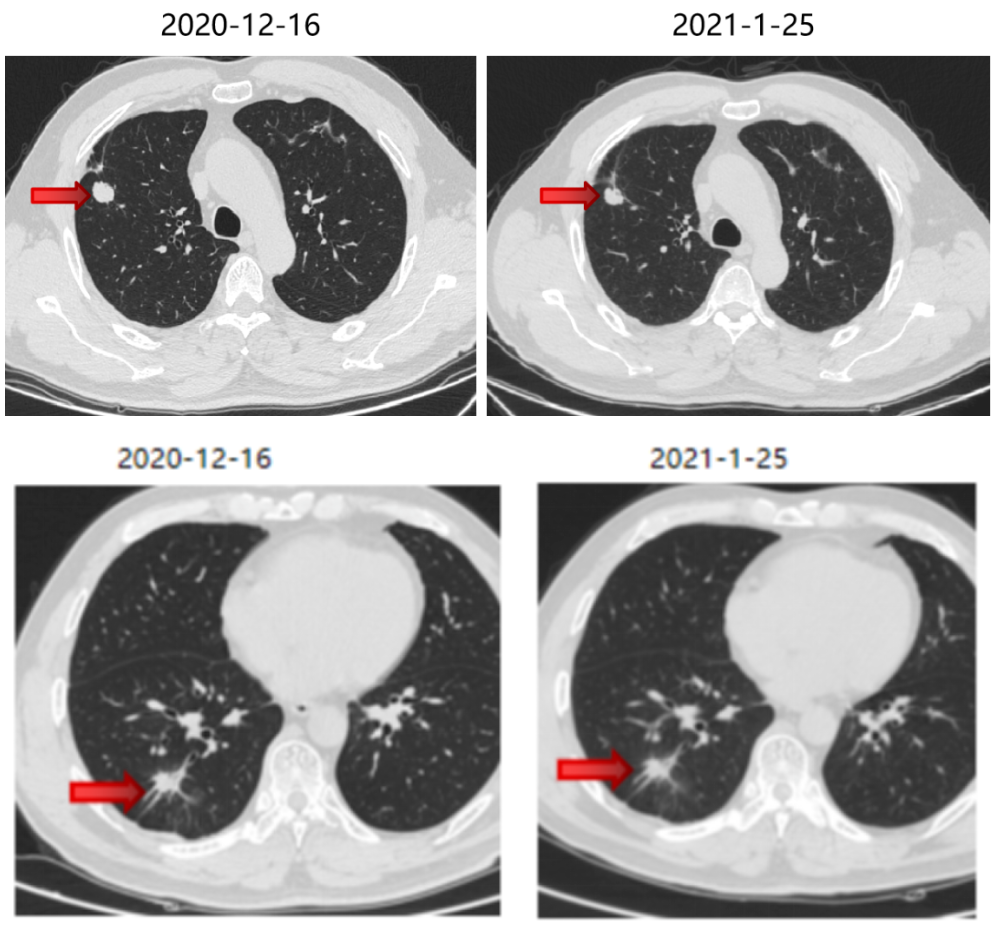
三线治疗
2021-1 起口服呋喹替尼3mg +曲妥珠单抗。
期间2021-3-15胸部CT:双肺转移瘤部分较前略增大,疗效SD。
三线治疗疗效评价:部分增大,PD。
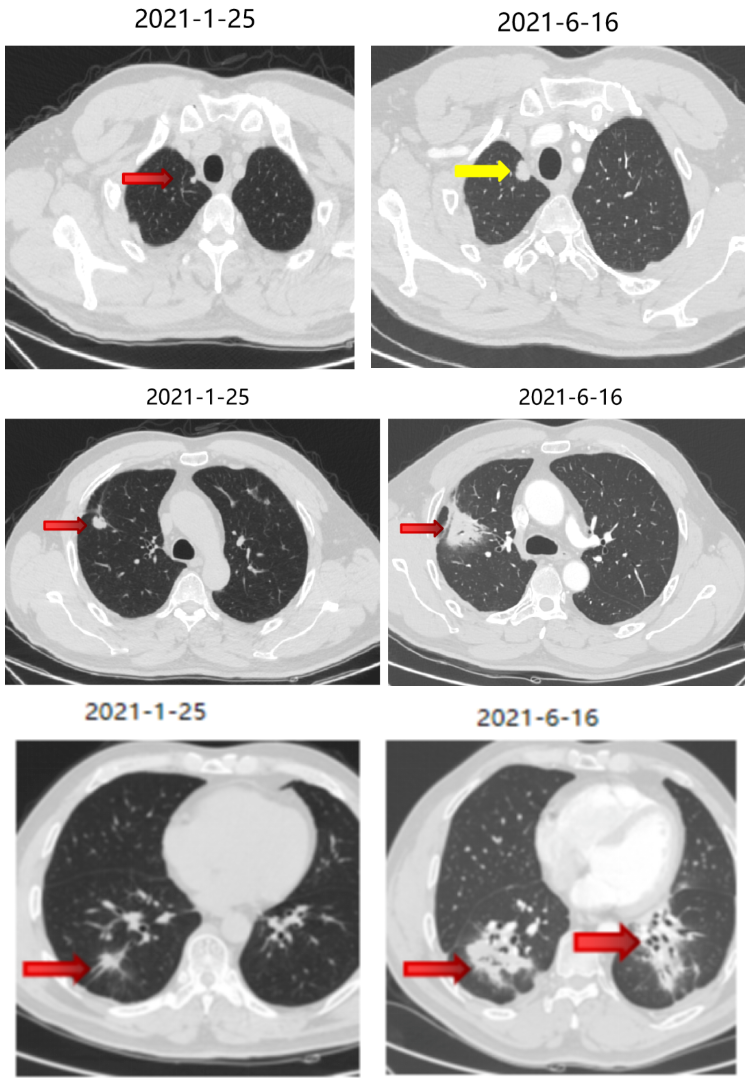
四线治疗
2021-6-17 起口服曲氟尿苷替匹嘧啶片(TAS-102)40mg bid。
四线治疗疗效:部分略减小,SD。
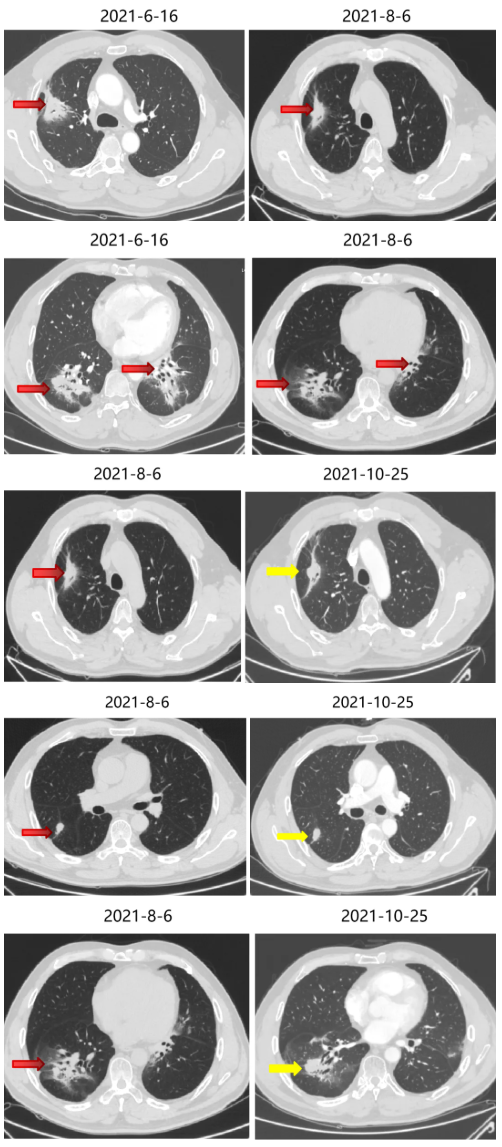
局部治疗(三):粒子植入
2021-10-29、2021-11-1 行CT引导下双肺转移灶放射性碘125粒子植入术。
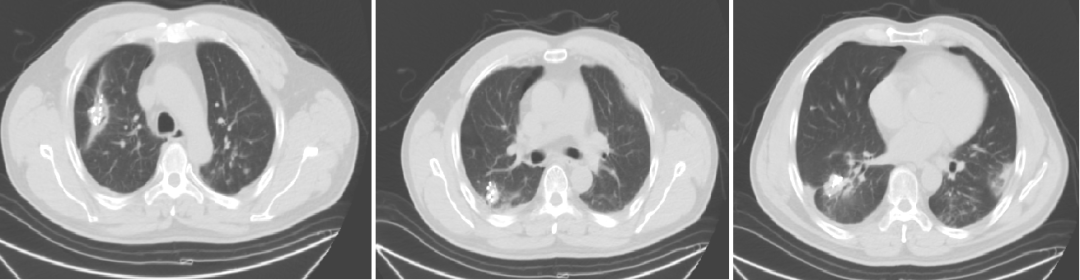
五线治疗
继续曲氟尿苷替匹嘧啶片(TAS-102)40mg bid+瑞戈非尼40mg qd(2021-11始)至今。
五线治疗疗效:病灶控制良好。
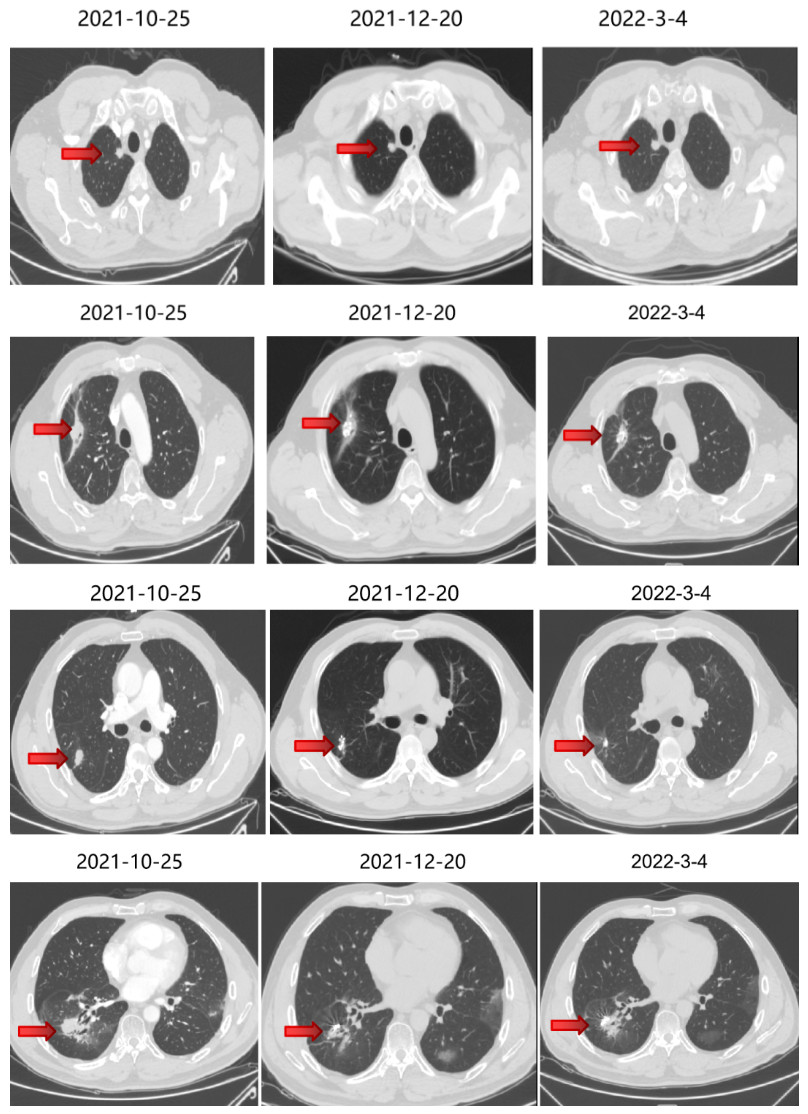
局部治疗(四):粒子植入
2022-4-13、2022-4-15 行CT引导下双肺转移灶放射性碘125粒子植入术。
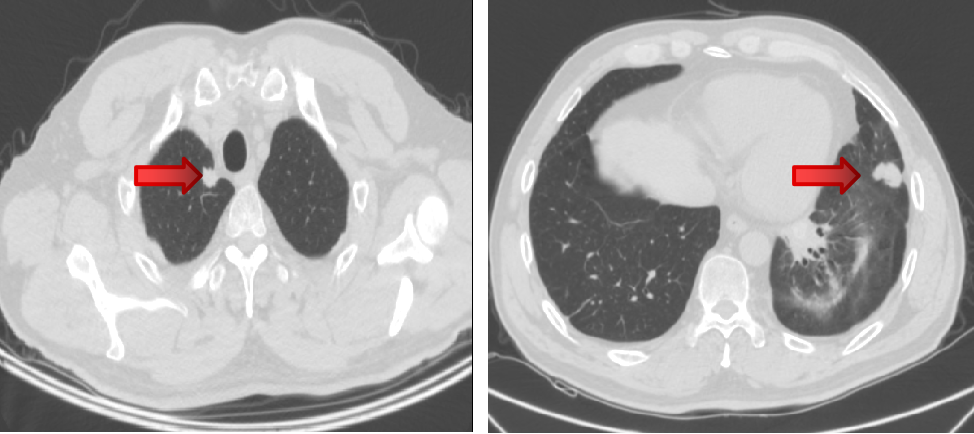
2022-4-21 肺转移组织基因检测。
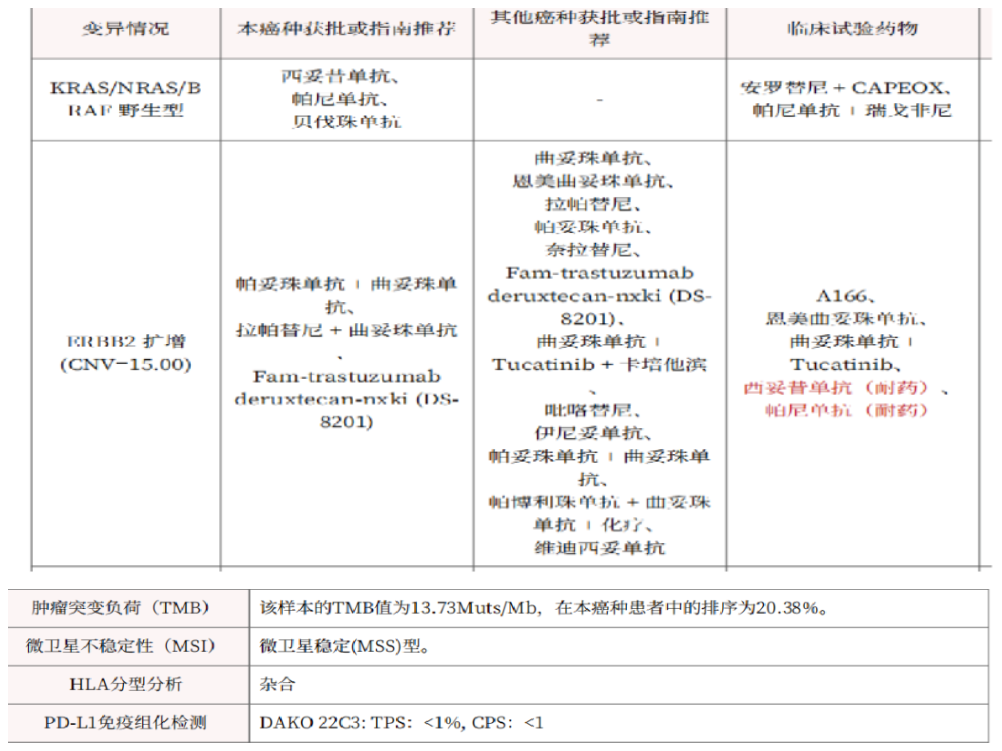
4 目前状况
患者ECOG PS 1分,多程多线治疗耐受性良好,未出现高血压、蛋白尿、骨髓抑制等不良反应。
血常规、肝肾功能及肿瘤标志物无明显异常。
5 病程总结
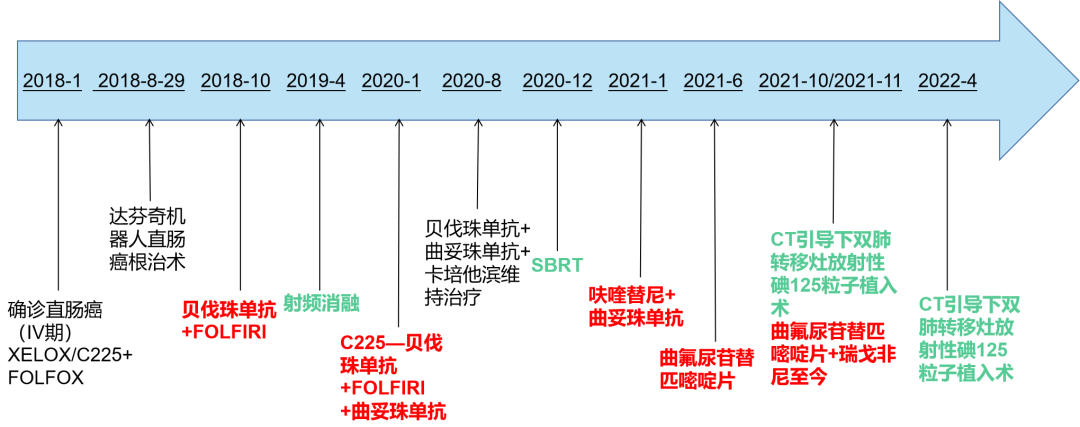
PFS 1:15个月 ,PFS 2:12个月,PFS 3:5个月,PFS 4:5个月,PFS 5(目前):6.5个月,OS(目前):51.5个月。
6 病例特点及思考
1. 患者体质条件较好,抗肿瘤治疗耐受性好,治疗依从性良好;
2. 患者转移灶局限于双肺,未出现其他远处转移灶;
3. 患者HER-2基因扩增,后续可考虑针对HER-2的ADC药物。
mCRC各线治疗合理排兵布阵,或可使患者长期生存;合理有效的全身治疗方案基础上适时联合局部治疗手段,或可延缓药物耐药时间,使PFS转换为OS。
*本文仅代表专家观点,并经专家审校。