2025年6月13日,同济大学附属东方医院周彩存教授在The Lancet Oncology发表舒格利单抗对比安慰剂联合铂类化疗一线治疗转移性非小细胞肺癌(NSCLC)的4年生存结局——一项双盲,随机,3期临床研究(GEMSTONE-302),题为“Sugemalimab versus placebo, in combination with platinum-based chemotherapy, as first-line treatment of metastatic non-small-cell lung cancer (GEMSTONE-302): 4-year outcomes from a double-blind, randomised, phase 3 trial”。研究结果显示,与安慰剂+化疗相比,舒格利单抗+化疗一线治疗无已知EGFR、ALK、ROS1或RET基因组敏感突变的NSCLC患者显示出优越的长期总生存获益。研究结果进一步夯实了舒格利单抗联合铂类化疗作为鳞状与非鳞状转移性NSCLC标准一线治疗方案的临床价值,同时其安全性特征亦保持可控。
免疫检查点抑制剂联合化疗已成为晚期非小细胞肺癌(NSCLC)的标准一线治疗。尽管多项抗PD-1抗体联合化疗的3期随机试验报告了4年或5年的临床生存结局,但特定亚组人群(包括PD-L1表达<1%、鳞状组织学或基线脑转移的患者)的长期生存仍然欠佳。尽管抗PD-L1抗体联合铂类化疗已显示出无进展生存期(PFS)获益,但与单纯化疗相比,抗PD-L1抗体带来的总生存改善有限。PD-L1联合化疗的长期生存数据仍不明确。
舒格利单抗(Sugemalimab,CS1001)是一种全长、全人源免疫球蛋白G4(s228p)抗PD-L1单克隆抗体。不同于其他含有减弱或消除Fc功能的PD-L1单抗,舒格利单抗保留了与Fcγ受体I的结合能力,可通过将PD-L1阳性肿瘤细胞与巨噬细胞交联,实现抗体依赖性细胞吞噬作用。
随机3期GEMSTONE-302试验评估了舒格利单抗联合化疗在既往未经治疗、无已知EGFR、ALK、ROS1或RET突变的转移性非鳞状或鳞状NSCLC患者中的疗效。结果显示,与安慰剂联合化疗相比,舒格利单抗联合化疗的患者的PFS和OS均显著改善(中位PFS:9.0个月 vs 4.9个月,HR=0.48,95%CI 0.39-0.60,P<0.0001;中位 OS:25.4个月 vs 16.9个月,HR=0.65 95%CI 0.50-0.84,P=0.0008)。这些发现促使舒格利单抗联合铂类化疗于2021年获NMPA批准用于无EGFR突变或ALK突变的转移性鳞状与非鳞状NSCLC的一线治疗。该方案随后于2024年在欧盟和英国获批,用于无EGFR敏感突变或无ALK、ROS1、RET基因组肿瘤突变的成人转移性NSCLC的一线治疗。
这项随机、双盲、3期试验在中国35家医院及学术研究中心开展。研究主要终点为研究者评估的PFS;次要研究终点包括OS、盲态独立中心评估(BICR)的PFS,PD-L1≥1%患者的PFS,客观缓解率(ORR),中位缓解持续时间(DOR)和安全性等。本文报告GEMSTONE-302研究事后4年疗效和安全性结局(2023年5月15日结束后所有患者均已中止治疗)。
2018年12月13日-2020年5月15日期间,479例患者被随机分配至舒格利单抗组(n=320)和安慰剂组(n=159)。截至数据截止时间2023年5月15日,舒格利单抗组的中位随访时间为43.5个月(IQR 41.2–46.9),安慰剂组为43.0个月(40.7–44.8);舒格利单抗组的中位治疗时间为7.2个月(4.2–18.8),安慰剂组为4.6个月(2.8–6.9)。
中位PFS:舒格利单抗组为9.0个月(95%CI 7.4–10.9),安慰剂组为4.9个月(95%CI 4.8–5.2)(HR=0.49,95%CI 0.39–0.60)。
中位OS:舒格利单抗组为25.2个月(95%CI 20.1–30.2),而安慰剂组为16.9个月(95%CI 12.8–20.7)(HR=0.68,95%CI 0.54–0.85)。
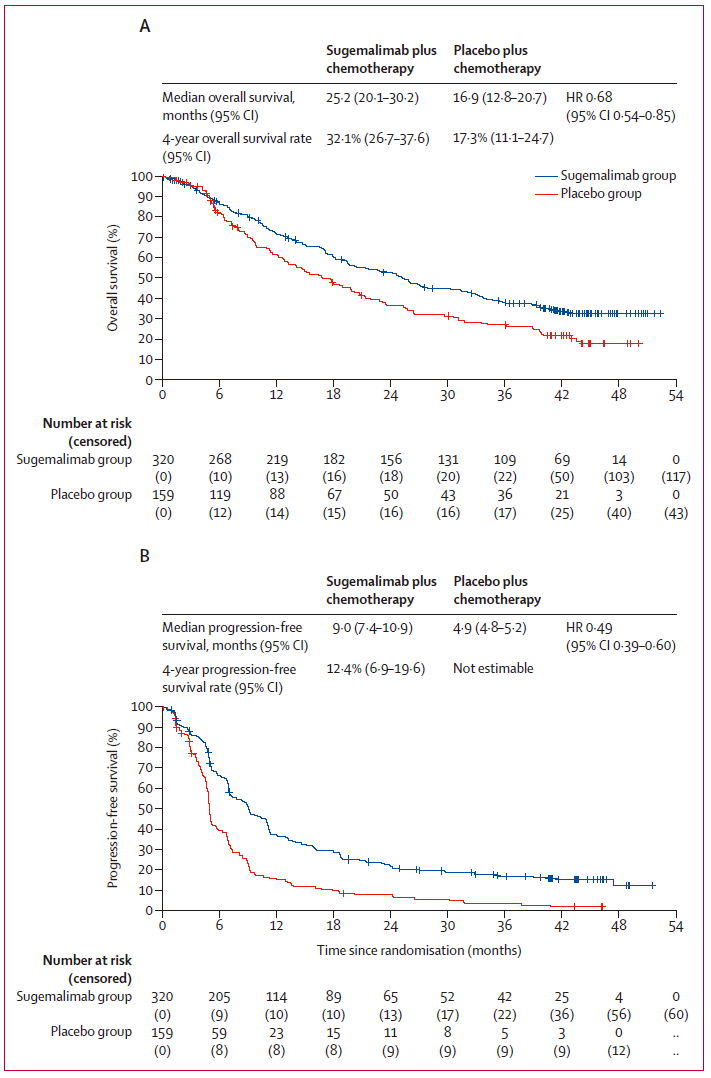
研究者评估的PFS和OS
在不同肿瘤组织学类型亚组分析中,舒格利单抗组较安慰剂组均展现出OS获益。鳞状NSCLC患者中舒格利单抗组的4年OS为27.6%(95%CI 19.8-35.8),而安慰剂组为11.7%(95%CI 3.9-24.3);非鳞状NSCLC患者中舒格利单抗组的4年OS为35.5%(95%CI 28.3-42.8),安慰剂组为20.2%(95%CI 12.1-29.9)。
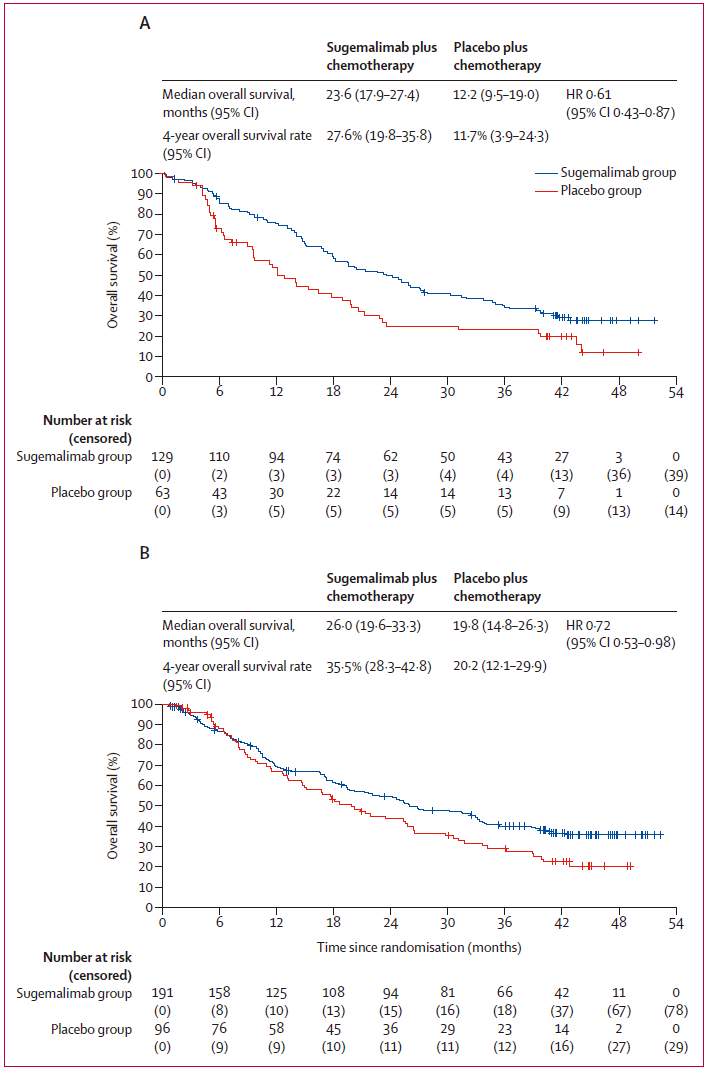
OS(A:鳞状NSCLC,B:非鳞状NSCLC)
在PD-L1表达水平不同的亚组分析中,舒格利单抗组较安慰剂组也展现出OS获益。舒格利单抗组与安慰剂组的4年OS分别为:
PD-L1≥50%:45.3%(95%CI 35.0-55.0)vs 20.1%(95%CI 9.1-34.3)
1<PD-L1<49%:29.3%(95%CI 19.6-39.7)vs 不可估计(不超过17.4%;95%CI 不可估计-不可估计)
PD-L1<1%:23.2%(95%CI 15.9-31.3)vs 16.6%(95%CI 8.2-27.6)
PD-L1≥1%:37.7%(95%CI 30.4-44.9)vs 17.4%(95%CI 9.4-27.4)
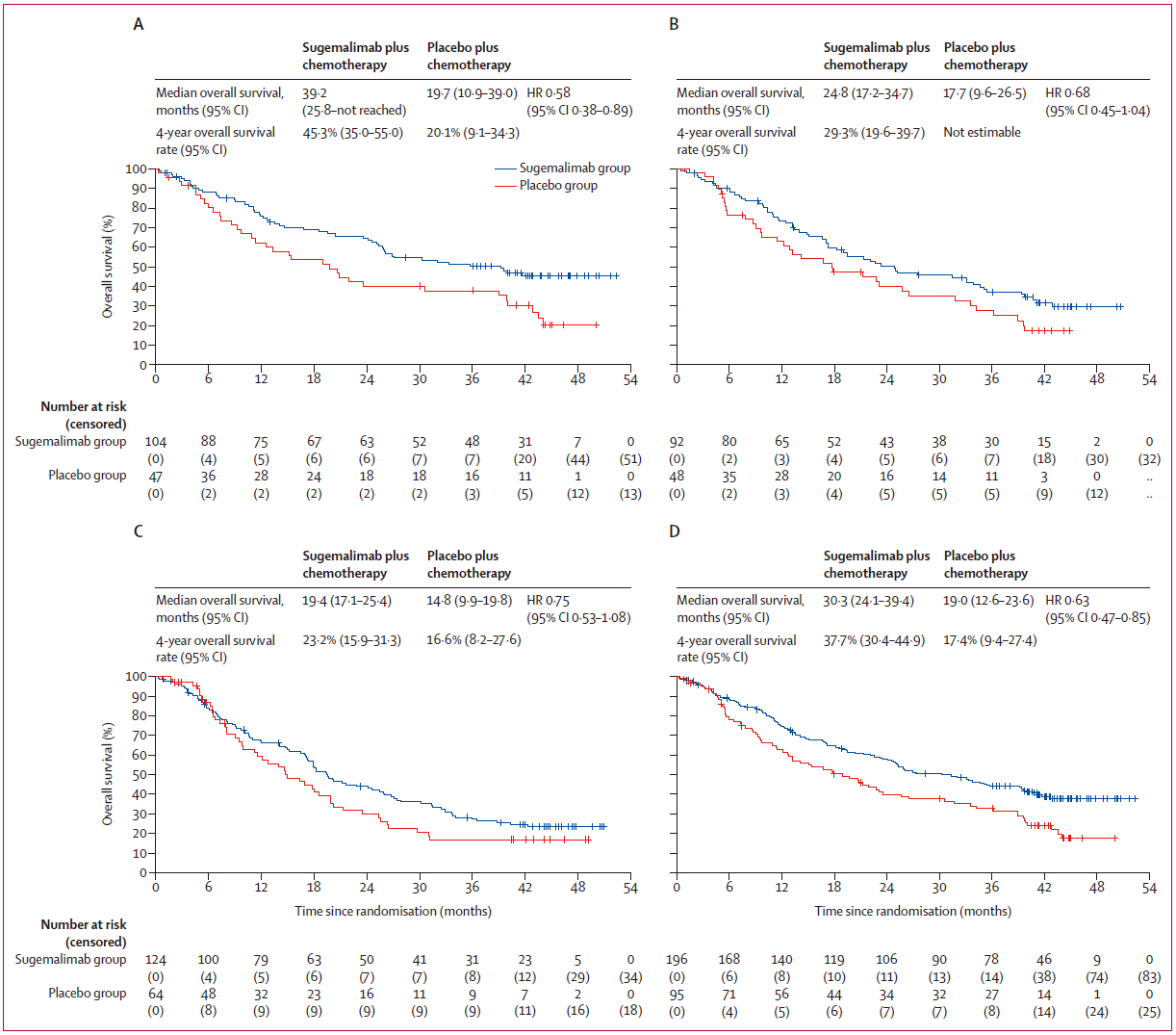
OS(A:PD-L1≥50%,B:1<PD-L1<49%, C:PD-L1<1,D:PD-L1≥1)
基线脑转移:与安慰剂组相比(n=17),舒格利单抗组(n=50)在基线脑转移患者中显示出生存获益。在基线脑转移患者中,舒格利单抗组与安慰剂组的OS分别为:
中位OS:26.0个月(95%CI 12.4-未达到)vs 9.0个月(95%CI 5.2-20.8)(HR=0.44,95%CI 0.24-0.81)
3年OS:39.0%(95%CI 25.3-52.6)vs 11.8%(95%CI 2.0-31.2)
4年OS:36.4%(95%CI 22.9-50.1)vs 不可估计(不超过5.9%;95%CI不可估计)
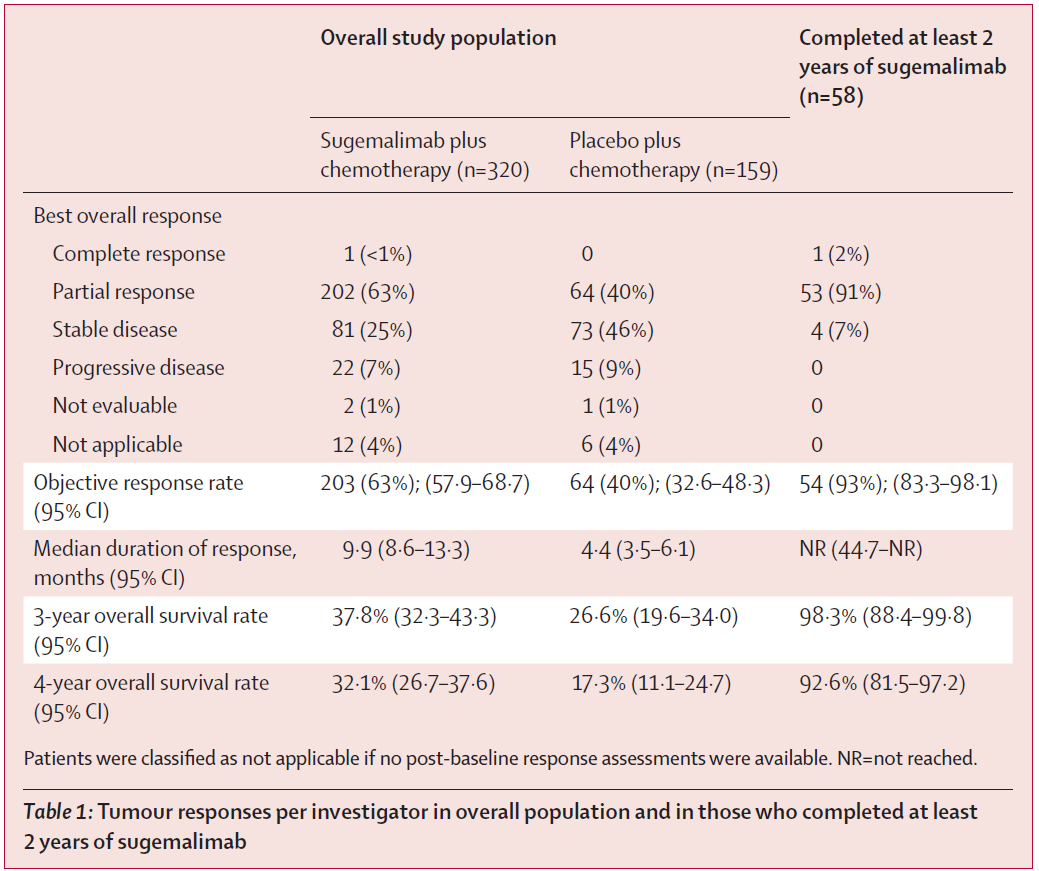
疗效数据
安全性:99%(317/320)舒格利单抗组患者 vs 96%(153/159)安慰剂组患者出现任何级别治疗相关不良事件。56%(180/320)舒格利单抗组患者 vs 57%(90/159)安慰剂组患者出现3-4级治疗相关不良事件。未发现新的安全性信号。
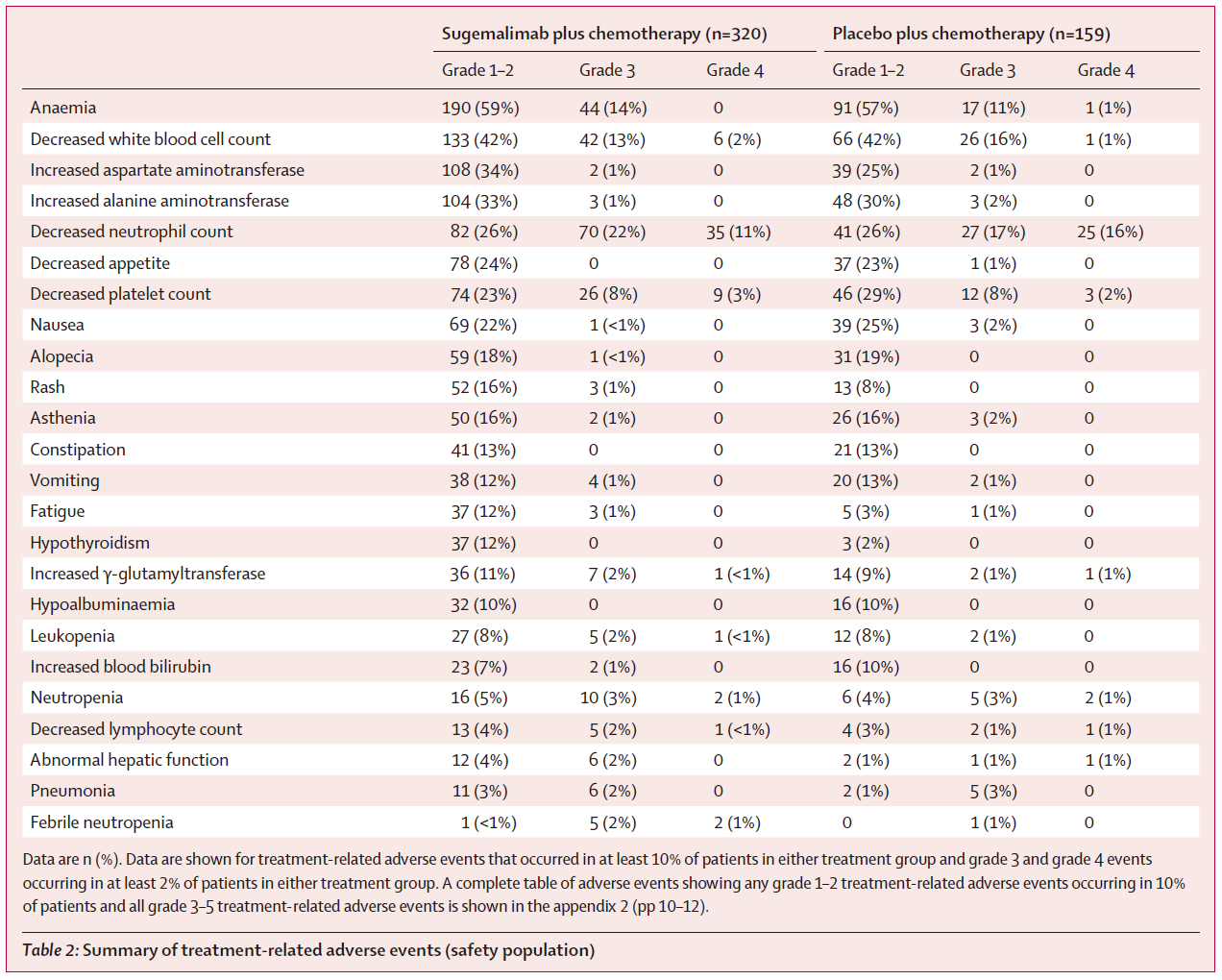
安全性数据
据目前所知,GEMSTONE-302研究是首个通过单次随机双盲3期试验证实 PD-L1抑制剂(舒格利单抗)联合铂类化疗在一线治疗鳞状及非鳞状NSCLC 时,均能显著改善PFS和OS的临床研究。该方案凭借持续的生存获益、可控的安全性特征,以及对脑转移等传统高危人群的临床获益覆盖能力,已成为NSCLC一线治疗的优选方案。值得关注的是,GEMSTONE-302研究也是当前唯一在初治NSCLC患者中积累了长期安全性和生存数据的抗PD-L1联合化疗方案。
来源:肿瘤界