近日,四川大学华西医院临床试验中心郑莉教授团队在Signal Transduction and Targeted Therapy发表文章“Multicenter phase 1/2 study of onatasertib, a dual TORC1/2 inhibitor, combined with the PD-1 antibody toripalimab in advanced solid tumors”。该论文首次揭示了mTORC1/2双重抑制剂Onatasertib联合特瑞普利单抗,在晚期实体瘤特别是宫颈癌中的安全性和初步疗效,为mTOR信号通路抑制剂联合检查点抑制剂治疗作为晚期实体瘤治疗的新策略提供了科学依据。

尽管免疫检查点抑制剂(如PD-1/PD-L1抗体)在多种实体瘤治疗中取得了突破,但单药治疗患者的获益有限。PI3K-AKT-mTOR信号通路的异常激活在肿瘤细胞增殖和存活中起关键作用,因此mTOR抑制剂目前正被开发为多种肿瘤的潜在治疗药物。然而,第一代靶向mTORC1的抑制剂可能导致AKT的反馈激活,而对mTORC2耐药。第二代mTOR抑制剂能够同时抑制mTORC1和mTORC2。临床前研究提示,mTORC1/2抑制剂可调节免疫微环境,并与免疫治疗具有协同增效作用,但未被临床证实。该研究前瞻性地首次探索出双重mTORC1/2抑制剂onatasertib联合PD-1抗体特瑞普利单抗在晚期实体瘤中安全治疗方案,并发现了宫颈癌等优势适应症。
该研究分为剂量探索和剂量拓展两个阶段。在剂量递增阶段,应用“3+3”设计探索15/20/30 mg onatasertib联合固定剂量特瑞普利的安全给药方案和初步疗效。在剂量拓展阶段对包括宫颈癌等优势瘤种进行了治疗方案进一步确认和临床疗效的初步验证(NCT04337463),每6周用RECIST 1.1标准评估肿瘤反应,对PD-L1表达(TPS≥1%为阳性)进行了分层分析。
研究共纳入46例既往接受2线治疗的晚期实体瘤患者(其中45.7%宫颈癌),考察治疗方案的安全性、耐受性、客观缓解率(ORR)、疾病控制率(DCR)、无进展生存期(PFS)、药代动力学(PK)特征及PD-L1表达相关性。
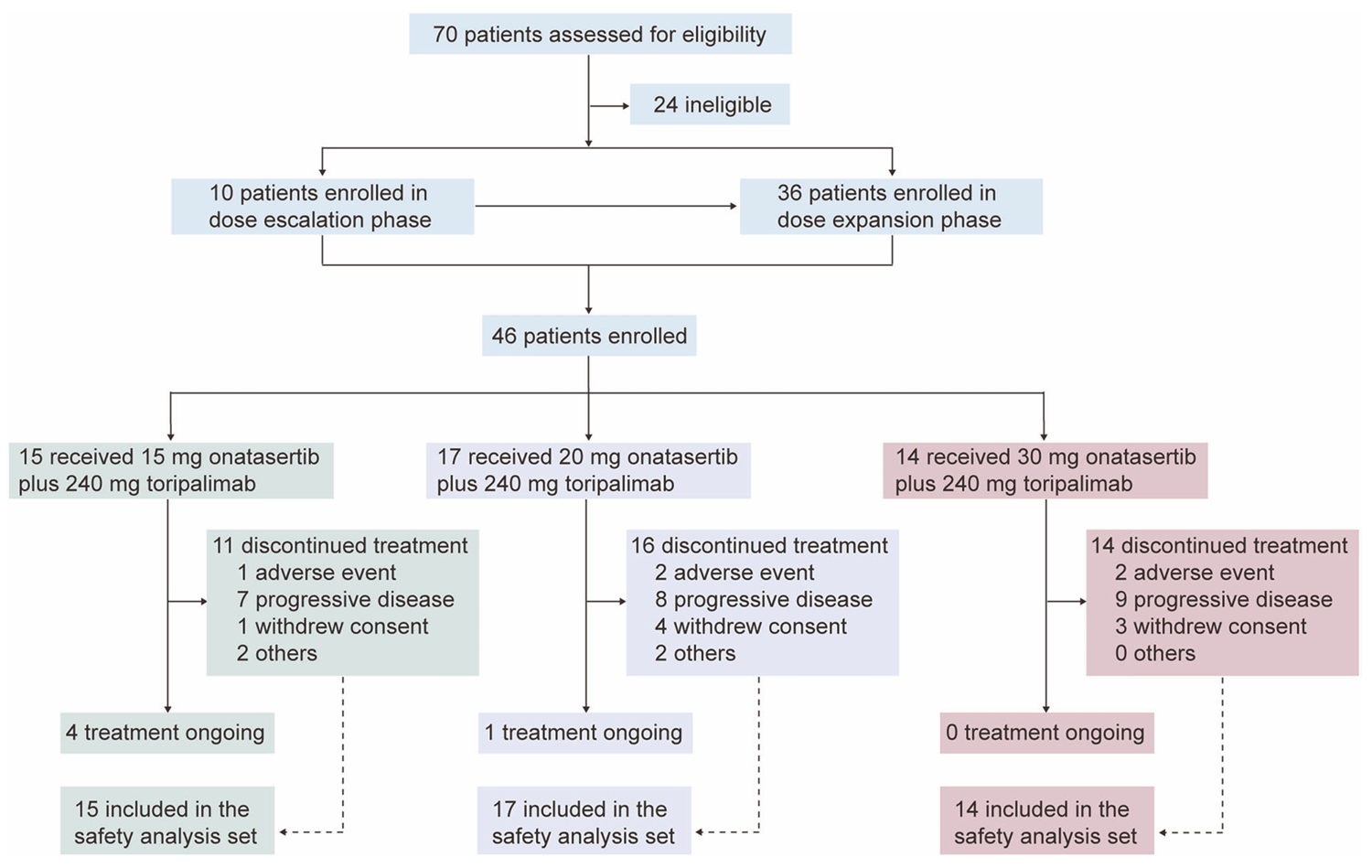
流程图
总体疗效:ORR为26.1%,DCR为73.9%,中位PFS为4.3个月,显示出联合疗法的初步抗肿瘤活性。
宫颈癌亚组:ORR 52.4%(PD-L1⁺:66.7% vs PD-L1⁻:41.7%),中位PFS 5.8个月;特别是在PD-L1阴性宫颈癌患者中ORR达41.7%,突破免疫单药治疗局限。
15 mg剂量组:中位PFS达7.8个月,治疗持续时间长达43.6周,显示出更优的生存获益与耐受性。
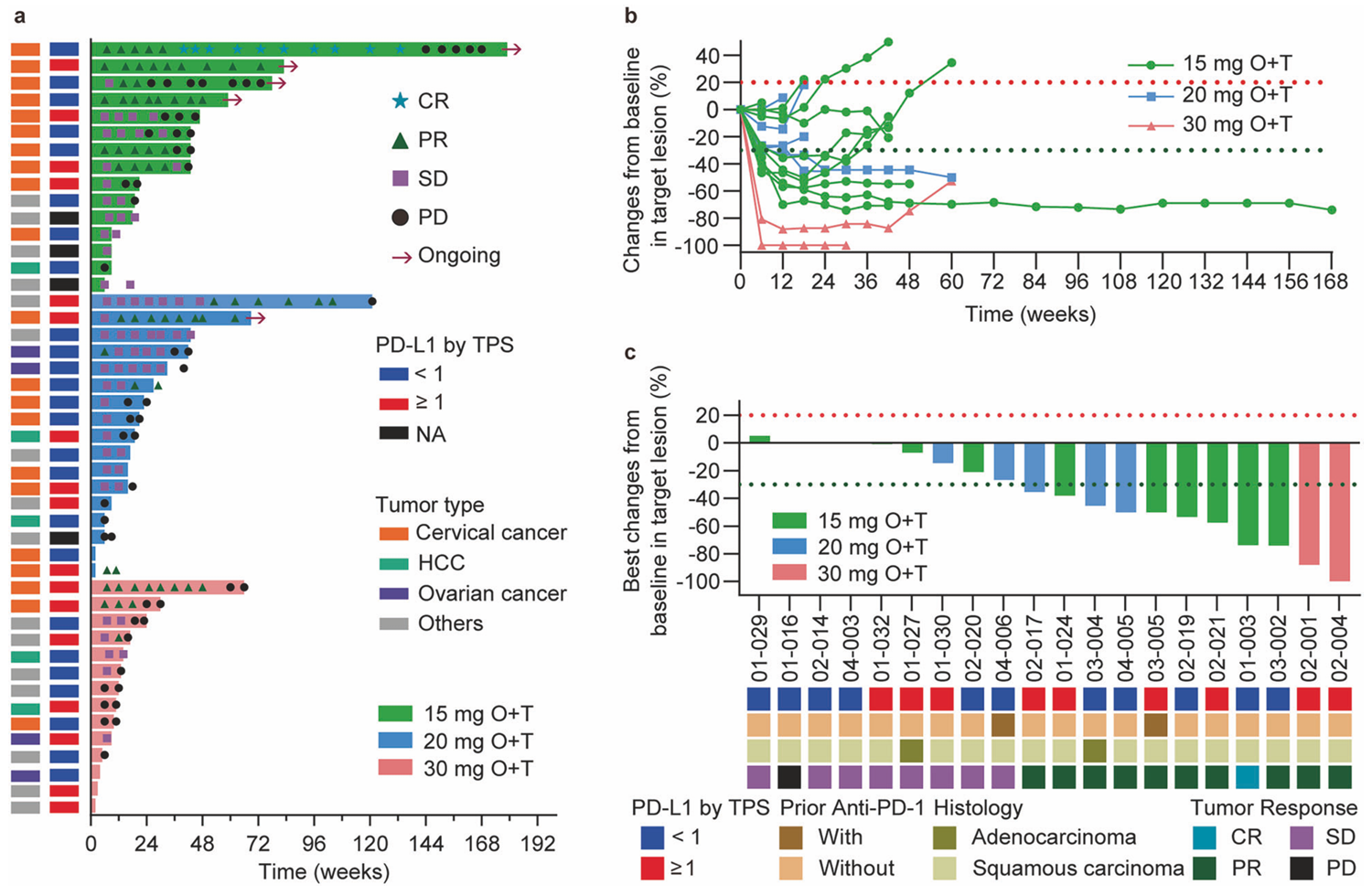
onatasertib和特瑞普利联合治疗疗效分析
a.46例患者按肿瘤类型分组的治疗持续时间、最佳总体反应及进展时间
b.宫颈癌患者靶病灶的反应随时间的变化
c.宫颈癌患者靶病灶的最佳反应
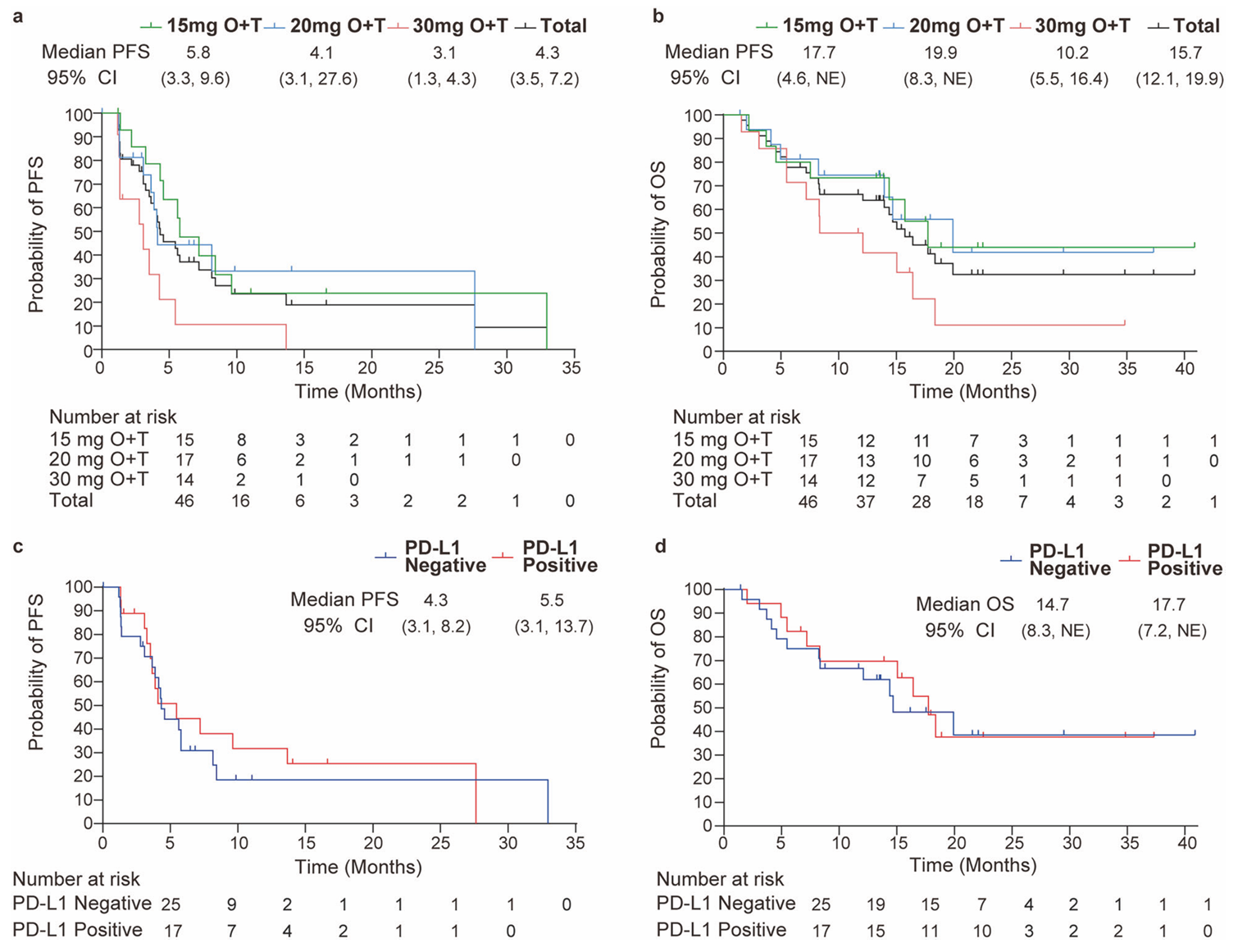
onatasertib和特瑞普利联合治疗的生存分析
(a,b)三个剂量组的PFS和OS
(c,d)按PD-L1状态分层的PFS和OS分析
该研究工作在晚期实体瘤患者中阐明了mTORC1/2双重抑制剂onatasertib联合特瑞普利单抗的安全性是可控的,并且在晚期实体瘤中显示出令人欣喜的临床活性,尤其是在宫颈癌患者中的疗效不受PD-L1表达的限制。这一重要发现为既往难以从免疫治疗中获益的宫颈癌患者提供了新的治疗选择,具有重要的临床意义。
来源:四川大学华西医院官网、华西医学时间官微