2025年8月9日,国际顶级期刊Lancet(《柳叶刀》)在线发表了题为“Adagrasib versus docetaxel in KRASG12C-mutated non-small-cell lung cancer (KRYSTAL-12): a randomised, open-label, phase 3 trial”的3期临床试验结果。该研究由上海交通大学附属胸科医院陆舜教授、香港中文大学莫树锦教授、四川省肿瘤医院姚文秀教授等全球22国230家中心研究者共同完成,首次在3期试验中证实,与传统化疗药物多西他赛相比,KRASG12C抑制剂Adagrasib可显著延长经治KRASG12C突变晚期非小细胞肺癌(NSCLC)患者的无进展生存期,且具有更优的客观缓解率和颅内活性,安全性可控。这一成果为KRASG12C突变NSCLC的靶向治疗提供了高级别循证医学证据。
研究背景
Kirsten大鼠肉瘤病毒基因同源物(KRAS)是人类癌症中最常见的致癌驱动基因之一,其中KRASG12C突变在肺腺癌中发生率约为14%,在亚洲NSCLC患者中占4%。长期以来,KRASG12C突变NSCLC因缺乏有效靶向药物被视为“难治性亚型”,患者在经化疗/免疫治疗进展后可选治疗方案有限,传统化疗药物多西他赛是此类患者的标准治疗方案。近年来,KRASG12C特异性抑制剂的研发取得突破,如Sotorasib和Adagrasib。
Adagrasib是一种强效、口服、小分子、共价KRASG12C抑制剂,能不可逆且选择性地与KRASG12C在非活性的GDP结合状态下结合。Adagrasib具有良好的药代动力学特性,半衰期长达23小时、剂量依赖性PK、可穿透血脑屏障。在2期KRYSTAL-1研究(NCT03785249)中,Adagrasib在经治KRASG12C突变NSCLC患者中表现出良好的临床活性(客观缓解率[ORR]达43%,中位无进展生存期[mPFS]6.5个月,中位总生存期[mOS] 12.6个月),基于此获美国加速批准和欧盟附条件批准。
在1/2期KRYSTAL-1研究的汇总队列中(随访时间更长,为2年),Adagrasib的mOS为14.1个月(2年OS率为31%),长期安全性特征可控。Adagrasib在稳定、经治脑转移及未经治脑转移NSCLC患者中显示出有前景的颅内活性。因此,Adagrasib被NCCN指南(2a类)、ESMO指南列为推荐方案,用于经治晚期KRASG12C突变NSCLC患者(包括脑转移)。本文报告了验证性、随机、开放标签、3期KRYSTAL-12试验(NCT04685135)的主要分析结果,该试验评估了Adagrasib与多西他赛在既往接受化疗和免疫治疗的KRASG12C突变晚期NSCLC患者中的疗效。
研究内容
KRYSTAL-12是一项在22个国家的230家中心开展的随机、多中心、开放标签的3期试验。2021年2月-2023年11月纳入全球453例经治KRASG12C突变局部晚期/转移性NSCLC患者患者,按2:1比例随机分配至Adagrasib组(n=301)或多西他赛组(n=152)。主要终点为所有随机化患者(意向性治疗[ITT]人群)中经盲态独立中心评估(BICR)的PFS。安全性评估对象为所有接受治疗的患者。
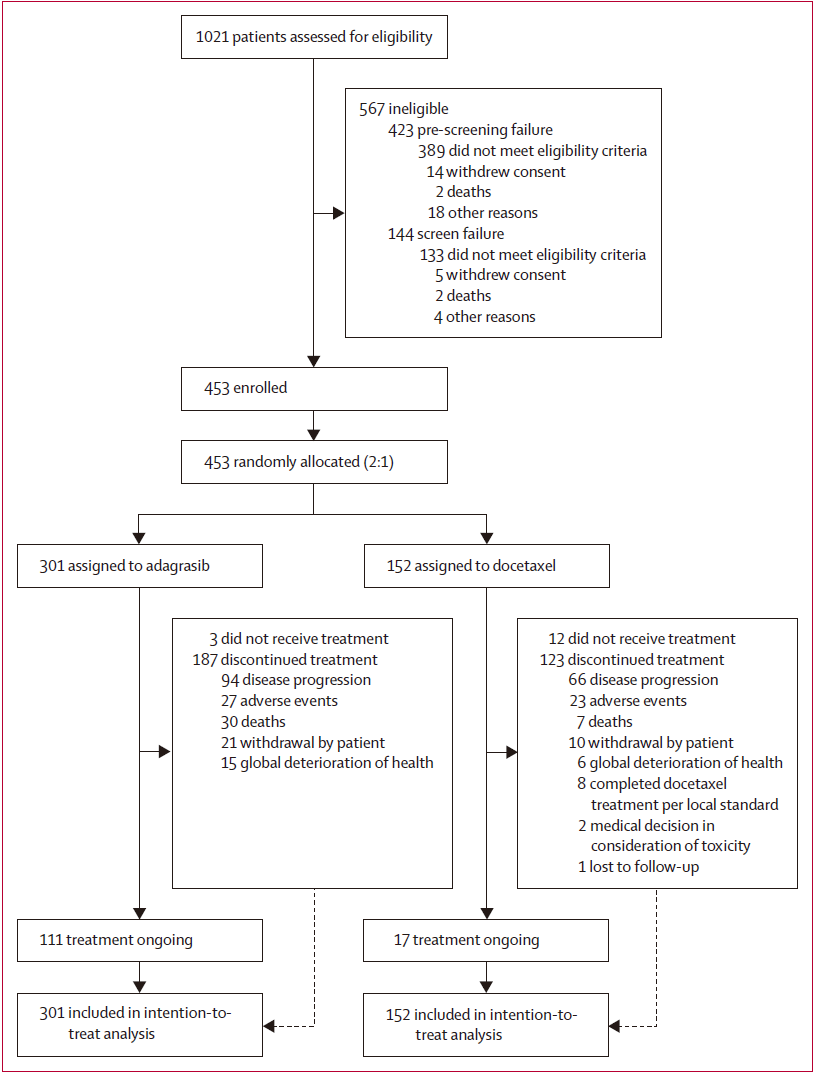
试验概况
PFS
在ITT人群中(中位随访时间为7.2个月[95%CI 5.8–8.7]),Adagrasib组中位PFS为5.5个月(95%CI 4.5-6.7),显著优于多西他赛组的3.8个月(95%CI 2.7-4.7),疾病进展或死亡风险降低42%(HR=0.58,95%CI 0.45-0.76,P<0.0001)。
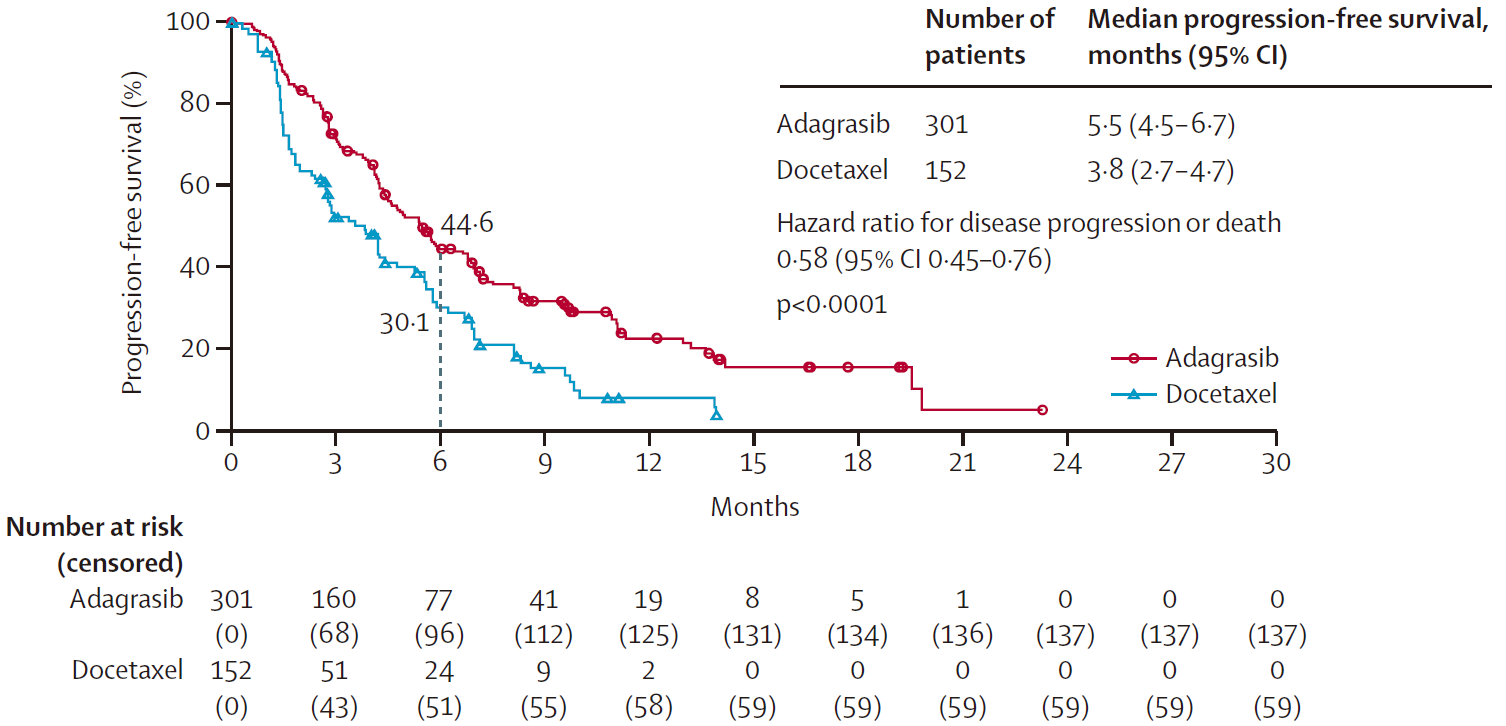
ITT人群PFS
所有患者亚组(包括基线时脑转移的患者)中,Adagrasib相较于多西他赛的PFS改善一致。
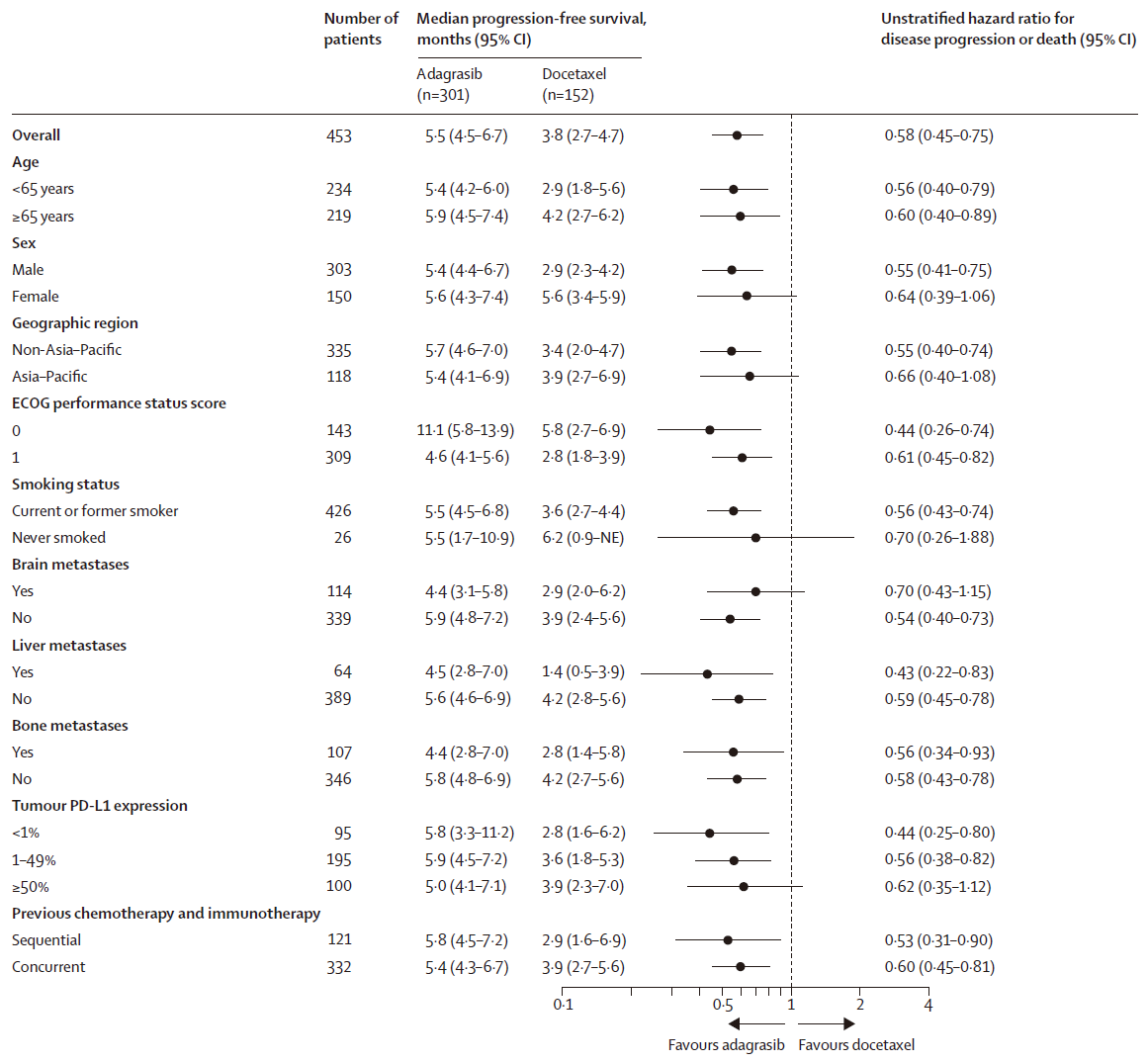
亚组PFS
ORR、疾病控制率(DCR)
Adagrasib组ORR为32%(95%CI 26.7-37.5,包括1%完全缓解[CR]和31%部分缓解[PR]),显著高于多西他赛组的9%(仅PR,95%CI 5.1-15.0),比值比(ORR)为4.68(95%CI 2.56-8.56,P<0.0001)。
Adagrasib组DCR为78%,同样优于多西他赛组的59%。此外,Adagrasib组的缓解持续时间(DOR)更长(中位DOR:8.3个月 vs 5.4个月),75%的患者实现肿瘤缩小,而多西他赛组为47%。
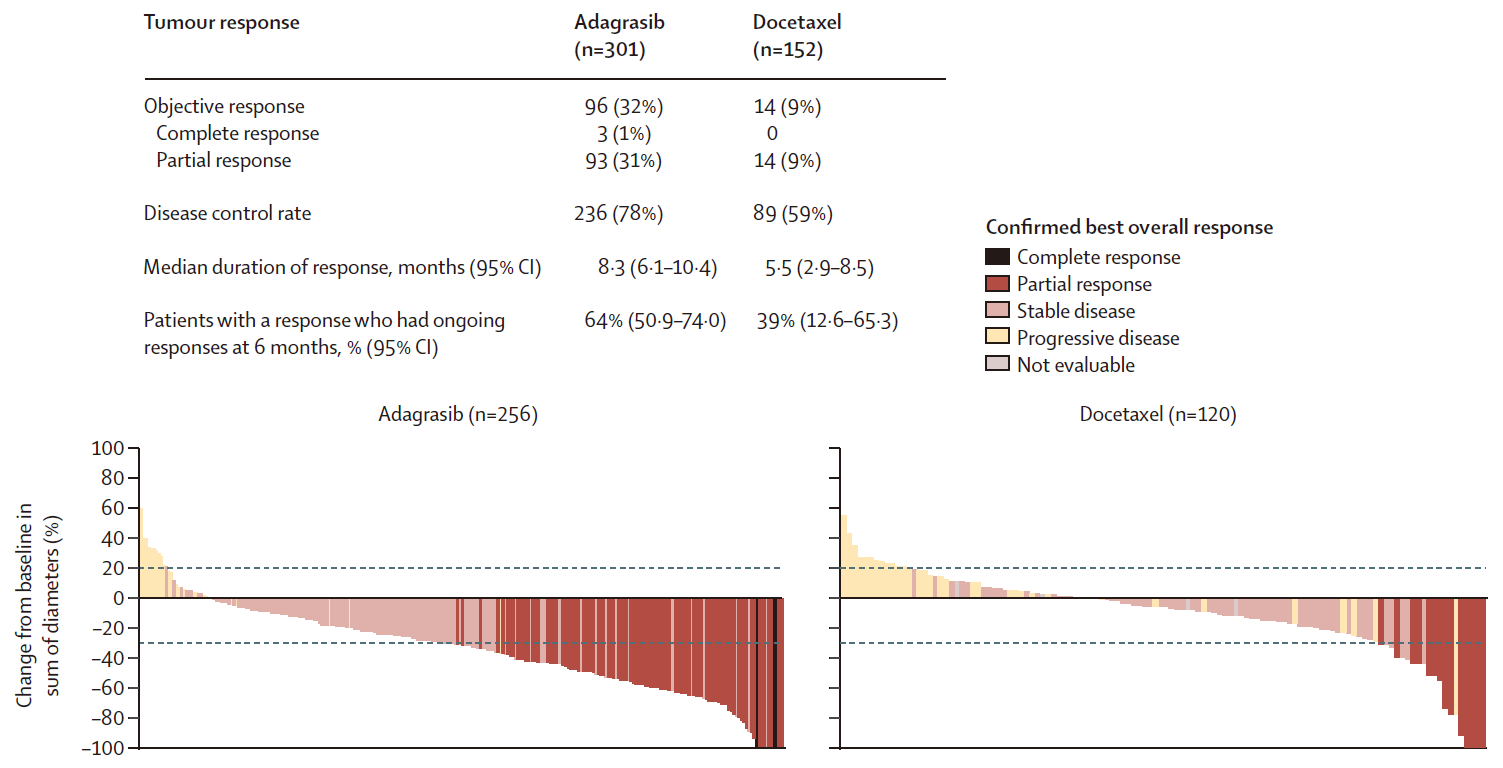
ORR、DCR、DOR、肿瘤直径较基线变化
在所有患者亚组中,Adagrasib相较于多西他赛的ORR改善一致,包括基线脑转移患者。
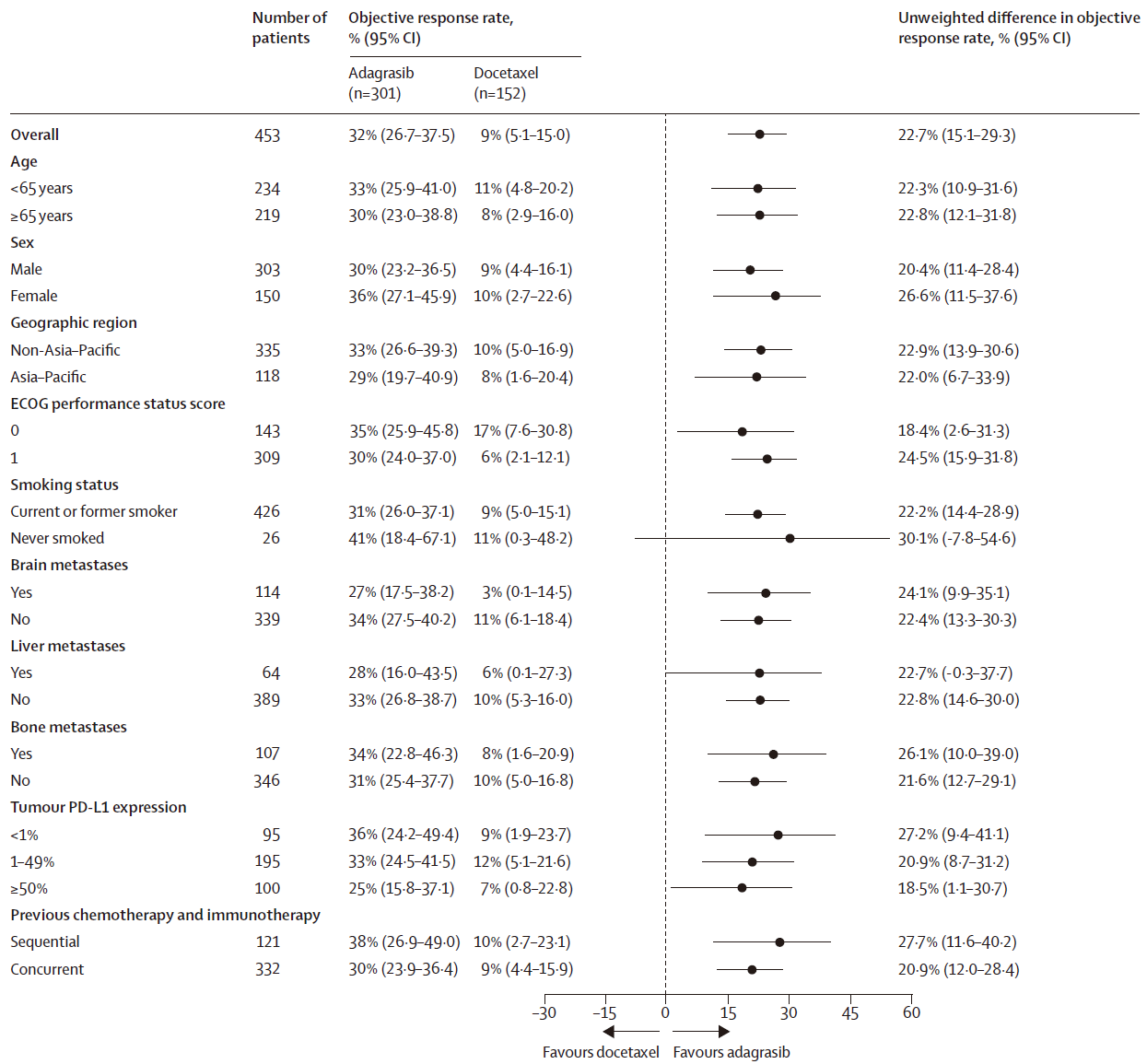
亚组ORR
颅内缓解
基线脑转移患者中(Adagrasib组78例,多西他赛组36例),
颅内ORR:Adagrasib组为24%(CR:14%),多西他赛组为11%(CR:8%)
颅内DCR:Adagrasib组为82%,多西他赛组为56%
在存在可测量脑转移灶的亚组中,Adagrasib组颅内ORR达40%(10/25),多西他赛组仅11%(1/9)。
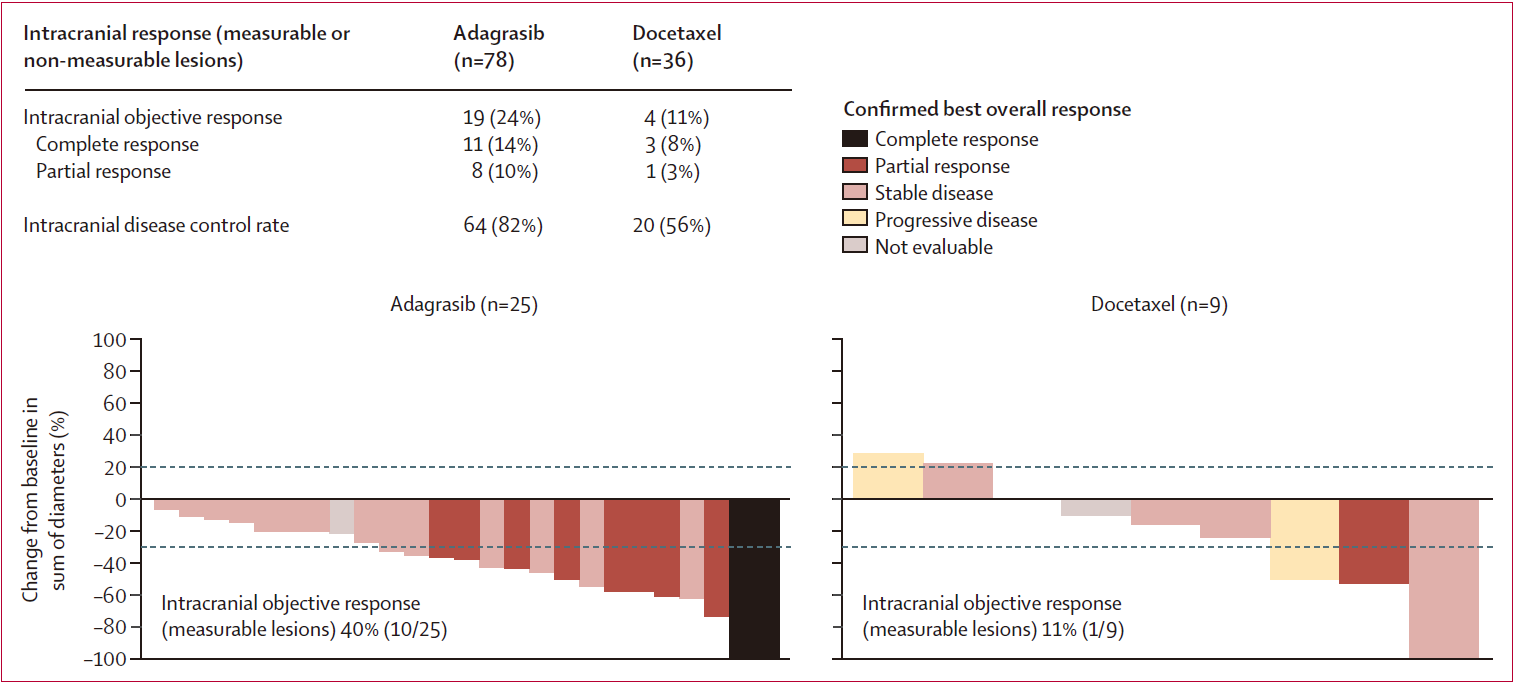
颅内缓解
安全性特征
安全性分析纳入298例Adagrasib组患者和140例多西他赛组患者:
任何级别治疗相关不良事件(TRAE):Adagrasib组280例(94%),多西他赛组121例(86%)
≥3级TRAE:Adagrasib组140例(47%),多西他赛组64例(46%)
治疗相关死亡:Adagrasib组4例(1%),多西他赛组1例(1%)
最常见TRAE:Adagrasib组为胃肠道反应(腹泻53%、呕吐35%、恶心34%,多为1级);多西他赛组为腹泻(31%)、贫血(30%)和乏力(27%)
值得注意的是,即使在免疫治疗结束后30天内启动Adagrasib治疗的患者中,肝酶升高风险未显著增加,无需强制洗脱期,更贴合临床实践。
免疫治疗30天内启动Adagrasib(n=22):18%出现ALT升高,23%出现AST升高
免疫治疗30天后启动Adagrasib(n=276):31%出现ALT升高,32%出现AST升高
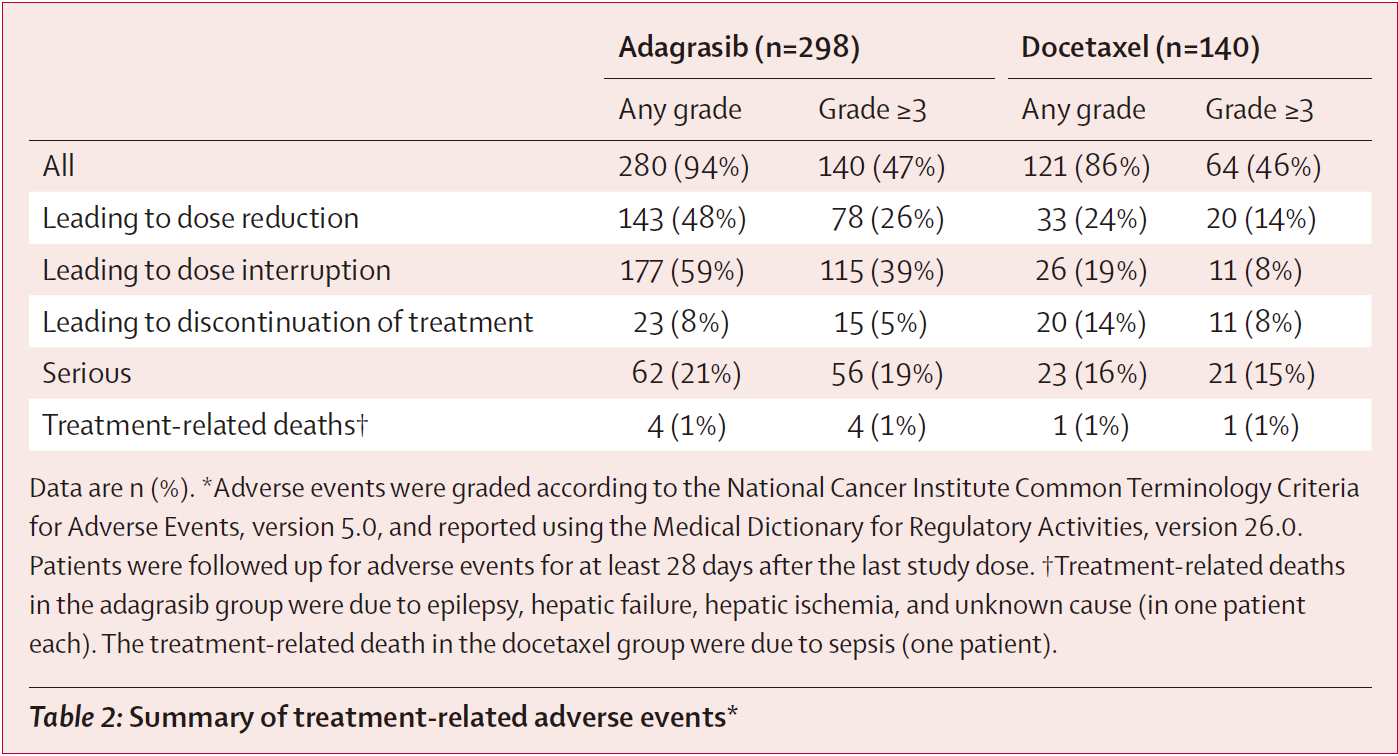
TRAE
总之,与多西他赛相比,Adagrasib显著改善了PFS和ORR,证实了KRYSTAL-1的初步结果,支持Adagrasib加速或有条件批准用于治疗KRASG12C突变晚期NSCLC患者。此外,Adagrasib在基线脑转移患者中显示出颅内活性。Adagrasib安全性特征可控,与既往报道一致。尽管目前缺乏总生存数据,但这些结果加强了Adagrasib作为KRASG12C突变晚期NSCLC患者在接受化疗/免疫治疗进展后的有效治疗选择。
目前,Adagrasib相关研究:KRYSTAL-21(NCT05853575)试验探索600mg vs 400mg每日两次的单药剂量优化;KRYSTAL-7(NCT04613596)和KRYSTAL-4(NCT06875310)试验则探索其联合帕博利珠单抗±化疗的一线治疗潜力。这些研究有望进一步拓宽 Adagrasib的应用场景,为KRASG12C突变NSCLC患者提供全程管理方案。
来源:肿瘤界