2025年9月19日,北京协和医学院赵海涛教授等研究团队在Cell Reports Medicine发表了题为“Therapeutic T cells with 3-in-1 strategy for the treatment of biliary tract cancer”的研究,提出了一种全新的“三合一”T细胞——超级循环肿瘤浸润淋巴细胞样T细胞(ScTILs)疗法,在部分晚期胆管癌患者中展现出卓越疗效,中位总生存期(mOS)达18.3个月,显著优于现有标准治疗,为实体瘤细胞治疗开辟了新路径。

近年来,嵌合抗原受体T(CAR-T)细胞疗法在血液肿瘤中取得显著疗效,但在实体瘤治疗中仍面临抗原异质性、肿瘤微环境(TME)抑制和T细胞扩增难三大瓶颈。尤其是胆管癌(BTC),恶性程度高、预后极差,早期诊断困难、治疗手段有限,晚期患者中位总生存期仅约12个月,亟需新的突破性治疗方案。
ScTILs是一种通过三大策略改造而成的“强化型T细胞”:
靶点筛选:从患者外周血中筛选出PD-1阳性T细胞(cTILs),这类细胞具有识别肿瘤异质性抗原的能力;
逆转抑制:引入“增强受体(ER)”,将肿瘤微环境中的PD-L1抑制信号转化为激活信号;
体内扩增:搭载靶向CD19的CAR结构(CFE),借助体内B细胞激活ScTILs,实现快速扩增。
简单来说,ScTILs同时具备“识别肿瘤、逆转抑制、自我扩增”三大能力,是一种真正意义上的“智能T细胞”。
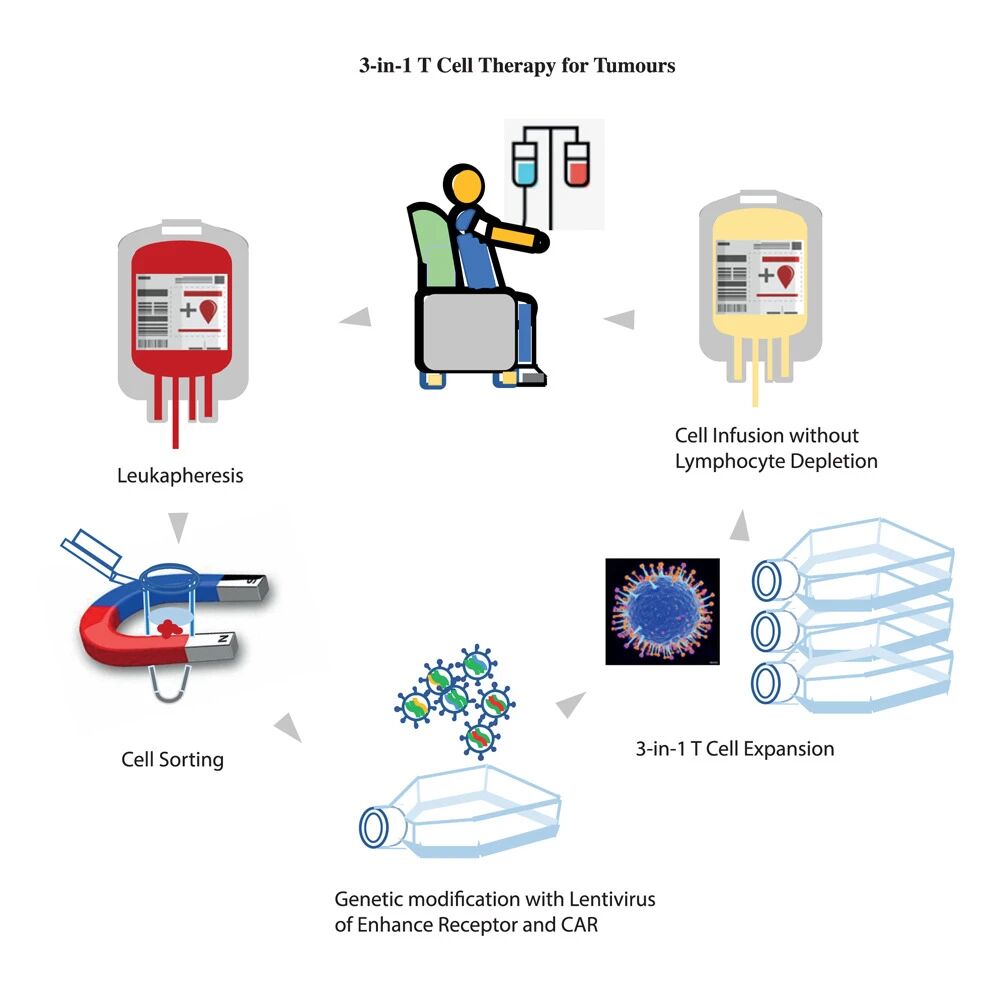
图形摘要
临床疗效数据
在该项I期临床试验中,共10例经治无效的晚期胆管癌患者接受ScTILs输注。研究结果显示:
在合适剂量(1×10⁸~5×10⁸细胞)或基线B细胞水平正常的患者(5/10)中,ScTIL 单药治疗的中位OS为18.3个月,而目前一线标准治疗(吉西他滨联合顺铂,GC方案)中位OS为11.7个月,GC联合PD-1抑制剂方案中位OS为12.7~12.8个月;
合适剂量组的6周和12周疾病控制率(DCR)分别为71%和43%,而高剂量组(1×10⁹细胞)因可能存在细胞耗竭,疗效反而不佳。
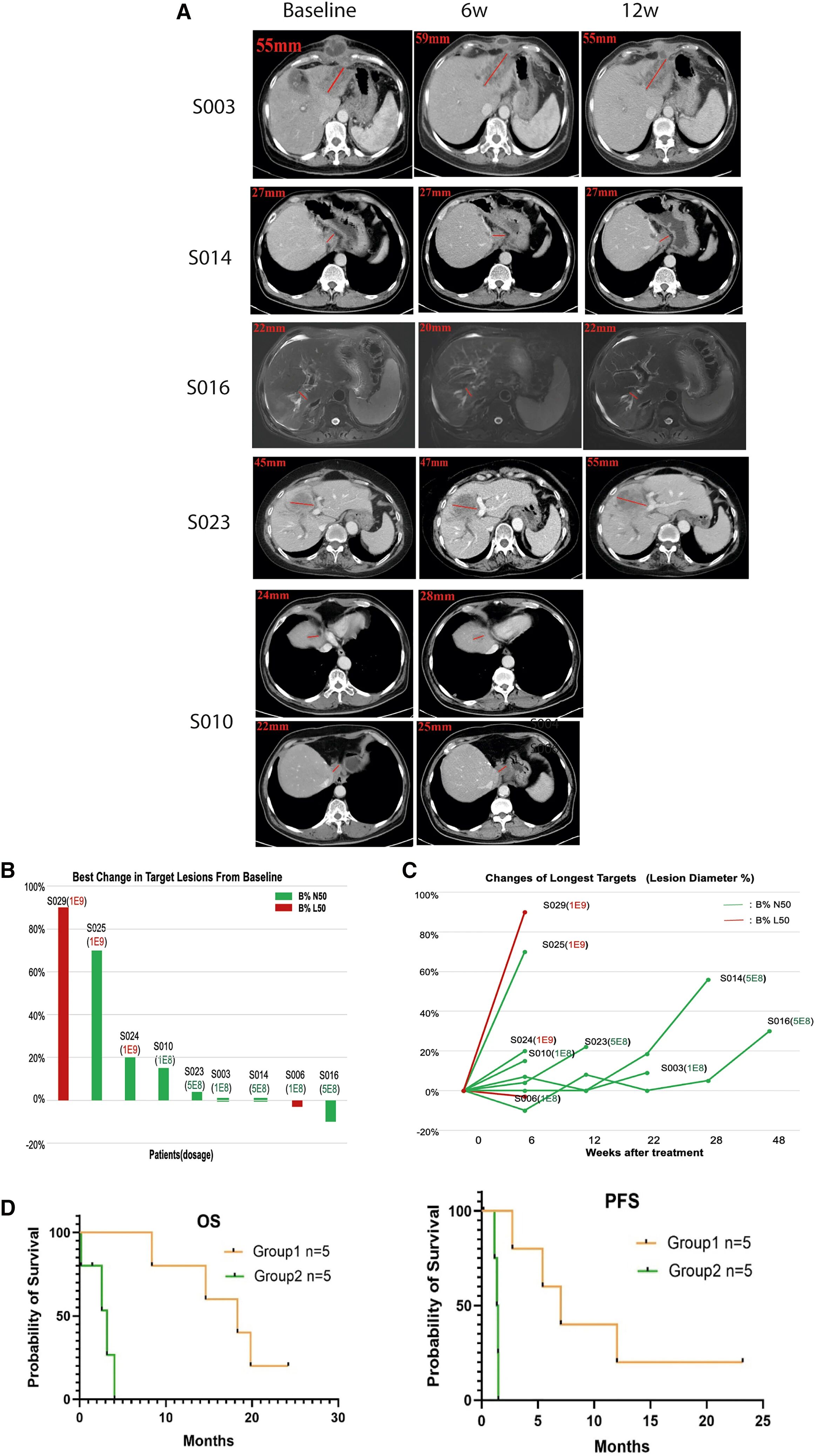
ScTILs治疗的疗效分析
安全性良好,无需化疗清淋
与传统TILs疗法相比,ScTILs具有明显优势:未发生细胞因子释放综合征(CRS)或神经毒性(ICANS)等严重不良反应;无需化疗清淋或大剂量白细胞介素2(IL2)支持,避免了相关毒性,提升了安全性和患者生活质量。对B细胞的影响为一过性、可逆的,12周内可恢复正常,不影响免疫功能。
研究结论
ScTILs代表了一种更具可行性、安全性和有效性的实体瘤细胞治疗新策略。随着进一步优化和扩大临床验证,未来有望成为晚期胆道癌的重要治疗选择。目前该研究存在样本量较小、缺乏对照组等局限,但无疑为胆管癌乃至其他实体瘤的患者带来了新的希望。
参考文献
Wan X, Zhao J, Yang X, Mou X, Liu B, Gao B, Gu W, Zhao H. Therapeutic T cells with 3-in-1 strategy for the treatment of biliary tract cancer. Cell Rep Med. 2025 Sep 18:102349. doi: 10.1016/j.xcrm.2025.102349. Epub ahead of print. PMID: 40972581.
来源:肿瘤界